解题方法
1 . 以下说法中正确的是
| A.冰在室温下自动熔化成水,是熵增的过程 |
| B.高锰酸钾加热分解是一个熵减小的过程 |
| C.放热过程(△H<0)或熵增加(△S>0)的过程一定是自发的 |
| D.自发进行的反应一定能迅速进行 |
您最近一年使用:0次
2 . 下列说法正确的是
| A.活化分子的每一次碰撞都能够发生化学反应 |
| B.催化剂可以降低反应的活化能,加快反应速率 |
| C.反应物用量增加后,有效碰撞次数一定增多,反应速率增大 |
| D.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H<0 |
您最近一年使用:0次
2022-09-14更新
|
157次组卷
|
2卷引用:湖南省岳阳市华容县2021-2022学年高二上学期期末教学质量监测化学试题
11-12高二下·安徽六安·单元测试
名校
解题方法
3 . 拿破仑在俄国时,当时法国士兵军服的纽扣都是用金属锡做的。灰锡结构松散,不能用于制造器皿,而白锡结构坚固,可以制造器皿。试分析现把白锡制成的器皿放在0℃、100kPa的室内存放,它会不会变成灰锡而不能再继续使用?已知:在0℃、100kPa条件下白锡转化为灰锡反应的焓变和熵变分别为ΔH=-2.1809kJ·mol-1,ΔS=-6.6J·mol-1·K-1。
| A.会变 | B.不会变 | C.不能确定 | D.升高温度才会变 |
您最近一年使用:0次
2022-09-14更新
|
289次组卷
|
18卷引用:2016-2017学年湖南省衡阳一中高二上10月月考化学卷
2016-2017学年湖南省衡阳一中高二上10月月考化学卷(已下线)2011-2012学年安徽省舒城晓天中学高二下学期质量测试1化学试卷(已下线)2018年10月25日 《每日一题》人教选修4--化学反应方向的判断山西省运城市2019-2020学年高二上学期期末调研测试化学试题(已下线)第02章 化学反应速率与化学平衡(A卷基础强化篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)吉林省白城市第一中学2021-2022学年高二上学期9月阶段考试化学试题福建省三明第一中学2021-2022学年高二上学期第一次月考化学试题黑龙江省牡丹江市海林市朝鲜族中学2021-2022学年上学期高二10月月考化学试题福建省莆田市擢英中学2021-2022学年高二上学期第一次月考化学试卷(已下线)必考点04 化学反应的方向和调控-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)福建省福州第一中学2021-2022学年高二上学期期中考试化学试题山东省青岛市第十九中学2021-2022学年高二上学期10月月考化学试题安徽省池州市贵池区2021-2022学年高二上学期期中考试化学试题福建省三明市四地四校2021-2022学年高二上学期期中联考协作卷化学试题安徽省池州市贵池区2021-2022学年高二上学期期中考试化学试题内蒙古自治区呼伦贝尔市鄂温克族自治旗第三中学2021-2022学年高二上学期第一次月考化学试题(已下线)第07讲 化学反应的方向-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)(已下线)第28练 化学反应的方向-2023年高考化学一轮复习小题多维练(全国通用)
名校
解题方法
4 . 用 催化还原
催化还原 ,可以消除氮氧化物的污染。已知:
,可以消除氮氧化物的污染。已知:
①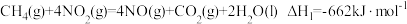
②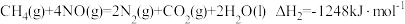
下列说法正确的是
 催化还原
催化还原 ,可以消除氮氧化物的污染。已知:
,可以消除氮氧化物的污染。已知:①
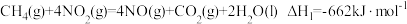
②
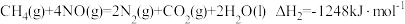
下列说法正确的是
| A.反应②在低温下不能自发进行 |
B.若反应①中消耗 (标准状况下) (标准状况下) ,则放出 ,则放出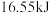 热量 热量 |
C.生成相同物质的量的 ,反应①②中转移的电子数不相同 ,反应①②中转移的电子数不相同 |
D.若用标准状况下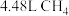 还原 还原 只生成 只生成 和 和 ,则放出的热量为 ,则放出的热量为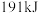 |
您最近一年使用:0次
2022-09-02更新
|
211次组卷
|
5卷引用:湖南省部分学校2022-2023学年高二8月联考化学试题
名校
解题方法
5 . 下列在常温下不能自发进行且是熵增过程的反应为
| A.工业合成氨的反应 | B.碳与二氧化碳的反应 |
| C.碳酸氢钠与盐酸的反应 | D.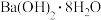 与 与 的反应 的反应 |
您最近一年使用:0次
2022-09-02更新
|
145次组卷
|
2卷引用:湖南省部分学校2022-2023学年高二8月联考化学试题
名校
解题方法
6 . 高中化学《化学反应原理》模块从不同的视角对化学反应进行了探究、分析,以下观点中不正确 的是
| A.难溶电解质在水中达到溶解平衡时,再加入难溶电解质,溶液中各离子浓度不变 |
B.将 加入水中并加热使其转化为 加入水中并加热使其转化为 |
C.乙烯聚合为聚乙烯的反应是熵减的过程,却能够自发进行,可知该反应的 |
D. 溶液显碱性的原因: 溶液显碱性的原因: |
您最近一年使用:0次
2022-09-02更新
|
587次组卷
|
5卷引用:湖南省郴州市2021-2022学年高二上学期期末考试化学试题
7 . 治理汽车尾气排放的NO、CO的办法是在汽车排气管上安装催化转化器,使NO与CO反应生成可参与大气生态循环的无毒气体,反应原理: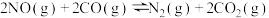 ,在298K、100kPa下,
,在298K、100kPa下,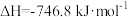 ,
,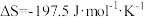 。下列说法错误的是
。下列说法错误的是
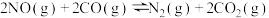 ,在298K、100kPa下,
,在298K、100kPa下,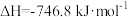 ,
,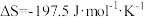 。下列说法错误的是
。下列说法错误的是| A.该反应为熵减小的反应 |
| B.该反应中反应物的总能量高于生成物的总能量 |
| C.该反应在任何条件下都不能自发进行 |
| D.其他条件不变时,加入催化剂,可以改变化学反应方向 |
您最近一年使用:0次
2022-09-01更新
|
397次组卷
|
2卷引用:湖南省长沙市湖南师范大学附属中学2022-2023学年高二上学期入学考试化学试题
解题方法
8 . 氮及其化合物与人类生产生活息息相关。
(1)氮气在雷电的作用下,生成氮的氧化物,再经复杂变化形成能供给植物营养的硝酸盐。涉及的部分反应:
I.2NO2(g)+H2O(l)=HNO3(aq)+HNO2(aq) △H1=-116.1 kJ·mol-1;
II.HNO3(aq)+2NO(g)+H2O(l)=3HNO2(aq) △H2=-75.9 kJ·mol-1;
III.3NO2(g)+H2O(l)=2HNO3(aq)+NO(g) △H3;
①△H3=____ kJ·mol-1。
②将两个充有等量NO2的A、B烧瓶,分别放入两个盛有等量的水的烧杯中,待气体颜色稳定后,若向右边的烧杯中加入5.0 g硝酸铵晶体,实验装置如图所示(略去铁架台等),则观察到B烧瓶中气体颜色____ (填“变深”、“不变”或“变浅”),其原因是_______ 。

(2)氮气是生产氮肥的主要原料。
①实验室可用氯化铵与消石灰反应制备少量NH3。
2NH4Cl(s)+Ca(OH)2(s)=CaCl2(s)+2NH3(g)+2H2O(g) △H>0,该反应在____ (填“高温”、“低温”或“任何温度”)下能自发进行,说明理由:____ 。
②已知N2(g)+3H2(g) 2NH3(g) △H=-92.4 kJ·mol-1,工业合成氨通常选择30MPa左右,700K左右,以铁触媒为催化剂,分析工业合成氨时不选用更高的压强或更高的温度的可能原因:
2NH3(g) △H=-92.4 kJ·mol-1,工业合成氨通常选择30MPa左右,700K左右,以铁触媒为催化剂,分析工业合成氨时不选用更高的压强或更高的温度的可能原因:____ 。
(3)CO和NO是汽车尾气中的主要污染物,将它们转化为无害物质是重要的研究课题。
已知:在25℃时,
IV.2NO(g) N2(g)+O2(g) △H4=-180.5 kJ·mol-1 K4
N2(g)+O2(g) △H4=-180.5 kJ·mol-1 K4
V.CO(g)+ O2(g)
O2(g) CO2(g) △H5=-283.0 kJ·mol-1K5
CO2(g) △H5=-283.0 kJ·mol-1K5
①25℃时,反应2NO(g)+2CO(g) N2(g)+2CO2(g)的平衡常数K6=
N2(g)+2CO2(g)的平衡常数K6=____ (填含K4、K5的代数式)。
②在某恒温恒压的条件下,向密闭容器中充入2 mol NO和2 mol CO,仅发生反应2NO(g)+2CO(g) N2(g)+2CO2(g),此时混合气体的总体积为1 L,在t1时刻达到平衡状态,此时NO的转化率为40%,则该条件下的平衡常数K′6=
N2(g)+2CO2(g),此时混合气体的总体积为1 L,在t1时刻达到平衡状态,此时NO的转化率为40%,则该条件下的平衡常数K′6=____ (保留两位有效数字)。
(1)氮气在雷电的作用下,生成氮的氧化物,再经复杂变化形成能供给植物营养的硝酸盐。涉及的部分反应:
I.2NO2(g)+H2O(l)=HNO3(aq)+HNO2(aq) △H1=-116.1 kJ·mol-1;
II.HNO3(aq)+2NO(g)+H2O(l)=3HNO2(aq) △H2=-75.9 kJ·mol-1;
III.3NO2(g)+H2O(l)=2HNO3(aq)+NO(g) △H3;
①△H3=
②将两个充有等量NO2的A、B烧瓶,分别放入两个盛有等量的水的烧杯中,待气体颜色稳定后,若向右边的烧杯中加入5.0 g硝酸铵晶体,实验装置如图所示(略去铁架台等),则观察到B烧瓶中气体颜色

(2)氮气是生产氮肥的主要原料。
①实验室可用氯化铵与消石灰反应制备少量NH3。
2NH4Cl(s)+Ca(OH)2(s)=CaCl2(s)+2NH3(g)+2H2O(g) △H>0,该反应在
②已知N2(g)+3H2(g)
 2NH3(g) △H=-92.4 kJ·mol-1,工业合成氨通常选择30MPa左右,700K左右,以铁触媒为催化剂,分析工业合成氨时不选用更高的压强或更高的温度的可能原因:
2NH3(g) △H=-92.4 kJ·mol-1,工业合成氨通常选择30MPa左右,700K左右,以铁触媒为催化剂,分析工业合成氨时不选用更高的压强或更高的温度的可能原因:(3)CO和NO是汽车尾气中的主要污染物,将它们转化为无害物质是重要的研究课题。
已知:在25℃时,
IV.2NO(g)
 N2(g)+O2(g) △H4=-180.5 kJ·mol-1 K4
N2(g)+O2(g) △H4=-180.5 kJ·mol-1 K4V.CO(g)+
 O2(g)
O2(g) CO2(g) △H5=-283.0 kJ·mol-1K5
CO2(g) △H5=-283.0 kJ·mol-1K5①25℃时,反应2NO(g)+2CO(g)
 N2(g)+2CO2(g)的平衡常数K6=
N2(g)+2CO2(g)的平衡常数K6=②在某恒温恒压的条件下,向密闭容器中充入2 mol NO和2 mol CO,仅发生反应2NO(g)+2CO(g)
 N2(g)+2CO2(g),此时混合气体的总体积为1 L,在t1时刻达到平衡状态,此时NO的转化率为40%,则该条件下的平衡常数K′6=
N2(g)+2CO2(g),此时混合气体的总体积为1 L,在t1时刻达到平衡状态,此时NO的转化率为40%,则该条件下的平衡常数K′6=
您最近一年使用:0次
2022-08-23更新
|
186次组卷
|
3卷引用:湖南省岳阳市2022-2023学年高二下学期6月期末考试化学试题
解题方法
9 . CH3OH和CH3CH2OH均是重要的有机合成原料、溶剂、燃料等。Cu2O可催化CH3OCH3制备CH3OH和CH3CH2OH。已知:
反应1:CH3OCH3(g)+CO(g) CH3COOCH3(g) △H1=akJ ·mol-1
CH3COOCH3(g) △H1=akJ ·mol-1
反应2: CH3COOCH3(g)+H2(g)
CH3COOCH3(g)+H2(g) 
 CH3OH(g)+
CH3OH(g)+  CH3CH2OH(g) △H2=b kJ·mol-1
CH3CH2OH(g) △H2=b kJ·mol-1
(1)CH3OCH3(g) +CO(g) +2H2(g) CH3OH(g) +CH3CH2OH(g)△H=。
CH3OH(g) +CH3CH2OH(g)△H=。 _______ (用含a、b的代数式表示)kJ·mol-1。
(2)在某恒容容器中发生反应1和反应2,达到平衡时,体系中物质的百分含量与温度的关系如图所示。由此推知,△H1_______ (填“>”、“<”或“=”,下同)0,△H2_______ 0。
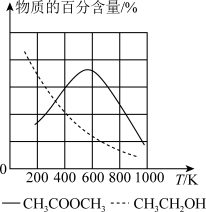
(3)T1 K时,向2 L恒容密闭容器中充入1 mol CH3OCH3(g)、1 molCO(g)、2 mol H2(g) ,发生反应:CH3OCH3(g)+CO(g) +2H2(g) CH3OHg)+CH3CH2OH(g),10 min时反应达到平衡,此时CH3OH(g)的体积分数为
CH3OHg)+CH3CH2OH(g),10 min时反应达到平衡,此时CH3OH(g)的体积分数为 ,容器内压强为p MPa。
,容器内压强为p MPa。
①0~10 min内,v(CH3OCH3)=_______ mol·L-1·min-1,平衡后,c(CH3CH2OH) = _______ mol·L-1,Kp=_______ MPa-2(分压=总压×物质的量分数)。
②若将该反应置于温度为T2K下进行,Kp2>Kp1则T2_______ (填“>”或“<”)T1,该反应在_______ (填“ 高温”“低温”或“任意温度”)条件下更有利于自发进行。
③下到说法能判断该反应达到平衡状态的是_______ (填标号)。
A.消耗1molCO时,生成1mol CH3OH
B.CH3CH2OH的浓度不再发生改变
C.混合气体的密度不变
D.容器压强不变
反应1:CH3OCH3(g)+CO(g)
 CH3COOCH3(g) △H1=akJ ·mol-1
CH3COOCH3(g) △H1=akJ ·mol-1反应2:
 CH3COOCH3(g)+H2(g)
CH3COOCH3(g)+H2(g) 
 CH3OH(g)+
CH3OH(g)+  CH3CH2OH(g) △H2=b kJ·mol-1
CH3CH2OH(g) △H2=b kJ·mol-1(1)CH3OCH3(g) +CO(g) +2H2(g)
 CH3OH(g) +CH3CH2OH(g)△H=。
CH3OH(g) +CH3CH2OH(g)△H=。 (2)在某恒容容器中发生反应1和反应2,达到平衡时,体系中物质的百分含量与温度的关系如图所示。由此推知,△H1

(3)T1 K时,向2 L恒容密闭容器中充入1 mol CH3OCH3(g)、1 molCO(g)、2 mol H2(g) ,发生反应:CH3OCH3(g)+CO(g) +2H2(g)
 CH3OHg)+CH3CH2OH(g),10 min时反应达到平衡,此时CH3OH(g)的体积分数为
CH3OHg)+CH3CH2OH(g),10 min时反应达到平衡,此时CH3OH(g)的体积分数为 ,容器内压强为p MPa。
,容器内压强为p MPa。①0~10 min内,v(CH3OCH3)=
②若将该反应置于温度为T2K下进行,Kp2>Kp1则T2
③下到说法能判断该反应达到平衡状态的是
A.消耗1molCO时,生成1mol CH3OH
B.CH3CH2OH的浓度不再发生改变
C.混合气体的密度不变
D.容器压强不变
您最近一年使用:0次
2022-07-10更新
|
225次组卷
|
2卷引用:湖南省衡阳市部分校2021-2022学年高二下学期期末考试化学试题
10-11高二上·吉林·阶段练习
名校
解题方法
10 . 知道了某过程有自发性之后,则
| A.可判断出过程的方向 | B.可确定过程是否一定会发生 |
| C.可预测过程发生完成的快慢 | D.可判断过程的热效应 |
您最近一年使用:0次
2022-07-09更新
|
484次组卷
|
29卷引用:2014-2015学年湖南省娄底市高二上学期期中联考化学试卷
(已下线)2014-2015学年湖南省娄底市高二上学期期中联考化学试卷(已下线)2010年吉林省东北师大附中高二上学期第一次月考(化学)(已下线)2011-2012年山东省莒南县三中高二上学期期中考试化学试卷(已下线)2011-2012学年云南省蒙自县文澜高级中学高二上学期期中考试化学试卷(已下线)2011-2012学年陕西师大附中高二年级第一学期期中考试化学试卷(已下线)2012年人教版高中化学选修4 2.4化学反应进行的方向练习卷(已下线)2012-2013学年广东省汕头市金山中学高二上学期期末考试化学试卷(已下线)2013-2014学年陕西省岐山县高二上学期期中质量检测理科化学试卷(已下线)2015安徽望江中学同步课时练(人教选修4)2.4化学反应进行的方向2016-2017学年黑龙江省大庆市杜蒙县高二上月考一化学卷河北省承德市第一中学2017-2018学年高二上学期第一次月考化学试题(已下线)2019年9月24日 《每日一题》选修4—— 自发过程与自发反应福建省厦门外国语学校2019-2020学年高二上学期期中考试化学试题云南省屏边县第一中学2019-2020学年高二上学期12月月考化学试题云南省陇川县民族中学2019-2020学年高二上学期期末考试化学试题山西省阳泉市2019-2020学年高二上学期期末考试化学试题云南省曲靖市富源县第六中学2019-2020学年高二上学期期末考试化学试题(已下线)2.2.1 化学反应的方向(基础练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)(已下线)2.3 化学反应的方向(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第三节 化学反应的方向 教材帮(已下线)2.2.1 化学反应的方向(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)2.3 化学反应进行的方向——同步学习必备知识第三节 化学反应的方向第1节 化学反应的方向(已下线)2011-2012学年陕西省师大附中高一下学期期末考试化学试卷2016届黑龙江省牡丹江一中高三上学期10月月考化学试卷(已下线)考点24 化学反应的方向-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点24 化学反应的方向(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)上海市向明中学 2023-2024学年高三上学期9月质量监控化学试题



