名校
解题方法
1 . 下列关于焓判据和熵判据的说法中,不正确的是
| A.放热的自发过程可能是熵减小的过程,吸热的自发过程一定为熵增加的过程 |
| B.由能量判据(以焓变为基础)和熵判据组合成的复合判据,将更适合于所有的过程 |
| C.对于孤立体系,自发过程向着熵增的方向进行 |
D.反应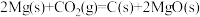 能自发进行,则该反应的 能自发进行,则该反应的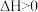 |
您最近一年使用:0次
2022-10-12更新
|
181次组卷
|
2卷引用:重庆市万州第二高级中学2022-2023学年高二上学期10月月考化学试题
名校
2 . 下列说法不正确的是
| A.NaHCO3(aq) +HCl(aq)=NaCl(aq)+CO2(g)+H2O(l) ΔH1=+31.4kJ·mol-1,是一个吸热反应,但反应能自发进行 |
| B.对于同一物质在不同状态时的熵值是:气态>液态>固态 |
| C.自发反应在常温下一定能实现 |
| D.化学反应的焓变与其反应的方向有关 |
您最近一年使用:0次
3 . 通过以下反应均可获取H2,下列有关说法正确的是
①太阳光催化分解水制氢:2H2O(l) = 2H2(g) + O2(g) ΔH1=+571.6 kJ·mol-1
②焦炭与水反应制氢:C(s) + H2O(g) = CO(g) + H2(g) ΔH2=+131.3 kJ·mol-1
③甲烷与水反应制氢:CH4(g) + H2O(g) = CO(g) + 3H2(g) ΔH3=+206.1 kJ·mol-1
①太阳光催化分解水制氢:2H2O(l) = 2H2(g) + O2(g) ΔH1=+571.6 kJ·mol-1
②焦炭与水反应制氢:C(s) + H2O(g) = CO(g) + H2(g) ΔH2=+131.3 kJ·mol-1
③甲烷与水反应制氢:CH4(g) + H2O(g) = CO(g) + 3H2(g) ΔH3=+206.1 kJ·mol-1
| A.反应①可知,氢气的燃烧热为571.6kJ·mol-1 |
| B.反应②为吸热反应,不能自发进行 |
| C.反应③使用催化剂,∆H3减小 |
| D.反应CH4(g) = C(s) + 2H2(g) 的∆H=+74.8 kJ·mol-1 |
您最近一年使用:0次
2022-08-16更新
|
291次组卷
|
2卷引用:重庆市第七中学校2021-2022学年高二上学期第二次月考化学试题
名校
4 . 可逆反应中生成物C的体积分数(C%)与压强(P)、温度(T)的关系如图所示,关于该反应的判断正确的是
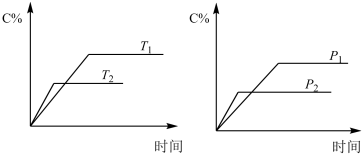

| A.该反应不能自发 | B.该反应能自发进行 |
| C.△H>0,△S>0 | D.△H<0,△S<0 |
您最近一年使用:0次
5 . I.回答下列问题:
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气。C(s)+H2O(g) H2(g)+CO(g),△H=+131.3kJ·mol-1,△S=+133.7J·mol-1·K-1,该反应在低温下
H2(g)+CO(g),△H=+131.3kJ·mol-1,△S=+133.7J·mol-1·K-1,该反应在低温下_______ (填“能”或“不能”)自发进行。
(2)已知在400℃时,N2(g)+3H2(g) 2NH3(g)的K=0.5。
2NH3(g)的K=0.5。
①在400℃时,2NH3(g) N2(g)+3H2(g)的K′=
N2(g)+3H2(g)的K′=_______ (填数值)。
②400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v正(N2)_______ (填“>”“<”“=”或“不确定”)v逆(N2)。
③若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡_______ (填“向左”“向右”或“不”)移动;使用催化剂_______ (填“增大”“减小”或“不改变”)反应的△H。
Ⅱ.目前工业合成氨的原理是N2(g)+3H2(g) 2NH3(g)。在一定温度下,将1molN2和3molH2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol。
2NH3(g)。在一定温度下,将1molN2和3molH2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol。
(3)达平衡时,H2的转化率α1=_______ 。
(4)判断反应达到平衡的依据为_______ (填字母代号)。
a.压强不随时间改变
b.气体的密度不随时间改变
c.c(N2)不随时间改变
d.单位时间里生成N2和NH3的物质的量相等
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气。C(s)+H2O(g)
 H2(g)+CO(g),△H=+131.3kJ·mol-1,△S=+133.7J·mol-1·K-1,该反应在低温下
H2(g)+CO(g),△H=+131.3kJ·mol-1,△S=+133.7J·mol-1·K-1,该反应在低温下(2)已知在400℃时,N2(g)+3H2(g)
 2NH3(g)的K=0.5。
2NH3(g)的K=0.5。①在400℃时,2NH3(g)
 N2(g)+3H2(g)的K′=
N2(g)+3H2(g)的K′=②400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v正(N2)
③若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡
Ⅱ.目前工业合成氨的原理是N2(g)+3H2(g)
 2NH3(g)。在一定温度下,将1molN2和3molH2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol。
2NH3(g)。在一定温度下,将1molN2和3molH2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol。(3)达平衡时,H2的转化率α1=
(4)判断反应达到平衡的依据为
a.压强不随时间改变
b.气体的密度不随时间改变
c.c(N2)不随时间改变
d.单位时间里生成N2和NH3的物质的量相等
您最近一年使用:0次
2022-05-06更新
|
143次组卷
|
2卷引用:重庆市巫山县官渡中学2021-2022学年高二下学期期末考试化学试题
名校
解题方法
6 . 一定条件下用甲烷可以消除氮氧化物(NOx)的污染。
已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
下列选项正确的是
已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
下列选项正确的是
| A.CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l) ΔH=-867 kJ·mol-1 |
| B.若把反应①设计为燃料电池,在碱性条件下负极的电极反应式为:CH4-8e-+8OH-=CO2+6H2O |
| C.反应①在任何温度下都能自发进行 |
| D.在其他条件不变的情况下,增大压强有利于提高氮氧化物的消除率 |
您最近一年使用:0次
名校
解题方法
7 . 下列说法正确的是
| A.用广泛pH试纸测某盐酸的pH=2.3 |
| B.某醋酸溶液的pH=a,将此溶液稀释100倍后,溶液的pH=b,则a > b-2 |
| C.常温下反应2Na2SO3(s)+O2(g)=2Na2SO4(s)能自发进行,则ΔH>0 |
| D.增大压强(对于气体反应),活化分子百分数增大,故反应速率增大 |
您最近一年使用:0次
2022-04-05更新
|
945次组卷
|
3卷引用:重庆市杨家坪中学2021-2022学年高二上学期第二次月考化学试题
8 . 下列关于反应热和热化学反应的描述中正确的是
| A.中和热为57.3 kJ∙mol−1,则浓H2SO4和NaOH反应的反应热为ΔH=−114.6 kJ∙mol−1 |
| B.2H2(g)+O2(g)=2H2O(g) △H1;2H2(g)+O2(g)=2H2O(l) △H2,则△H1>△H2 |
| C.2CO(g)+O2(g)=2CO2(g) ΔH=−283.0 kJ∙mol−1,则CO(g)的燃烧热是283.0 kJ∙mol−1 |
D.CH3Cl(g)+Cl2(g)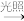 CH2Cl2(l)+HCl(g)常温下能自发进行,则该反应的ΔH>0 CH2Cl2(l)+HCl(g)常温下能自发进行,则该反应的ΔH>0 |
您最近一年使用:0次
名校
9 . 反应N2O4(g) 2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是

 2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
| A.A、B两点可知,T2<T1 |
| B.从A点变到C点,平衡逆移,气体的颜色:A深,C浅 |
| C.该反应ΔH>0,ΔS>0,高温下可以自发进行,室温下不能自发进行 |
D.B、C两点气体的平均相对分子质量: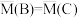 |
您最近一年使用:0次
2022-03-30更新
|
309次组卷
|
4卷引用:重庆市主城区六校2020-2021学年高二上学期期末联考化学试题
重庆市主城区六校2020-2021学年高二上学期期末联考化学试题重庆市铜梁一中等三校2022-2023学年高二上学期期末考试化学试题(已下线)2.3 化学反应的方向-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)四川省广安市华蓥中学2023-2024学年高二下学期开学化学试题
名校
10 . 多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃时(各物质均为气态),CH3OH与水在铜催化剂上的反应机理和能量变化如图:
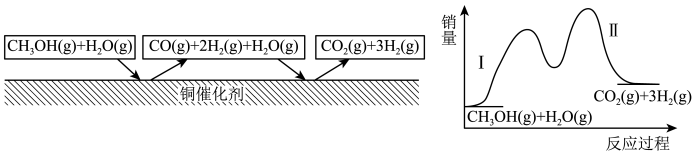
下列说法正确的是

下列说法正确的是
| A.总反应CH3OH(g)+H2O(g)=CO2(g)+3H2(g)有熵减的趋势,即ΔS<0 |
| B.1molCH3OH(g)和1molH2O(g)的总能量大于1molCO2(g)和3molH2(g)的总能量 |
| C.反应II的热化学方程式为CO(g)+H2O(g)=H2(g)+CO2(g) ΔH=-akJ·mol-1(a>0) |
| D.选择合适的催化剂可降低反应I和II的活化能,改变总反应的焓变 |
您最近一年使用:0次
2022-03-25更新
|
303次组卷
|
3卷引用:重庆市主城区六校2021-2022学年高二上学期期末联考化学试题
重庆市主城区六校2021-2022学年高二上学期期末联考化学试题浙江金华第一中学2022-2023学年高二上学期12月月考化学试题(已下线)押全国卷理综第13题 反应机理图分析、能垒图分析等创新题型及阿伏加德罗常数-备战2022年高考化学临考题号押题(全国卷)



