名校
1 . 硫元素形成的化合物有着广泛的用途,其中过二硫酸 是一种强氧化剂,可用作氧化剂和漂白剂,过二硫酸及其盐都是不稳定的,加热时分解,溶于水会发生一定程度的水解,电解硫酸钾溶液可得过二硫酸钾。下列说法不正确的是
是一种强氧化剂,可用作氧化剂和漂白剂,过二硫酸及其盐都是不稳定的,加热时分解,溶于水会发生一定程度的水解,电解硫酸钾溶液可得过二硫酸钾。下列说法不正确的是
 是一种强氧化剂,可用作氧化剂和漂白剂,过二硫酸及其盐都是不稳定的,加热时分解,溶于水会发生一定程度的水解,电解硫酸钾溶液可得过二硫酸钾。下列说法不正确的是
是一种强氧化剂,可用作氧化剂和漂白剂,过二硫酸及其盐都是不稳定的,加热时分解,溶于水会发生一定程度的水解,电解硫酸钾溶液可得过二硫酸钾。下列说法不正确的是A. 中硫的化合价为+6 中硫的化合价为+6 |
B. 分解的化学方程式可能为: 分解的化学方程式可能为: |
C.过二硫酸铵溶液可用于检验溶液中的 Mn2+,现象为溶液变为紫红色。该反应的离子方程式为 |
D.用惰性电极电解K2SO4溶液制取 时的阳极反应方程式为 时的阳极反应方程式为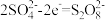 |
您最近一年使用:0次
解题方法
2 . 锌的用途广泛,主要用于镀锌板及精密铸造等行业。以粗氧化锌(主要成分为ZnO及少量Fe2O3、CuO、MnO、SiO2)为原料制备锌的工艺流程如图所示:
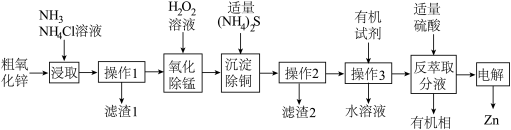
已知:①“浸取”时。ZnO、 CuO转化为[ Zn(NH3)4]2+、[Cu(NH3)4]2+进入溶液:
②25℃时,Ksp(CuS)=6.4×10-36, Ksp(ZnS)=1.6 ×10-24;
③沉淀除铜标准:溶液中 ≤2.0×10-6
≤2.0×10-6
回答下列问题:
(1)“滤渣1”的主要成分为Fe(OH)3、Mn(OH)2和___________ (填化学式),“ 操作3”的名称为___________ 。
(2)“氧化除锰”时,H2O2将Mn2+转化为难溶的MnO2,该反应的离子方程式为___________ 。
(3)“沉淀除铜”时,锌的最终回收率、除铜效果[除铜效果以反应后溶液中铜锌比 表示] 与“(NH4)2 S加入量”[以
表示] 与“(NH4)2 S加入量”[以 表示]的关系曲线如图所示。
表示]的关系曲线如图所示。
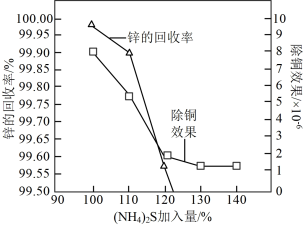
①当(NH4)2S加入量≥100%时,锌的最终回收率下降的原因是___________ (用离子方程式表示),该反应的平衡常数为___________ 。(已知) [ Zn(NH3)4]2+的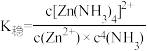 =2. 9 ×109]
=2. 9 ×109]
②“沉淀除铜”时(NH4 )2S加入量最好应选___________ 。
a.100% b.110% c.120% d.130%
(4)电解后溶液中的溶质主要成分是___________ , 可用于循环使用。

已知:①“浸取”时。ZnO、 CuO转化为[ Zn(NH3)4]2+、[Cu(NH3)4]2+进入溶液:
②25℃时,Ksp(CuS)=6.4×10-36, Ksp(ZnS)=1.6 ×10-24;
③沉淀除铜标准:溶液中
 ≤2.0×10-6
≤2.0×10-6回答下列问题:
(1)“滤渣1”的主要成分为Fe(OH)3、Mn(OH)2和
(2)“氧化除锰”时,H2O2将Mn2+转化为难溶的MnO2,该反应的离子方程式为
(3)“沉淀除铜”时,锌的最终回收率、除铜效果[除铜效果以反应后溶液中铜锌比
 表示] 与“(NH4)2 S加入量”[以
表示] 与“(NH4)2 S加入量”[以 表示]的关系曲线如图所示。
表示]的关系曲线如图所示。
①当(NH4)2S加入量≥100%时,锌的最终回收率下降的原因是
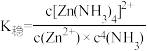 =2. 9 ×109]
=2. 9 ×109]②“沉淀除铜”时(NH4 )2S加入量最好应选
a.100% b.110% c.120% d.130%
(4)电解后溶液中的溶质主要成分是
您最近一年使用:0次
3 . 铌是汽车和飞机制造业特别重要的材料,具有良好的耐腐蚀、冷热加工等性能,以高钛渣(含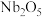 、
、 、
、 、CaO)为原料制取单质的流程如图甲所示:
、CaO)为原料制取单质的流程如图甲所示:


已知:①MIBK为甲基异丁基酮;②钽铌液中含有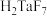 、
、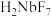 均为弱酸;③
均为弱酸;③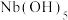 难溶于水。
难溶于水。
(1)酸溶时, 发生的反应的离子方程式为
发生的反应的离子方程式为_______ 。
(2)酸溶时,HF的浓度对铌、钽的浸出率的影响如图丙所示,则HF的最佳浓度为_______  。
。
(3)沉铌时,发生的反应的化学方程式为_______ 。
(4)电解制备铌的原理如图乙所示,阴极发生的电极反应为_______ 。
(5)铌(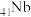 )和镍合金的用途非常广泛,Nb、Ni互化物的晶胞结构如图所示:
)和镍合金的用途非常广泛,Nb、Ni互化物的晶胞结构如图所示:

①铌元素位于周期表中的位置是_______ 。
②图中Nb原子与Ni原子的最短距离为_______ nm。
③Nb、Ni互化物晶体的密度为_______ 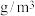 (列出计算式)。
(列出计算式)。
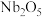 、
、 、
、 、CaO)为原料制取单质的流程如图甲所示:
、CaO)为原料制取单质的流程如图甲所示:

已知:①MIBK为甲基异丁基酮;②钽铌液中含有
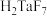 、
、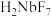 均为弱酸;③
均为弱酸;③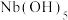 难溶于水。
难溶于水。(1)酸溶时,
 发生的反应的离子方程式为
发生的反应的离子方程式为(2)酸溶时,HF的浓度对铌、钽的浸出率的影响如图丙所示,则HF的最佳浓度为
 。
。(3)沉铌时,发生的反应的化学方程式为
(4)电解制备铌的原理如图乙所示,阴极发生的电极反应为
(5)铌(
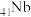 )和镍合金的用途非常广泛,Nb、Ni互化物的晶胞结构如图所示:
)和镍合金的用途非常广泛,Nb、Ni互化物的晶胞结构如图所示:
①铌元素位于周期表中的位置是
②图中Nb原子与Ni原子的最短距离为
③Nb、Ni互化物晶体的密度为
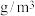 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
名校
解题方法
4 . 电化学原理在现代工业中应用广泛,回答下列问题:
(1)氯碱工业上利用电解精制饱和食盐水的方法制取氯气、氯气、烧碱和氯的含氧酸盐等一系列化工产品,如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
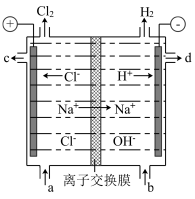
①离子交换膜的作用为___________ 、___________ 。
②氯氧化钠溶液从图中___________ (填“a”“b”“c”或“d”)处收集。
(2) 可作超级电容器材料。用惰性电极电解
可作超级电容器材料。用惰性电极电解 溶液制得
溶液制得 ,其阳极的电极反应式为
,其阳极的电极反应式为___________ 。
(3)金属镍有广泛的用途,粗镍中含有少量的Fe、Zn、Cu、Pt等杂质,故可用电解法制备高纯度的镍。(金属活动性: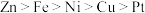 )
)
①电解过程中,阳极杂质的电极反应式为___________ 。
②电解过程中,阳极减少的质量与阴极增加的质量___________ (填“相等”或“不相等”),电解结束后,Pt以___________ 形式存在。
(4)图甲是一种将废水中的氯乙烯(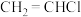 )进行环境无害化处理的微生物电池装置,同时利用此装置在铁上镀铜。
)进行环境无害化处理的微生物电池装置,同时利用此装置在铁上镀铜。
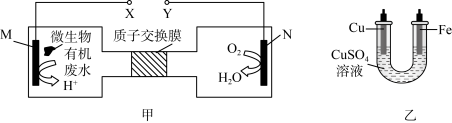
①M为___________ (填“正极”“负极”“阴极”或“阳极”),镀铜时,___________ (填“X”或“Y”)与铁电极相连,工作过程中,N极区域溶液中pH将___________ (填“增大”“减小”或“不变”)。
②若M极消耗0.1mol氯乙烯,则铁电极增重___________ g,硫酸铜溶液的浓度将___________ (填“增大”“减小”或“不变”)。
(1)氯碱工业上利用电解精制饱和食盐水的方法制取氯气、氯气、烧碱和氯的含氧酸盐等一系列化工产品,如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。

①离子交换膜的作用为
②氯氧化钠溶液从图中
(2)
 可作超级电容器材料。用惰性电极电解
可作超级电容器材料。用惰性电极电解 溶液制得
溶液制得 ,其阳极的电极反应式为
,其阳极的电极反应式为(3)金属镍有广泛的用途,粗镍中含有少量的Fe、Zn、Cu、Pt等杂质,故可用电解法制备高纯度的镍。(金属活动性:
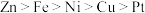 )
)①电解过程中,阳极杂质的电极反应式为
②电解过程中,阳极减少的质量与阴极增加的质量
(4)图甲是一种将废水中的氯乙烯(
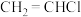 )进行环境无害化处理的微生物电池装置,同时利用此装置在铁上镀铜。
)进行环境无害化处理的微生物电池装置,同时利用此装置在铁上镀铜。
①M为
②若M极消耗0.1mol氯乙烯,则铁电极增重
您最近一年使用:0次
2023-08-08更新
|
384次组卷
|
2卷引用:安徽省滁州市实验中学等2校2022-2023学年高二上学期1月期末考试化学试题
9-10高二下·浙江台州·阶段练习
名校
解题方法
5 . 金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:还原性Fe>Ni>Cu)
| A.阳极发生还原反应,其电极反应式:Ni2++2e-=Ni |
| B.电解过程中,阳极质量的减少与阴极质量的增加相等 |
| C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+ |
| D.电解后,电解槽底部的阳极泥中有Cu和Pt |
您最近一年使用:0次
2022-08-15更新
|
1464次组卷
|
119卷引用:安徽省蚌埠市第二中学2017-2018学年高二上学期期中考试化学试题
安徽省蚌埠市第二中学2017-2018学年高二上学期期中考试化学试题(已下线)浙江省临海市白云中学2009—2010学年度高二下学期第一次月考化学试题(已下线)2010年云南省玉溪一中高二下学期期末考试化学试题(已下线)2011届福建省三明一中高三上学期期中考试化学卷(已下线)2011届山东省济南外国语学校高三上学期第三次质量检测化学试卷(已下线)2010-2011学年江苏省南京六中高二下学期期末考试化学试题(已下线)2011-2012学年山东省潍坊市高二寒假作业化学(一)试卷(已下线)2011-2012学年福建南平政和一中高二期末考试化学试卷(已下线)2011-2012学年天津市耀华中学高二上学期期末考试化学试卷(已下线)2011-2012学年陕西省师大附中高一下学期期末考试化学试卷(已下线)2013届江苏省泰州中学高三上学期期中考试化学试卷(已下线)2013届山东省济宁市鱼台一中高三上学期期中考试化学试卷(已下线)2014高考名师推荐化学电解三池的应用(已下线)2013-2014天津市耀华中学高二上学期期末考试化学试卷(已下线)2015安徽望江中学同步课时练(人教选修4)第四章检测试卷2014-2015四川省重点中学高二下学期期中考试化学试卷2015-2016学年福建省四地六校高二上学期10月联考化学试卷2015-2016学年福建省四地六校高二上学期10月一次联考化学试卷2016届湖南省十校共同体高三上学期12月联考化学试卷2015-2016学年河北省故城高级中学高二上12月月考化学试卷2016届山东省菏泽一中高三上学期12月月考化学试卷2015-2016学年吉林省延边三中高二上12月月考化学试卷2017届山东省滕州市第二中学高三上学期10月月考化学试卷2017届甘肃省天水一中高三上学期第一次月考化学卷2016-2017学年福建省四地六校高二上第一次月考化学试卷(已下线)同步君 选修4 第4章 第3节 电解原理的应用2016-2017学年河北石家庄一中高二上期中考试化学试卷2016-2017学年黑龙江哈尔滨六中高二上期末化学卷2016-2017学年江苏省如东高级中学高一下学期第一次(3月)阶段检测化学试卷福建省龙海市程溪中学2016-2017学年高二下学期期末考试化学试题山东省寿光现代中学2017-2018学年高二上学期开学考试化学试题河南省郑州市中牟县二中2017-2018学年高二第一次月考化学试题宁夏银川市六盘山高级中学2017-2018学年高二上学期第一次月考化学试题福建省三明市第一中学2017-2018学年高二上学期第一次月考化学试题河北省承德市第一中学2017-2018学年高二上学期第一次月考化学试题山东省垦利第一中学2017-2018学年高二上学期第一次月考化学试题四川省成都经开区实验中学2018届高三10月月考理综化学试题山东省菏泽市2017-2018学年高二上学期期中考试(B)化学试题高中化学人教版 选修四 第四章 电化学基础 第三节 电解池 电解池第二课时(电解原理的应用)陕西师范大学附中2017-2018第一学期高二年级化学期中考试化学试题天津市红桥区2017-2018学年高二上学期期末考试化学试题河南省豫南九校2017-2018学年高二上学期期末联考化学试题1河南省豫南九校2017-2018学年高二上学期期末联考化学试题2河北省承德市第二中学2017-2018学年高二上学期第一次月考化学试题2018-2019学年鲁科版高中化学选修四:第1章检测题河南省镇平县第一高级中学2018-2019学年高二上学期第一次月考化学试题吉林省辽源市田家炳高级中学2018-2019学年高二9月月考化学试题广东省惠州市惠东县惠东高级中学2018-2019学年高二上学期10月月考化学试题山东省鄄城市第一中学2018-2019学年高二上学期第一次月考化学试题陕西省黄陵中学2018-2019学年高二(重点班)上学期期中考试化学试题高二人教版选修4 第四章 第三节 电解池山东省泰安市宁阳一中2018-2019学年高二上学期阶段性考试三(12月)化学试题(已下线)考点10 电解原理 金属的腐蚀与防护——备战2019年浙江新高考化学考点四川省遂宁市2018-2019学年高二下学期期末考试化学试题云南省普洱市澜沧县民族中学2018-2019学年高二下学期期末考试化学试题四川省武胜县烈面中学校2018届高三9月入学考试化学试题(已下线)2019年9月22日 《每日一题》 2020年高考一轮复习-每周一测山东省泰安市宁阳县第一中学2019-2020学年高二上学期第一次段考化学试题(已下线)2019年12月4日 《每日一题》人教版(选修4)——电解精炼铜福建省泉州第十六中学2019-2020学年高二10月份月考化学试题2020年春季人教版高中化学选修4第四章《电化学基础》测试卷河北省沧州市泊头市第一中学2019-2020学年高二月考检测化学试题(已下线)【新东方】 2020-2福建省安溪一中2020年高一实验班线上阶段测试化学试题河北省泊头市第一中学2019-2020学年高二上学期期末模拟考试化学试卷四川省自贡市田家炳中学2019-2020学年高二下学期开学考试化学试题甘肃省西北师范大学附属中学2019-2020学年高二上学期期中考试化学试题甘肃省武威第一中学2019-2020学年高二下学期期中考试化学试题四川省泸县第四中学2019-2020学年高二下学期第四学月考试化学试题四川省泸县第一中学2019-2020学年高二下学期第四学月考试化学试题云南省昆明市官渡区第一中学2019-2020学年高二下学期期中考试化学试题黑龙江省哈尔滨师范大学青冈实验中学校2020-2021学年高二上学期开学考试化学试题黑龙江省哈尔滨市第一中学校2021届高三上学期开学测试化学试题河北省邯郸市大名县第一中学2020-2021学年高二上学期9月月考化学试题鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第3节 电能转化为化学能——电解 课时2 电解原理的应用鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第3节 电能转化为化学能——电解高中必刷题高二选择性必修1第四章 化学反应与电能 第二节 电解池 课时2 电解原理的应用山东省菏泽市单县第五中学2020-2021学年高二上学期第一次月考(10月)化学试题福建省永安市第三中学2020-2021学年高二10月月考化学(选考班)试题福建省三明第一中学2020-2021学年高二上学期第一次月考化学试题人教版(2019)高二化学选择性必修1第四章 化学反应与电能 第二节 电解池 课时2 电解原理的应用湖北省武汉市蔡甸区汉阳一中2020-2021学年高二上学期9月联考化学试题(已下线)专题4.3.2 电解原理的应用-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)4.2.2 电解原理的应用(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)河北省石家庄市藁城区第一中学2019-2020学年高二上学期第三次月考化学试题(已下线)4.3.2 电解原理的应用(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练浙江省宁波市北仑中学2020-2021学年高一下学期期中考试化学(1班选考)试题解题达人.化学选择题(2021全国卷)提升小卷05江苏省苏州市吴中区2020-2021学年高二下学期期中调研测试化学试题河北沧州泊头一中2020-2021学年高一下学期第二次月考化学试卷黑龙江省鹤岗市第一中学2020-2021学年高一6月月考化学试题贵州省遵义市2020~2021学年高二下学期期末质量检测化学试题黑龙江省哈尔滨市第九中学校2020-2021学年高一下学期6月月考化学试题选择性必修1专题1第二单元 课时4 电解原理的应用(已下线)1.2.4 电解原理的应用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)江苏省外国语学校2020-2021学年高二下学期期中调研测试化学试卷河南省南阳市第五中学2021-2022学年高二上学期10月月考化学试题 福建师范大学附属中学2021-2022学年高二上学期期中考试化学试题黑龙江省实验中学2021-2022学年高二上学期期中考试化学试题(已下线)4.2.2 电解原理的应用(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)内蒙古包头市2021-2022学年高二上学期期末考试化学试题辽宁省沈阳市市级重点高中联合体2021-2022学年高二上学期期末考试化学试题浙江省舟山市2021-2022学年高二上学期期末检测化学试题河北省保定市博野中学2021-2022学年高二上学期12月月考化学试题河北省衡水市武强中学2021-2022学年高二下学期期中考试化学试题辽宁省部分中学2021-2022学年高二下学期期末检测化学试题山东省德州市2020-2021学年高二上学期反应原理月考(B)化学试题辽宁省部分中学2021-2022学年高二上学期期末测试化学试题黑龙江省嫩江市第一中学2021-2022学年高二下学期开学考试化学试题河南省濮阳市元龙高级中学2021-2022学年高二下学期5月月考化学试题(已下线)第四章 化学反应与电能(B卷·能力提升练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)湖北省襄阳市第一中学2022-2023学年高二上学期12月线上考试化学试题新疆阿克苏市实验中学2021-2022学年高二上学期期末考试化学试题(已下线)4.2.2 电解原理的应用-同步学习必备知识(已下线)第六章 化学反应与能量 第37讲 电解池 金属的腐蚀与防护第2课时 电解原理的应用福建省宁德市第一中学2021-2022学年高二上学期9月月考化学试题
名校
6 .  、
、 是大气污染物但又有着重要用途。
是大气污染物但又有着重要用途。
Ⅰ.已知: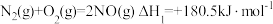
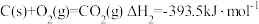
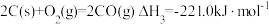
(1)某反应的平衡常数表达式为 ,此反应的热化学方程式为:
,此反应的热化学方程式为:___________ 。
(2)向绝热恒容密闭容器中充入等量的 和
和 进行反应,能判断反应已达到化学平衡状态的是
进行反应,能判断反应已达到化学平衡状态的是___________ (填序号)。
a.容器中的压强不变b.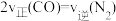
c.气体的平均相对分子质量保持34.2不变d.该反应平衡常数保持不变
e. 和
和 的体积比保持不变
的体积比保持不变
Ⅱ. 可用于制。为探究某浓度的的化学性质,某同学设计如下实验流程:
可用于制。为探究某浓度的的化学性质,某同学设计如下实验流程:

(3)用离子方程式表示 溶液具有碱性的原因
溶液具有碱性的原因___________ 。 与氯水反应的离子方程式是
与氯水反应的离子方程式是___________ 。
(4)含 的烟气可用
的烟气可用 溶液吸收。可将吸收液送至电解槽再生后循环使用。再生电解槽如图所示。a电极上含硫微粒放电的反应式为
溶液吸收。可将吸收液送至电解槽再生后循环使用。再生电解槽如图所示。a电极上含硫微粒放电的反应式为___________ 。(任写一个)。离子交换膜___________ (填标号)为阴离子交换膜。
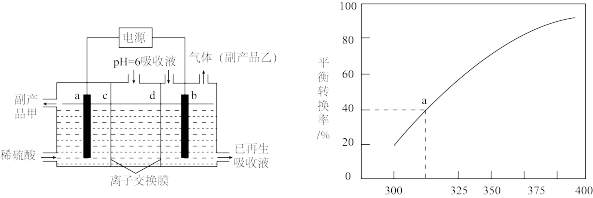
(5)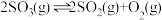 ,将一定量的
,将一定量的 放入恒容的密闭容器中,测得其平衡转化率随温度变化如图所示。图中a点对应温度下,已知
放入恒容的密闭容器中,测得其平衡转化率随温度变化如图所示。图中a点对应温度下,已知 的起始压强为
的起始压强为 ,该温度下反应的平衡常数
,该温度下反应的平衡常数
___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 、
、 是大气污染物但又有着重要用途。
是大气污染物但又有着重要用途。Ⅰ.已知:
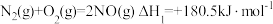
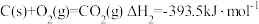
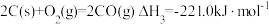
(1)某反应的平衡常数表达式为
 ,此反应的热化学方程式为:
,此反应的热化学方程式为:(2)向绝热恒容密闭容器中充入等量的
 和
和 进行反应,能判断反应已达到化学平衡状态的是
进行反应,能判断反应已达到化学平衡状态的是a.容器中的压强不变b.
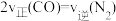
c.气体的平均相对分子质量保持34.2不变d.该反应平衡常数保持不变
e.
 和
和 的体积比保持不变
的体积比保持不变Ⅱ.
 可用于制。为探究某浓度的的化学性质,某同学设计如下实验流程:
可用于制。为探究某浓度的的化学性质,某同学设计如下实验流程:
(3)用离子方程式表示
 溶液具有碱性的原因
溶液具有碱性的原因 与氯水反应的离子方程式是
与氯水反应的离子方程式是(4)含
 的烟气可用
的烟气可用 溶液吸收。可将吸收液送至电解槽再生后循环使用。再生电解槽如图所示。a电极上含硫微粒放电的反应式为
溶液吸收。可将吸收液送至电解槽再生后循环使用。再生电解槽如图所示。a电极上含硫微粒放电的反应式为
(5)
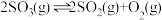 ,将一定量的
,将一定量的 放入恒容的密闭容器中,测得其平衡转化率随温度变化如图所示。图中a点对应温度下,已知
放入恒容的密闭容器中,测得其平衡转化率随温度变化如图所示。图中a点对应温度下,已知 的起始压强为
的起始压强为 ,该温度下反应的平衡常数
,该温度下反应的平衡常数
您最近一年使用:0次
2022-04-04更新
|
172次组卷
|
4卷引用:安徽省六安第一中学2021-2022学年高二上学期期末考试化学试题
名校
解题方法
7 . 乙醛酸(OHC-COOH)是一种重要的有机化学中间体,具有极其活跃的化学性质和广泛的用途,常温下易溶于水,微溶于酒精,其有多种制备方法,如硝酸氧化法、过氧化氢氧化法和电解法等。
I.硝酸氧化法

第一步:向三颈烧瓶中依次加入质量分数为40%的乙二醛78.5mL,质量分数为30%的盐酸17.2mL,蒸馏水30mL;
第二步:搅拌并通入氧气5分钟,升温至50℃,加入亚硝酸钠固体2.5g,搅拌下升温至60℃,缓慢分批滴加质量分数为40%的硝酸溶液47mL(23分钟加完),恒温下反应2小时,然后升温至75℃,搅拌30分钟反应结束;
第三步:降温结晶、过滤、洗涤,得到产品。
(1)装置a、b的名称分别为_______ 。
(2)在催化剂亚硝酸钠的作用下,可用浓硝酸氧化乙二醛(OHC-CHO)制取乙醛酸,该反应的化学方程式为_______ 。
(3)第二步通入氧气的目的是_______ (用化学方程式并结合简单文字说明);硝酸需要缓慢分批加入的原因是_______ 。
(4)第三步中洗涤产品所用的最佳试剂为_______ 。
II.过氧化氢氧化法
(5)乙二醛硝酸氧化法具有原料易得及反应条件温和等优点,但也存在明显不足。因此用过氧化氢代替硝酸制取乙醛酸的理由是_______ 。
II.电解法
(6)乙醛酸溶液可以由草酸(HOOC-COOH)水溶液经电解获得,请写出电解过程中阴极的电极反应式_______ 。
I.硝酸氧化法

第一步:向三颈烧瓶中依次加入质量分数为40%的乙二醛78.5mL,质量分数为30%的盐酸17.2mL,蒸馏水30mL;
第二步:搅拌并通入氧气5分钟,升温至50℃,加入亚硝酸钠固体2.5g,搅拌下升温至60℃,缓慢分批滴加质量分数为40%的硝酸溶液47mL(23分钟加完),恒温下反应2小时,然后升温至75℃,搅拌30分钟反应结束;
第三步:降温结晶、过滤、洗涤,得到产品。
(1)装置a、b的名称分别为
(2)在催化剂亚硝酸钠的作用下,可用浓硝酸氧化乙二醛(OHC-CHO)制取乙醛酸,该反应的化学方程式为
(3)第二步通入氧气的目的是
(4)第三步中洗涤产品所用的最佳试剂为
II.过氧化氢氧化法
(5)乙二醛硝酸氧化法具有原料易得及反应条件温和等优点,但也存在明显不足。因此用过氧化氢代替硝酸制取乙醛酸的理由是
II.电解法
(6)乙醛酸溶液可以由草酸(HOOC-COOH)水溶液经电解获得,请写出电解过程中阴极的电极反应式
您最近一年使用:0次
8 . 锰的重要用途是制造锰钢。一种以高铁锰矿(含MnO2、Fe2O3及少量FeO、CaO、K2O、Na2O)为原料生产金属锰的工艺流程如下:
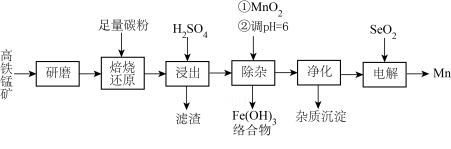
回答下列问题:
(1)“焙烧还原”时,高铁锰矿中MnO2被还原为MnO。
①理论上,还能被还原的成分有___________ 、___________ (填化学式)。
②根据下表数据,焙烧时应选择的温度为___________ 。
(2)“浸出”产生“滤渣”的主要成分为___________ (填化学式);该步骤中需再加入MnSO4以促进“滤渣"析出,结合化学反应原理解释其原因:___________ 。
(3)“除杂”时,加入的MnO2将Fe2+氧化为Fe3+,其离子方程式为___________ ;再将pH逐步调至6,Fe3+水解为Fe(OH)3,同时Fe3+与Na+、K+形成络合物沉淀。
(4)电解“净化”所得溶液(MnSO4的酸性溶液)制备Mn。
①电解时,溶液中的阳离子在阴极存在两个相互竞争的电极反应,其产物分别为Mn和___________ (填化学式)。
②研究表明,加入适量的SeO2有利于Mn在电极上析出。机理为:SeO2与水反应生成的H2SeO3(二元弱酸)在阴极放电生成Se单质,该电极反应为___________ ,电极上的Se对Mn2+有特殊的吸附性能,使Mn2+的电还原沉积成为主要反应。

回答下列问题:
(1)“焙烧还原”时,高铁锰矿中MnO2被还原为MnO。
①理论上,还能被还原的成分有
②根据下表数据,焙烧时应选择的温度为
| 还原温度/℃ | 焙烧后Mn元素在主要含锰物质中的分布/% | ||
| MnO2 | 高价锰(MnxOy) | 低价锰(MnO) | |
| 600 | 40.92 | 34.76 | 24.32 |
| 800 | 10.56 | 6.63 | 82.81 |
| 1000 | 5.77 | 2.70 | 91.29 |
| 1100 | 痕量 | 0.46 | 98.76 |
| 1200 | 痕量 | 0.30 | 97.94 |
(2)“浸出”产生“滤渣”的主要成分为
(3)“除杂”时,加入的MnO2将Fe2+氧化为Fe3+,其离子方程式为
(4)电解“净化”所得溶液(MnSO4的酸性溶液)制备Mn。
①电解时,溶液中的阳离子在阴极存在两个相互竞争的电极反应,其产物分别为Mn和
②研究表明,加入适量的SeO2有利于Mn在电极上析出。机理为:SeO2与水反应生成的H2SeO3(二元弱酸)在阴极放电生成Se单质,该电极反应为
您最近一年使用:0次
2021-06-03更新
|
185次组卷
|
3卷引用:安徽省舒城中学2020-2021学年高二下学期第三次月考化学试题
9 . 二甲醚(CH3OCH3)具有优良的燃烧性能,被称为21世纪的“清洁能源”。一步法合成二甲醚是以合成气(CO/H2)为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应:
①CO(g)+2H2(g) CH3OH(g) △H1=-90.7kJ•mol-1
CH3OH(g) △H1=-90.7kJ•mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-23.5kJ•mol-1
CH3OCH3(g)+H2O(g) △H2=-23.5kJ•mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41.2kJ•mol-1
CO2(g)+H2(g) △H3=-41.2kJ•mol-1
(1)一种新合成二甲醚的方法为一定条件下:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g),该反应的△H=
CH3OCH3(g)+3H2O(g),该反应的△H=___ kJ•mol-1;
判断该反应在一定温度下、体积恒定的密闭容器中,下列不能作为达到化学平衡状态的依据是___ 。
A.平均摩尔质量保持不变
B.容器的密度不变
C.容器内压强保持不变
D.单位时间内消耗2molCO2,同时消耗1mol二甲醚
(2)可采用CO和二甲醚催化合成乙醇。
反应①:CH3OCH3(g)+CO(g) CH3COOCH3(g) △H1
CH3COOCH3(g) △H1
反应②:CH3COOCH3(g)+2H2(g) CH3OH(g)+ C2H5OH(g) △H2
CH3OH(g)+ C2H5OH(g) △H2
a.压强为pKpa时,温度对二甲醚和乙酸甲酯平衡转化率的影响如图甲所示,则△H1____ (填“>”或“<”)0。

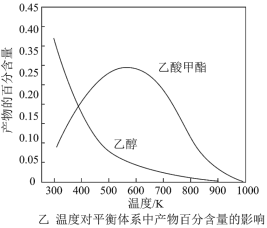
b.温度对平衡体系中乙酸甲酯的含量和乙醇的影响如图乙所示,在300~600K范围内,乙酸甲酯的含量逐渐增大,而乙醇的百分含量逐渐减小的原因是:___ 。
c.若压强为pKpa、温度为800K时,向2L恒容密闭容器中充入1molCH3OCH3和1molCO发生反应①,2min时达到平衡,则前2min内CH3COOCH3的平均生成速率为___ ,该条件下反应①的平衡常数K=___ 。
(3)以铜为原料,利用电解法可制取具有广泛用途的光电材料——纳米Cu2O,其工作原理如图3所示。则b是___ 极,电解时阳极的电极反应式为___ 。

①CO(g)+2H2(g)
 CH3OH(g) △H1=-90.7kJ•mol-1
CH3OH(g) △H1=-90.7kJ•mol-1②2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H2=-23.5kJ•mol-1
CH3OCH3(g)+H2O(g) △H2=-23.5kJ•mol-1③CO(g)+H2O(g)
 CO2(g)+H2(g) △H3=-41.2kJ•mol-1
CO2(g)+H2(g) △H3=-41.2kJ•mol-1(1)一种新合成二甲醚的方法为一定条件下:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g),该反应的△H=
CH3OCH3(g)+3H2O(g),该反应的△H=判断该反应在一定温度下、体积恒定的密闭容器中,下列不能作为达到化学平衡状态的依据是
A.平均摩尔质量保持不变
B.容器的密度不变
C.容器内压强保持不变
D.单位时间内消耗2molCO2,同时消耗1mol二甲醚
(2)可采用CO和二甲醚催化合成乙醇。
反应①:CH3OCH3(g)+CO(g)
 CH3COOCH3(g) △H1
CH3COOCH3(g) △H1反应②:CH3COOCH3(g)+2H2(g)
 CH3OH(g)+ C2H5OH(g) △H2
CH3OH(g)+ C2H5OH(g) △H2a.压强为pKpa时,温度对二甲醚和乙酸甲酯平衡转化率的影响如图甲所示,则△H1


b.温度对平衡体系中乙酸甲酯的含量和乙醇的影响如图乙所示,在300~600K范围内,乙酸甲酯的含量逐渐增大,而乙醇的百分含量逐渐减小的原因是:
c.若压强为pKpa、温度为800K时,向2L恒容密闭容器中充入1molCH3OCH3和1molCO发生反应①,2min时达到平衡,则前2min内CH3COOCH3的平均生成速率为
(3)以铜为原料,利用电解法可制取具有广泛用途的光电材料——纳米Cu2O,其工作原理如图3所示。则b是

您最近一年使用:0次
名校
解题方法
10 . 金属镍有广泛的用途。粗镍中含有少量 、
、 、
、 、
、 等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性
等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性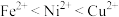 )
)
 、
、 、
、 、
、 等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性
等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性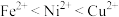 )
)A.电解后,电解槽底部的阳极泥中含有 和 和 |
| B.电解过程中,阳极质量的减少与阴极质量的增加相等 |
C.阳极发生还原反应,其电极反应式: |
D.电解后,溶液中存在的金属阳离子只有 和 和 |
您最近一年使用:0次
2021-01-19更新
|
553次组卷
|
9卷引用:安徽省师范大学附中2019-2020学年高二上学期期中考试化学试题
安徽省师范大学附中2019-2020学年高二上学期期中考试化学试题安徽省淮北市树人高级中学2020-2021学年高二上学期第一次联考化学试题【全国百强校】山东省济南第一中学2018-2019学年高二上学期期中考试化学试题湖南省长沙市雨花区2019-2020学年高二上学期期末考试化学(选考)试题福建省连城县第一中学2020-2021学年高二上学期第一次月考化学试题天津市耀华中学2020-2021学年高二上学期期末考试化学试题(已下线)专题09 电化学基础-备战2021届高考化学二轮复习题型专练福建省南安市侨光中学、昌财实验中学2021-2022学年高二上学期第二次阶段考化学试题吉林省长春希望高中2021-2022学年高二上学期期末考试化学试题



