1 . 原子序数大于4的主族元素A和B的离子分别为Am+和Bn﹣, 已知它们的核外电子排布相同,据此推断:
①A和B所属周期数之差为(填具体数字)________ ,
②A和B的核电荷数之差为(用含m或n的式子表示)________ ,
③B和A的族序数之差为________ .
①A和B所属周期数之差为(填具体数字)
②A和B的核电荷数之差为(用含m或n的式子表示)
③B和A的族序数之差为
您最近一年使用:0次
10-11高一下·福建莆田·阶段练习
2 . 元素在周期表中的位置,反映了元素的原子结构和元素的性质。下图是元素周期表的一部分。
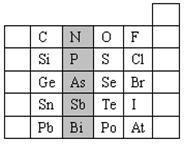
(1)阴影部分元素N的最高价氧化物为______ 。根据元素周期律,请你预测:H3AsO4、H3PO4 的酸性强弱:H3AsO4______ H3PO4。(用“>”、“<”或“=”表示)
(2)元素S的最高正价和最低负价分别为______ 、______ ,
(3)在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断在相同条件下Se与H2反应的限度______ (选填“更大”、“更小”或“相同”)。
(4)羰基硫(COS)分子结构与二氧化碳分子结构相似,所有原子的最外层都满足8电子结构。请写出羰基硫分子的电子式______
(5)单质砷和热的浓H2SO4反应,生成As2O3,反应的化学方程式为______ ;

(1)阴影部分元素N的最高价氧化物为
(2)元素S的最高正价和最低负价分别为
(3)在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断在相同条件下Se与H2反应的限度
(4)羰基硫(COS)分子结构与二氧化碳分子结构相似,所有原子的最外层都满足8电子结构。请写出羰基硫分子的电子式
(5)单质砷和热的浓H2SO4反应,生成As2O3,反应的化学方程式为
您最近一年使用:0次
名校
3 . 短周期元素X、Y、Z、R在周期表中的相对位置如图所示,请回答以下问题:

(1)X的原子结构示意图为________________ 。
(2)与R同周期的元素,最高价氧化物对应水化物酸性最强的是(填化学式)______________ 。
(3)X与R的非金属性强弱顺序是:X____ R(填“>”或“<”)。
(4)位于Y下一周期的同主族元素的最高价氧化物对应的水化物的化学式为_________________ 。
(5)Y和Z最高价氧化物对应水化物反应的化学方程式为_____________________________________ 。

(1)X的原子结构示意图为
(2)与R同周期的元素,最高价氧化物对应水化物酸性最强的是(填化学式)
(3)X与R的非金属性强弱顺序是:X
(4)位于Y下一周期的同主族元素的最高价氧化物对应的水化物的化学式为
(5)Y和Z最高价氧化物对应水化物反应的化学方程式为
您最近一年使用:0次
名校
4 . 元素①~⑧在元素周期表中的位置如下,回答有关问题:

(1)写出⑦元素名称_____ ,画出⑥的离子结构示意图__________ ;写出②含有10个中子的核素的化学符号_________ 。
(2)在②、③、④、⑤四种元素中,其离子半径按由大到小的排列顺序为_______________ 。(用化学式表示,下同)
(3)②③⑥元素氢化物的稳定性由强到弱的顺序为________ (填化学式)。
(4)表中能形成两性氢氧化物的元素是_______ (填元素符号)
(5)由②④⑥三种元素组成的一种盐在空气中放置会变质,请用化学方程式表示变质的反应____________________________________ 。
(6)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH碱性强于NH3·H2O,继而可以验证Na的金属性强于氮,你认为此设计是否合理?并说明理由_______________ 。

(1)写出⑦元素名称
(2)在②、③、④、⑤四种元素中,其离子半径按由大到小的排列顺序为
(3)②③⑥元素氢化物的稳定性由强到弱的顺序为
(4)表中能形成两性氢氧化物的元素是
(5)由②④⑥三种元素组成的一种盐在空气中放置会变质,请用化学方程式表示变质的反应
(6)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH碱性强于NH3·H2O,继而可以验证Na的金属性强于氮,你认为此设计是否合理?并说明理由
您最近一年使用:0次
名校
5 . (1)下图的虚线框中每一列、每一行相当于课本附录的元素周期表的每一族和每一周期,并已标出氢元素的位置,但它的列数和行数都多于元素周期表。请在虚线框中用实线画出周期表第一至第五周期的轮廓,并画出金属与非金属的分界线________ 。

(2)部分短周期主族元素的原子半径及主要化合价
①乙元素的原子结构示意图____________ ,丙在元素周期表中的位置___________ ,戊、庚、辛以原子个数比1∶1∶1形成的化合物的结构式______________ 。
②甲的单质与丁的最高价氧化物的水化物反应的化学方程式是___________ ,辛的单质与己的最高价氧化物的水化物反应的离子方程式是______________________________ 。

(2)部分短周期主族元素的原子半径及主要化合价
| 元素 | 甲 | 乙 | 丙 | 丁 | 戊 | 己 | 庚 | 辛 |
| 原子半径(nm) | 0.077 | 0.143 | 0.111 | 0.104 | 0.066 | 0.186 | 0.037 | 0.099 |
| 主要化合价 | +4,-4 | +3 | +2 | +6,-2 | -2 | +1 | +1 | +7,-1 |
①乙元素的原子结构示意图
②甲的单质与丁的最高价氧化物的水化物反应的化学方程式是
您最近一年使用:0次
2018-09-04更新
|
233次组卷
|
3卷引用:福建省晋江市(安溪一中、养正中学、惠安一中、泉州实验中学四校)2017-2018学年高一下学期期末联考化学试题
福建省晋江市(安溪一中、养正中学、惠安一中、泉州实验中学四校)2017-2018学年高一下学期期末联考化学试题(已下线)2019年3月3日 《每日一题》人教(必修2)-每周一测四川省凉山州2018-2019学年高一下学期期末考试化学试题
名校
6 . A、B、C、D、E代表5种元素.请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为_______ ;
(2)B元素的负一价离子的电子层结构都与氩相同,B的原子结构示意图为____ ;
(3)C元素是第三周期中无未成对电子的主族元素,它的轨道排布式为___________ ;
(4)D元素的正三价离子的3d能级为半充满,其基态原子的电子排布式为______ 。
(5)E原子共有3个价电子,其中一个价电子位于第三能层d轨道,指出该元素在周期
表中所处的周期数和族序数:____________________ .
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为
(2)B元素的负一价离子的电子层结构都与氩相同,B的原子结构示意图为
(3)C元素是第三周期中无未成对电子的主族元素,它的轨道排布式为
(4)D元素的正三价离子的3d能级为半充满,其基态原子的电子排布式为
(5)E原子共有3个价电子,其中一个价电子位于第三能层d轨道,指出该元素在周期
表中所处的周期数和族序数:
您最近一年使用:0次
2017-11-02更新
|
541次组卷
|
2卷引用:福建省福州市八县(市)协作校2016-2017学年高二下学期期中考试化学试题
7 . 有A、B、C、D四种元素,A元素形成的离子中只有一个质子,B原子的最外层电子数是次外层的3倍,C元素的一价阳离子核外有10个电子,D元素的原子得到一个电子后能形成与氩原子电子层结构相同的离子。回答下列问题:
(1)画出D元素的离子结构示意图________ ;C2B2的电子式为___________ 。
(2)由B、C、D三种元素组成的化合物中含有的化学键有______________ 。
(3)A和B可形成电子数相同的两种粒子,该两种粒子反应后生成一种中性分子,反应的离子方程式:_________________________ 。
(1)画出D元素的离子结构示意图
(2)由B、C、D三种元素组成的化合物中含有的化学键有
(3)A和B可形成电子数相同的两种粒子,该两种粒子反应后生成一种中性分子,反应的离子方程式:
您最近一年使用:0次
名校
8 . 硼及硼的化合物有着广泛的用途。请回答下列问题:
(1)硼在元素周期表中的位置为____________ ,硼元素有两种天然同位素10B和11B,硼元素的近似相对原子质量为10.8,则两种同位素原子的原子个数之比为_____________ 。
(2)单质硼(B)在一定条件下与NaOH溶液反应生成NaBO2和一种气体,请写出该反应的化学方程式__________________________ 。
(3)硼酸(H3BO3)是一种白色片状晶体,微溶于水,对人体的受伤组织有着和缓的防腐消毒作用。硼酸是一元弱酸,室温时0.1mol/L硼酸的pH为5,计算硼酸的电离常数数K=____________ 。
氟硼酸(HBF4)是一种强酸,仅以离子状态存在于水中,请写出BF4-的电子式____________ 。
(4)B2H6是硼的一种气态氢化物,因组成与乙烷(C2H6)相似而被称为乙硼烷。
①经测定B2H6中B原子最外层也满足8电子结构,由此推测B2H6与C2H6分子结构____________ (填“相同”或“不相同”)。
②B2H6可由BF3与NaBH4在一定条件下反应制得,写出该反应的化学方程式_____________ 。
③B2H6是强还原剂,它与水反应生成H3BO3和H2。若有0.1mol B2H6与水完全反应,则产生H2在标准状况下的体积为____________ L。
(1)硼在元素周期表中的位置为
(2)单质硼(B)在一定条件下与NaOH溶液反应生成NaBO2和一种气体,请写出该反应的化学方程式
(3)硼酸(H3BO3)是一种白色片状晶体,微溶于水,对人体的受伤组织有着和缓的防腐消毒作用。硼酸是一元弱酸,室温时0.1mol/L硼酸的pH为5,计算硼酸的电离常数数K=
氟硼酸(HBF4)是一种强酸,仅以离子状态存在于水中,请写出BF4-的电子式
(4)B2H6是硼的一种气态氢化物,因组成与乙烷(C2H6)相似而被称为乙硼烷。
①经测定B2H6中B原子最外层也满足8电子结构,由此推测B2H6与C2H6分子结构
②B2H6可由BF3与NaBH4在一定条件下反应制得,写出该反应的化学方程式
③B2H6是强还原剂,它与水反应生成H3BO3和H2。若有0.1mol B2H6与水完全反应,则产生H2在标准状况下的体积为
您最近一年使用:0次
2017-05-07更新
|
803次组卷
|
3卷引用:2020届高三化学二轮选修大题必练—— 物质结构与性质大题练
名校
解题方法
9 . 原子结构与元素周期表存在着内在联系。根据已学知识,请回答下列问题:
(1)指出31号元素镓(Ga)在元素周期表中的位置:第________ 周期第________ 族。
(2)写出原子序数最小的第Ⅷ族元素原子的核外电子排布式:____________ 。
(3)写出3p轨道上只有2个未成对电子的元素的符号:____________ 、____________ 。
(1)指出31号元素镓(Ga)在元素周期表中的位置:第
(2)写出原子序数最小的第Ⅷ族元素原子的核外电子排布式:
(3)写出3p轨道上只有2个未成对电子的元素的符号:
您最近一年使用:0次
2017-05-06更新
|
205次组卷
|
2卷引用:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
名校
10 . 下表列出了①~⑨九种元素在周期表中的位置。
请按要求回答下列问题:
(1)①~⑨九种元素中非金属性最强的是________ (填元素符号)。
(2)元素⑧的原子结构示意图是_________ ;由①、④、⑥三种元素组成的化合物,其电子式是_________ 。
(3)元素②、⑧的气态氢化物的稳定性较强的是________________ (填化学式);元素③、⑨的最高价氧化物对应的水化物的酸性较强的是________________ (填化学式)。
(4)③、④、⑧三种元素的原子半径由大到小的顺序是________________ (填元素符号)。
(5)元素⑤、⑥组成的化合物的化学键类型是________________________ 。
(6)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式是________________
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
请按要求回答下列问题:
(1)①~⑨九种元素中非金属性最强的是
(2)元素⑧的原子结构示意图是
(3)元素②、⑧的气态氢化物的稳定性较强的是
(4)③、④、⑧三种元素的原子半径由大到小的顺序是
(5)元素⑤、⑥组成的化合物的化学键类型是
(6)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式是
您最近一年使用:0次
2016-12-09更新
|
655次组卷
|
6卷引用:福建省建瓯市芝华中学2019-2020学年高一下学期居家学习检测化学试题



