名校
1 . 如表是元素周期表的一部分,根据表中给出的10种元素,按要求作答。
(1)金属性最强的元素是_______ ;
(2)F的原子结构示意图是________ ;
(3)地壳中含量最多的元素是_______ ;
(4)Ne原子的最外层电子数是_______ ;
(5)N与O原子半径较大的是_______ ;
(6)H2S与HCl热稳定性较弱的是______ ;
(7)Na2O与MgO难与水反应的是______ ;
(8)Mg(OH)2与Al(OH)3能与强碱反应的是______ ;
(9)用于制造光导纤维的物质是______ (填“Si”或“SiO2”);
(10)次氯酸(HClO)具有杀菌漂白作用,其中Cl元素的化合价为____ ,HClO不稳定,易分解生成HCl和O2,写出其在光照条件下分解的化学方程式:____ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | N | O | F | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(1)金属性最强的元素是
(2)F的原子结构示意图是
(3)地壳中含量最多的元素是
(4)Ne原子的最外层电子数是
(5)N与O原子半径较大的是
(6)H2S与HCl热稳定性较弱的是
(7)Na2O与MgO难与水反应的是
(8)Mg(OH)2与Al(OH)3能与强碱反应的是
(9)用于制造光导纤维的物质是
(10)次氯酸(HClO)具有杀菌漂白作用,其中Cl元素的化合价为
您最近一年使用:0次
2019-10-04更新
|
503次组卷
|
4卷引用:2019年6月福建省普通高中学业水平合格性考试化学试题
2019年6月福建省普通高中学业水平合格性考试化学试题福建省平潭县新世纪学校2020-2021学年高二上学期第一次月考化学试题(学考)福建省龙海市第二中学2020-2021学年高二上学期期中考试化学试题(已下线)专题08 原子结构与元素周期表(核心素养卷)——【新教材精创】2019-2020学年高中化学新教材知识讲学
2 . 下表为元素周期表的一部分,请参照元素①-⑩在表中的位置,回答下列问题:
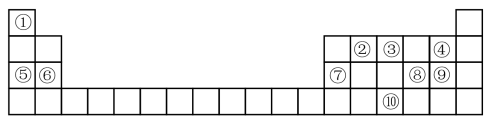
(1)元素⑩在周期表中的位置是_____ ,⑦的原子结构示意图为_____ 。
(2)④、⑤、⑥的简单离子半径由大到小的顺序为______ (用离子符号和“>”表示)。
(3)④⑧⑨的气态氢化物中,最稳定的是______ (用化学式表示),最高价氧化物对应水化物中,酸性最强的是_____ (用化学式表示)。
(4)⑤的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物发生反应的离子方程式___ 。
(5)由①③⑨组成的离子化合物的化学式为____ ,其中含有的化学键类型是______ 。

(1)元素⑩在周期表中的位置是
(2)④、⑤、⑥的简单离子半径由大到小的顺序为
(3)④⑧⑨的气态氢化物中,最稳定的是
(4)⑤的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物发生反应的离子方程式
(5)由①③⑨组成的离子化合物的化学式为
您最近一年使用:0次
2019-06-10更新
|
263次组卷
|
2卷引用:【校级联考】福建省宁德市高中同心顺联盟校2018-2019学年高一下学期期中考试化学试题
名校
3 . 下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。
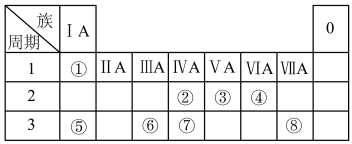
(1)⑦号元素的原子结构示意图为___________________________ 。
(2)②、③、⑤的单质熔点由大到小的顺序为(填化学式)________ 。
(3)①和②、①和③、①和⑦形成的化合物稳定性由强到弱的顺序是(填化学式)__________________________________________________ 。
(4)④、⑤可形成既含离子键又含共价键的化合物,请写出其电子式:________ 。
(5)由①和②组成的最简单的化合物的键角是________ 。
(6)⑤、⑥两种元素形成的最高价氧化物的水化物之间相互反应的离子方程式为__________________________________________________ 。

(1)⑦号元素的原子结构示意图为
(2)②、③、⑤的单质熔点由大到小的顺序为(填化学式)
(3)①和②、①和③、①和⑦形成的化合物稳定性由强到弱的顺序是(填化学式)
(4)④、⑤可形成既含离子键又含共价键的化合物,请写出其电子式:
(5)由①和②组成的最简单的化合物的键角是
(6)⑤、⑥两种元素形成的最高价氧化物的水化物之间相互反应的离子方程式为
您最近一年使用:0次
4 . 下表是元素周期表的一部分,请回答有关问题:
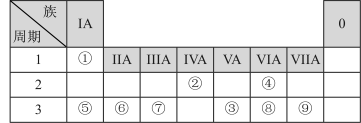
请按要求回答下列问题:
(1)元素⑦的原子结构示意图______________________ 。由②、④两种元素组成的化合物是___________ 化合物(填“共价”或“离子”)
(2)元素①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式__________________ ;一种离子化合物的化学式_________
(3)④⑤⑥三种元素的离子半径由大到小的顺序是____________ (填离子符号)。
(4)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较弱的是________ (填化学式)。
(5)元素③的气态氢化物和元素⑧的气态氢化物更稳定的是___________ (填化学式)。
(6)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应水化物反应,其离子方程式为_________________________________________

请按要求回答下列问题:
(1)元素⑦的原子结构示意图
(2)元素①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式
(3)④⑤⑥三种元素的离子半径由大到小的顺序是
(4)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较弱的是
(5)元素③的气态氢化物和元素⑧的气态氢化物更稳定的是
(6)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应水化物反应,其离子方程式为
您最近一年使用:0次
5 . 下图是中学教材中元素周期表的一部分,其中标出A~R 15种元素,试根据它们回答下列问题(填具体元素符号 或化学式 ):
(1)化学性质最不活泼的是____ ,原子半径最小的是(除稀有气体元素)___ 属于过渡元素的是____ (填A~R中的代号)。
(2)最高价氧化物对应的水化物中酸性最强的是_____ ,单质中氧化性最强的是________ ,第三周期元素形成的简单离子中半径最小的是______ 。
(3)F与K形成的化合物溶于水发生电离,所破坏的化学键为______ 。
(4)Q在元素周期表中的位置是_____ ,B、C可形成化合物B2C,该化合物的核外电子总数为_____ 。
(5)P的最高价氧化物对应的水化物与B的最高价氧化物对应的水化物的离子方程式:____________ 。
(6)元素E与元素F相比,金属性较强的是________ (用元素符号表示),下列表述中能证明这一事实的是______ (填序号)。
a.与酸反应时,每个F原子比每个E原子失电子数多
b.E的氢化物比F的氢化物稳定
c.E和F的单质与水反应E较剧烈
d.最高价氧化物对应水化物碱性E比F强
| A | B | C | D | ||||||||||||||
| E | F | G | H | I | J | K | L | ||||||||||
| R | |||||||||||||||||
| P | Q |
(2)最高价氧化物对应的水化物中酸性最强的是
(3)F与K形成的化合物溶于水发生电离,所破坏的化学键为
(4)Q在元素周期表中的位置是
(5)P的最高价氧化物对应的水化物与B的最高价氧化物对应的水化物的离子方程式:
(6)元素E与元素F相比,金属性较强的是
a.与酸反应时,每个F原子比每个E原子失电子数多
b.E的氢化物比F的氢化物稳定
c.E和F的单质与水反应E较剧烈
d.最高价氧化物对应水化物碱性E比F强
您最近一年使用:0次
6 . 下表为元素周期表的一部分,表中序号分别代表某一元素。请回答下列问题。
(1)①~⑩中,最活泼的金属元素是________ (写元素符号,下同),最不活泼的元素是________ 。
(2)①⑧的简单离子,其半径更大的是________ (写离子符号)。
(3)⑧⑨的气态氢化物,更稳定的是____________ (填化学式)。
(4)元素的非金属性:⑥________ ⑦(填“>”或“<”)。
(5)①~⑨的最高价氧化物的水化物中:酸性最强的是____________ (填化学式);碱性最强的是__________ (填化学式),该碱与⑤的最高价氧化物的水化物反应的离子方程式为__________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑦ | ⑧ | ⑩ | |||||
| 3 | ① | ② | ⑤ | ⑥ | ⑨ | |||
| 4 | ② | ④ |
(2)①⑧的简单离子,其半径更大的是
(3)⑧⑨的气态氢化物,更稳定的是
(4)元素的非金属性:⑥
(5)①~⑨的最高价氧化物的水化物中:酸性最强的是
您最近一年使用:0次
2019-04-24更新
|
120次组卷
|
4卷引用:福建省德化县第一中学、永安市第一中学、漳平市第一中学2017--2018学年高一年第一次联考(4月)化学试题
福建省德化县第一中学、永安市第一中学、漳平市第一中学2017--2018学年高一年第一次联考(4月)化学试题甘肃省武威市第五中学2018-2019学年高一下学期第一次月考化学试题(已下线)5.1.4 元素周期表的应用(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)湖南省邵阳市新邵县2021-2022学年高一上学期期末质量检测化学试题
名校
7 . 下表为长式周期表的一部分,其中的编号代表对应的元素。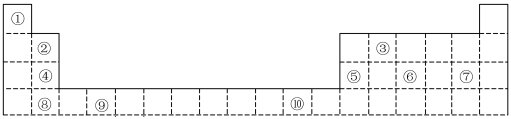
请回答下列问题:
(1)表中属于d区元素的是________ (填元素符号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为____ ;③和⑦形成的一种常见溶剂的化学式为_____ 。
(3)元素④的第一电离能________ 元素⑤(选填“>”、“=”或“<”)的第一电离能;元素⑥的电负性________ 元素⑦(选填“>”、“=”或“<”)的电负性。
(4)元素⑦和⑧形成的化合物的电子式为________________ 。
(5)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:________ 。

请回答下列问题:
(1)表中属于d区元素的是
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为
(3)元素④的第一电离能
(4)元素⑦和⑧形成的化合物的电子式为
(5)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
您最近一年使用:0次
名校
8 . 碳、硅、锗等碳族元素的单质及化合物广泛应用于我们生活的各个领域。回答下列问题。
(1)锗(Ge)曾被作为半导体材料,其的原子序数为32,则周期表的位置为__________ 。
(2)和田玉成分是Ca2Mg5H2Si8O24,将其用氧化物的形式表示__________ 。
(3)光导纤维在强碱性条件下容易发生“断路”,用离子方程式解释其原因________ 。
(4)水玻璃的主要成分是____ (化学式),是制备硅胶和木材防火剂的原料。
(5)铅为碳族元素中的一种元素,低价铅相对高价铅更稳定,铅的氧化物Pb3O4的氧化性比MnO2更强,请写出Pb3O4与浓盐酸反应的化学方程式____________ 。
(6)在12C、13C、14C、16O、17O、18O微粒中,共有_____ 种原子,属于________ 种元素;组成CO2分子种类有_______ 种。
(1)锗(Ge)曾被作为半导体材料,其的原子序数为32,则周期表的位置为
(2)和田玉成分是Ca2Mg5H2Si8O24,将其用氧化物的形式表示
(3)光导纤维在强碱性条件下容易发生“断路”,用离子方程式解释其原因
(4)水玻璃的主要成分是
(5)铅为碳族元素中的一种元素,低价铅相对高价铅更稳定,铅的氧化物Pb3O4的氧化性比MnO2更强,请写出Pb3O4与浓盐酸反应的化学方程式
(6)在12C、13C、14C、16O、17O、18O微粒中,共有
您最近一年使用:0次
名校
9 . 下表是元素周期表的一部分,表中字母分别代表一种元素。回答下列问题。
(1)表中所标元素,最活泼的金属元素形成简单离子符号为____ ;最不活泼的元素的原子结构示意图为 _____ ;其中一种元素的气态氢化物与其最高价氧化物的水化物可直接化合生成一种盐,该盐是_______ 。
(2)写出两种满足下列条件的物质______ (写化学式)。
①由c、x、e组成的;②含有共价键的离子化合物。
(3)g、x、y的气态氢化物,最稳定的是______ (填化学式)。
(4)表中元素的最高价氧化物的水化物中:酸性最强的是______ (填化学式,下同);碱性最强的是_______ ,这两种物质反应的离子方程式为_________ 。
(5)推测元素的非金属性:a______ g(填“>”或“<”)。利用图装置设计实验,证明推测结论。

①仪器A的名称为___________ ,干燥管D的作用是______________ 。
②填空。
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | a | b | c | d | ||||
| 3 | e | f | g | x | y | z |
(2)写出两种满足下列条件的物质
①由c、x、e组成的;②含有共价键的离子化合物。
(3)g、x、y的气态氢化物,最稳定的是
(4)表中元素的最高价氧化物的水化物中:酸性最强的是
(5)推测元素的非金属性:a

①仪器A的名称为
②填空。
| 装置内试剂 | C中发生反应的化学方程式 | ||
| A | B | C | |
| 稀硫酸 | 碳酸钠 | ||
您最近一年使用:0次
名校
10 . 下表为元素周期表的一部分, 表中列出10种元素在周期表中的位置,按要求回答下列各题。
(1)写出下列序号所代表的元素符号③_____ ;⑩______
(2)写出⑥的一种用途_________________ ;常温下可与表中_______ 单质反应(填化学式)
(3)元素④的原子结构示意图为________________________ ;
(4)⑤和⑨形成的化合物的化学式为:_____________ ;向该化合物的水溶液里逐滴滴入苛性钠溶液,现象为__________________________________________________ .
(5)②⑤⑦⑧的原子半径由大到小的顺序是__________________________ (用元素符号表示)
(6)将①⑤同时投入到水中,发生反应的化学方程式有:______________
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑧ | ⑩ | ||||||
| 3 | ① | ③ | ⑤ | ⑥ | ⑦ | ⑨ | ||
| 4 | ② | ④ |
(1)写出下列序号所代表的元素符号③
(2)写出⑥的一种用途
(3)元素④的原子结构示意图为
(4)⑤和⑨形成的化合物的化学式为:
(5)②⑤⑦⑧的原子半径由大到小的顺序是
(6)将①⑤同时投入到水中,发生反应的化学方程式有:
您最近一年使用:0次
2019-04-16更新
|
280次组卷
|
2卷引用:福建省永安第十二中学2018-2019学年高一下学期3月月考化学试题



