1 . 活泼金属镁可在氯气、氧气、氮气、二氧化碳等气氛中点燃。
(1)镁在元素周期表中的位置是___ 。
(2)熔融态氯化镁可导电,氯化镁晶体属于__ (选填“共价晶体”、“离子晶体”、金属晶体”、“分子晶体”)。
(3)若需扑灭空气中镁燃烧,你认为可用的灭火材料是__ 。
(4)纯净的氮化镁为黄绿色的粉末,氮化镁遇水反应生成氢氧化镁和氨气.氮化镁溶于稀硫酸,生成___ 。
(5)等质量镁单质分别转化为氧化镁和氮化镁,两者的质量比m(MgO)∶m(Mg3N2)=__ 。
(1)镁在元素周期表中的位置是
(2)熔融态氯化镁可导电,氯化镁晶体属于
(3)若需扑灭空气中镁燃烧,你认为可用的灭火材料是
(4)纯净的氮化镁为黄绿色的粉末,氮化镁遇水反应生成氢氧化镁和氨气.氮化镁溶于稀硫酸,生成
(5)等质量镁单质分别转化为氧化镁和氮化镁,两者的质量比m(MgO)∶m(Mg3N2)=
您最近一年使用:0次
2021-01-31更新
|
250次组卷
|
2卷引用:福建省福州市2020-2021学年高一上学期期末考试化学试题
2 . 如表是元素周期表的一部分,根据表中给出的10种元素,按要求使用化学用语填空作答:
(1)地壳中含量最高的元素是___ (填元素符号);金属性最强的元素是___ (填元素符号);单质的化学性质最不活泼的元素是___ (填元素符号)。
(2)最高价氧化物对应水化物酸性最强的是___ (填化合物化学式);最高价氧化物不溶于水,但既溶于稀硫酸又溶于氢氧化钠溶液的是___ (填化合物化学式)。
(3)烧焦羽毛味气体A和臭鸡蛋味气体B相遇可发生反应生成一种单质和水,该反应化学方程式为____ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | |||||||
| 2 | C | N | O | Ne | ||||
| 3 | Na | Al | P | S | Cl |
(2)最高价氧化物对应水化物酸性最强的是
(3)烧焦羽毛味气体A和臭鸡蛋味气体B相遇可发生反应生成一种单质和水,该反应化学方程式为
您最近一年使用:0次
2021-01-31更新
|
215次组卷
|
2卷引用:福建省福州市2020-2021学年高一上学期期末考试化学试题
3 . 如图是元素周期表的一部分。回答下列问题:
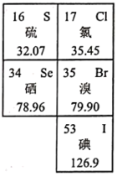
(1)溴被称为海洋元素。
①溴在元素周期表中位于第___________ 周期___________ 族。
②表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是___________ (填化学式)。
③能够证明溴单质的氧化性强于碘单质的离子方程式是___________ 。
(2)硒是人体必需的微量元素。
①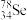 与
与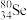 互称为
互称为___________ 。
②元素的气态氢化物的化学式为___________ 。
③SeO2溶于水生成H2SeO3,向所得溶液中通入SO2气体发生反应,生成硒单质和H2SO4.写出SO2与H2SeO3的反应方程式:___________ 。
(3)溴化硒是一种重要的电子元件材料,其分子的球棍模型如图所示。下列说法正确的是___________ (填字母)。
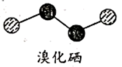
a.溴化硒属于离子化合物 b.原子半径r:r(Se)>r(Br)
c. Se元素的非金属性比Br的强 d.溴化硒的相对分子质量为317.72

(1)溴被称为海洋元素。
①溴在元素周期表中位于第
②表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是
③能够证明溴单质的氧化性强于碘单质的离子方程式是
(2)硒是人体必需的微量元素。
①
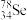 与
与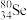 互称为
互称为②元素的气态氢化物的化学式为
③SeO2溶于水生成H2SeO3,向所得溶液中通入SO2气体发生反应,生成硒单质和H2SO4.写出SO2与H2SeO3的反应方程式:
(3)溴化硒是一种重要的电子元件材料,其分子的球棍模型如图所示。下列说法正确的是

a.溴化硒属于离子化合物 b.原子半径r:r(Se)>r(Br)
c. Se元素的非金属性比Br的强 d.溴化硒的相对分子质量为317.72
您最近一年使用:0次
2021-01-27更新
|
241次组卷
|
2卷引用:福建省莆田第二十四中学2021-2022学年高一下学期开学摸底考试化学(2卷)试题
名校
4 . 下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
(1)11种元素中,化学性质最不活泼的是__________ ,原子半径最小的是_________ 。
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是___________ 。
(3)②③④中形成的简单离子半径由大到小的顺序是_________________ 。
(4)元素⑦的氢化物电子式为_______ ,该氢化物常温下和元素②的单质反应的离子方程式是________________ 。
(5)①和⑨的最高价氧化物对应的水化物化学式为__________ 和__________ 。①和⑨两元素形成化合物中化学键的类型为____________ ,该化合物灼烧时焰色为_________ ,该化合物的溶液与元素⑧的单质反应的离子方程式为__________________ 。
(6)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为___________ 。
(7)⑧⑨⑪三种元素形成的气态氢化物最稳定的是_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(1)11种元素中,化学性质最不活泼的是
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是
(3)②③④中形成的简单离子半径由大到小的顺序是
(4)元素⑦的氢化物电子式为
(5)①和⑨的最高价氧化物对应的水化物化学式为
(6)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为
(7)⑧⑨⑪三种元素形成的气态氢化物最稳定的是
您最近一年使用:0次
2021-01-20更新
|
1811次组卷
|
6卷引用:福建省政和县第二中学2022-2023学年高一下学期第一次月考化学试题
福建省政和县第二中学2022-2023学年高一下学期第一次月考化学试题新疆哈密市第八中学2019-2020学年高一下学期期中考试化学试题(已下线)专题07 物质结构与元素周期律-备战2021届高考化学二轮复习题型专练河南省新蔡县第一高级中学2020-2021学年高一下学期5月月考化学试题甘肃省金昌市第一中学2020-2021学年高一下学期期中考试化学(理)试题(已下线)专题17 化学键(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练
名校
解题方法
5 . 在1-18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
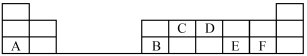
(1)金属性最强的元素是_______ ;
(2)画出D的原子结构示意图_______ ;
(3)地壳中含量最多的元素是_______ ;
(4)Ne原子的最外层电子数是_______ ;
(5)E和F分别形成的气态氢化物中最稳定的是_______ (填写氢化物的化学式)
(6)Mg(OH)2与Al(OH)3能与强碱反应的是_______ ;
(7)用于制造光导纤维的物质是_______ (填“Si”或“SiO2”);
(8)肼(N2H4)中氮元素和氢元素的质量比m(N):m(H)=_______ ;(相对原子质量:N-14,H-1)
(9)次氯酸(HClO)具有杀菌漂白作用,其中Cl元素的化合价为_______ ,HClO不稳定,易分解生成HCl和O2,写出其在光照条件下分解的化学方程式:_______ 。

(1)金属性最强的元素是
(2)画出D的原子结构示意图
(3)地壳中含量最多的元素是
(4)Ne原子的最外层电子数是
(5)E和F分别形成的气态氢化物中最稳定的是
(6)Mg(OH)2与Al(OH)3能与强碱反应的是
(7)用于制造光导纤维的物质是
(8)肼(N2H4)中氮元素和氢元素的质量比m(N):m(H)=
(9)次氯酸(HClO)具有杀菌漂白作用,其中Cl元素的化合价为
您最近一年使用:0次
名校
解题方法
6 . 下表是元素周期表的一部分,根据表中给出10种元素按要求作答。
(1)镁元素位于元素周期表中第____________ 周期____________ 族;
(2)空气组成中体积分数最大的气体是____________ ;
(3)O与S相比,原子半径较小的是____________ ;
(4)金刚石的组成元素是____________ ;
(5)单质的化学性质最不活泼的元素是____________ ;
(6)Na与Mg元素相比,金属性较强的是____________ ;
(7)NH3与PH3相比,热稳定性较弱的是____________ ;
(8)H2SO4与H3PO4相比,酸性较强的是____________ ;
(9)Mg(OH)2与Al(OH)3,其中属于两性氢氧化物的是____________ ;
(10)单质呈黄绿色的气体组成元素是____________ ,其单质的水溶液呈____________ (填“酸性”或“碱性”)。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | C | N | O | Ne | ||||
3 | Na | Mg | Al | P | S | Cl |
(1)镁元素位于元素周期表中第
(2)空气组成中体积分数最大的气体是
(3)O与S相比,原子半径较小的是
(4)金刚石的组成元素是
(5)单质的化学性质最不活泼的元素是
(6)Na与Mg元素相比,金属性较强的是
(7)NH3与PH3相比,热稳定性较弱的是
(8)H2SO4与H3PO4相比,酸性较强的是
(9)Mg(OH)2与Al(OH)3,其中属于两性氢氧化物的是
(10)单质呈黄绿色的气体组成元素是
您最近一年使用:0次
2020-12-16更新
|
237次组卷
|
2卷引用:福建省永安市第三中学2020-2021学年高二上学期期中考试化学(会考)试题
7 . 下表是元素周期表的一部分,根据表中给出10种元素(其中X、Y分别代表某种化学元素),按要求作答。
(1)X、Y两种元素符号分别是___________ 和___________ ;
(2)最外层电子数为4的原子,其元素符号是___________ ;
(3)某阴离子结构示意图为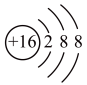 ,该离子符号是
,该离子符号是___________ ;
(4)C与N原子半径较小的是___________ ;
(5)保存在煤油中的金属是___________ ;
(6)化学性质最不活泼的单质是___________ ;
(7)HF与HCl热稳定性较强的是___________ ;
(8) 与
与 酸性较强的是
酸性较强的是___________ ;NaOH与 碱性较弱的是
碱性较弱的是___________ ;
(9)写出Y元素组成的单质与氧气反应的化学方程式:___________ 。
周期 族 | IA | IIA | ⅢA | IVA | VA | ⅥA | ⅦA | O |
| 2 | C | N | X | F | Ne | |||
| 3 | Na | Mg | Y | S | Cl |
(1)X、Y两种元素符号分别是
(2)最外层电子数为4的原子,其元素符号是
(3)某阴离子结构示意图为
 ,该离子符号是
,该离子符号是(4)C与N原子半径较小的是
(5)保存在煤油中的金属是
(6)化学性质最不活泼的单质是
(7)HF与HCl热稳定性较强的是
(8)
 与
与 酸性较强的是
酸性较强的是 碱性较弱的是
碱性较弱的是(9)写出Y元素组成的单质与氧气反应的化学方程式:
您最近一年使用:0次
名校
解题方法
8 . 三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工,太阳能电池制造和液晶显示器制造中得到广泛应用。NF3是一种三角锥型分子,键角102°,沸点-129℃;可在铜的催化作用下由F2和过量NH3反应得到。
(1)NF3的沸点比NH3的沸点(-33℃)低得多的主要原因是________ 。
(2)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下面各题:
①在周期表中,最可能处于同一族的是_________ 。
②T元素最可能是_______ 区元素。若T为第二周期元素,F是第三周期元素中原子半径最小的元素,则T、F形成化合物的空间构型为________ ,其中心原子的杂化方式为________ 。
(1)NF3的沸点比NH3的沸点(-33℃)低得多的主要原因是
(2)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下面各题:
元素代号 | I1 | I2 | I3 | I4 |
Q | 2080 | 4000 | 6100 | 9400 |
R | 500 | 4600 | 6900 | 9500 |
S | 740 | 1500 | 7700 | 10500 |
T | 580 | 1800 | 2700 | 11600 |
U | 420 | 3100 | 4400 | 5900 |
①在周期表中,最可能处于同一族的是
②T元素最可能是
您最近一年使用:0次
名校
解题方法
9 . 表是元素周期表的一部分,根据表中列出的10种元素,回答下列问题。
(1)单质化学性质最不活泼的是___ ;地壳中含量最多的元素是___ (填名称);
(2)单质常用作半导体材料的是___ ;Mg原子结构示意图为___ ;
(3)O和S中,原子半径较大的是;CH4和NH3中,热稳定性较强的是___ (填名称);
(4)新制氯水有漂白作用___ ,是因为其中含有___ (填“HCl”或“HClO”);
(5)元素最高价氧化物对应水化物中,碱性最强的是___ (填化学式),两性氢氧化物是___ ;
(6)某烃分子中含有6个碳原子,结构简式为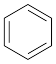 ,常用作有机溶剂。该有机物分子式为
,常用作有机溶剂。该有机物分子式为___ ,其中碳元素与氢元素的质量比m(C)∶m(H)=___ (相对原子质量:H-1 C-12)
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(2)单质常用作半导体材料的是
(3)O和S中,原子半径较大的是;CH4和NH3中,热稳定性较强的是
(4)新制氯水有漂白作用
(5)元素最高价氧化物对应水化物中,碱性最强的是
(6)某烃分子中含有6个碳原子,结构简式为
 ,常用作有机溶剂。该有机物分子式为
,常用作有机溶剂。该有机物分子式为
您最近一年使用:0次
2020-10-23更新
|
115次组卷
|
3卷引用:福建省莆田市仙游县枫亭中学2019-2020学年高二上学期期中考试化学试题
解题方法
10 . 下表是元素周期表的一部分,根据所给的10种元素,完成以下各小题。
(1)金属性最强的元素是____________  填元素符号
填元素符号 。
。
(2)最不活泼元素的原子结构示意图为___________ 。
(3)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是__________  填元素名称
填元素名称 。
。
(4)Na、Mg两种元素中,原子半径较大的是__________ 。
(5)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式为___________ 。
(6)Na极易与水反应,该反应的化学方程式为____________ 。
(7)HF与HCl热稳定性较强的是_________ 。
(8)由碳与氢元素形成的最简单有机物的化学式为________ ,该物质中碳元素与氢元素的质量比为____________ ,其分子空间构型为____________ 。
(9)重氢( )和超重氢(
)和超重氢(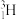 )两种核素都可用作制造氢弹的原料,它们所含中子数之比为
)两种核素都可用作制造氢弹的原料,它们所含中子数之比为___________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | H | |||||||
2 | C | N | F | Ne | ||||
3 | Na | Mg | Al | S | Cl |
(1)金属性最强的元素是
 填元素符号
填元素符号 。
。 (2)最不活泼元素的原子结构示意图为
(3)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是
 填元素名称
填元素名称 。
。 (4)Na、Mg两种元素中,原子半径较大的是
(5)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式为
(6)Na极易与水反应,该反应的化学方程式为
(7)HF与HCl热稳定性较强的是
(8)由碳与氢元素形成的最简单有机物的化学式为
(9)重氢(
 )和超重氢(
)和超重氢(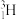 )两种核素都可用作制造氢弹的原料,它们所含中子数之比为
)两种核素都可用作制造氢弹的原料,它们所含中子数之比为
您最近一年使用:0次



