解题方法
1 . 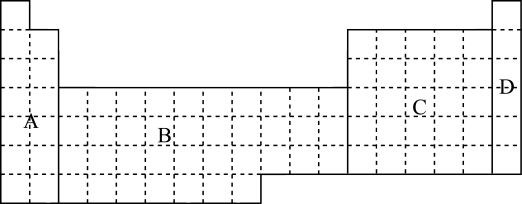
(1)在上面元素周期表中全部是金属元素的区域为____ 。
A B C D
(2)有人认为形成化合物最多的元素不是IVA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是____ (写出元素符号)。
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①画出甲原子的基态外围电子轨道表示式:_____ 。
② 甲、乙两元素相比较,金属性较强的是____ (填名称),可以验证该结论的实验是__ 。
A 将在空气中放置已久的这两种元素的块状单质分别放入热水中
B 将这两种元素的单质粉末分别和同浓度的盐酸反应
C 将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
D 比较这两种元素的气态氢化物的稳定性
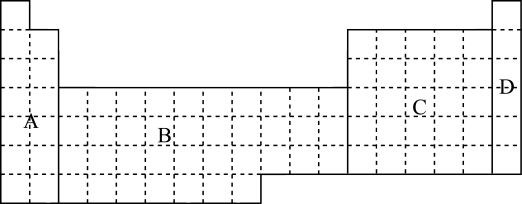
(1)在上面元素周期表中全部是金属元素的区域为
A B C D
(2)有人认为形成化合物最多的元素不是IVA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①画出甲原子的基态外围电子轨道表示式:
② 甲、乙两元素相比较,金属性较强的是
A 将在空气中放置已久的这两种元素的块状单质分别放入热水中
B 将这两种元素的单质粉末分别和同浓度的盐酸反应
C 将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
D 比较这两种元素的气态氢化物的稳定性
您最近一年使用:0次
解题方法
2 . 为纪念元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。下图是扇形元素周期表的一部分,针对元素①~⑩按要求作答。
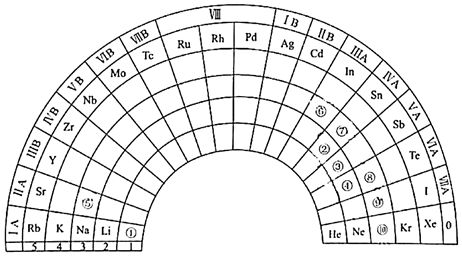
(1)⑩的原子结构示意图为___________________ 。
(2)①和②组成的最简单化合物的电子式为_______________ 。
(3)④和⑤的简单离子半径较大的是________ (填序号)。
(4)③的简单氢化物与其最高价氧化物对应水化物反应得到的盐的化学式为________________ 。
(5)某元素原子的M层电子数为K层电子数的两倍,则该元素是_________ (填序号)。
(6)把⑥投入烧碱溶液中发生反应的化学方程式为__________________ 。
(7)写出一个能证明⑧的非金属性小于⑨的离子方程式____________________ 。

(1)⑩的原子结构示意图为
(2)①和②组成的最简单化合物的电子式为
(3)④和⑤的简单离子半径较大的是
(4)③的简单氢化物与其最高价氧化物对应水化物反应得到的盐的化学式为
(5)某元素原子的M层电子数为K层电子数的两倍,则该元素是
(6)把⑥投入烧碱溶液中发生反应的化学方程式为
(7)写出一个能证明⑧的非金属性小于⑨的离子方程式
您最近一年使用:0次
名校
解题方法
3 . 下表是元素周期表前三周期,针对表中的①~⑧元素,回答下列问题:
(1)元素④在周期表中的位置是________ 。
(2)在这些元素原子中,得电子能力最强的是______ (填元素符号)。
(3)单质化学性质最不活泼的元素是______ (填元素符号),元素②原子结构示意图为______ 。
(4)元素⑥、⑦形成的氢化物中,沸点高的是______ (填化学式)。
(5)元素①的最高价氧化物对应的水化物所含化学键的类型是_______ 。
(6)元素⑤最简单的氢化物和最高价氧化物对应的水化物相互反应的产物是_______ 。
(7)写出元素③的单质与稀盐酸反应的离子方程式_______ 。
⑤ | ⑥ | ||||||||||||||||
① | ② | ③ | ④ | ⑦ | ⑧ | ||||||||||||
(2)在这些元素原子中,得电子能力最强的是
(3)单质化学性质最不活泼的元素是
(4)元素⑥、⑦形成的氢化物中,沸点高的是
(5)元素①的最高价氧化物对应的水化物所含化学键的类型是
(6)元素⑤最简单的氢化物和最高价氧化物对应的水化物相互反应的产物是
(7)写出元素③的单质与稀盐酸反应的离子方程式
您最近一年使用:0次
2020-08-12更新
|
175次组卷
|
2卷引用:福建省宁德市2019-2020学年高一下学期期末考试化学试题
名校
4 . 如表列出了①~⑧八种元素在周期表中的位置:
请按要求回答下列问题:
(1)②、③、④三种元素的最高价氧化物对应的水化物,其中碱性最强的是________ (填写化学式)。
(2)②、③、⑥三种元素按原子半径由大到小的顺序排列为_____________ (用元素符号表示)。
(3)元素①的气态氢化物的电子式是_________ ,写出实验室里制取该气体的化学方程式为 ____________________ 。
(4)元素③的原子结构示意图是_____ 。元素⑤的单质的导电性介于导体和绝缘体之间.因此是一种良好的____ 材料。
(5)向元素②的单质与水反应后的溶液中加入元素④的单质,发生反应的化学方程式为_______________________ 。
(6)用离子方程式证明⑦⑧两素非金属性的强弱______________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ | ⑦ | |||
| 4 | ⑥ | ⑧ |
请按要求回答下列问题:
(1)②、③、④三种元素的最高价氧化物对应的水化物,其中碱性最强的是
(2)②、③、⑥三种元素按原子半径由大到小的顺序排列为
(3)元素①的气态氢化物的电子式是
(4)元素③的原子结构示意图是
(5)向元素②的单质与水反应后的溶液中加入元素④的单质,发生反应的化学方程式为
(6)用离子方程式证明⑦⑧两素非金属性的强弱
您最近一年使用:0次
2020-08-08更新
|
490次组卷
|
2卷引用:福建省泉州科技中学2020-2021学年高二下学期期中考试化学试题
5 . 下表是元素周期表的一部分,根据表中给出的10种元素,按要求作答
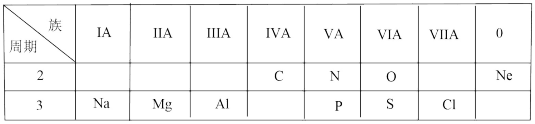
(1)镁元素位于元素周期表中第___ 周期_____ 族;
(2)空气组成中体积分数最大的气体是_____ ;
(3)O与S相比,原子半径较小的是____ ;
(4)金刚石的组成元素是________ ;
(5)单质的化学性质最不活泼的元素是______ ;
(6)Na与Mg元素相比金属性较强的是_________
(7)NH3与PH3相比,热稳定性较弱的是______
(8)H2SO4与H3PO4相比酸性较强的是______
(9)Mg(OH)2与Al(OH)3其中属于两性氢氧化物的是________
(10)单质呈黄绿色的气体组成元素是_____ ,其单质的水溶液呈__ (填“酸性或“碱性”)。

(1)镁元素位于元素周期表中第
(2)空气组成中体积分数最大的气体是
(3)O与S相比,原子半径较小的是
(4)金刚石的组成元素是
(5)单质的化学性质最不活泼的元素是
(6)Na与Mg元素相比金属性较强的是
(7)NH3与PH3相比,热稳定性较弱的是
(8)H2SO4与H3PO4相比酸性较强的是
(9)Mg(OH)2与Al(OH)3其中属于两性氢氧化物的是
(10)单质呈黄绿色的气体组成元素是
您最近一年使用:0次
名校
6 . 针对下面11种元素,完成以下各小题。
(1)地壳中含量最多的元素是________ (填元素符号)
(2)化学性质最不活泼的元素是___________ (填名称)
(3)Cl的离子结构示意图为_____________
(4)C与N相比,原子半径较小的是_______ (填元素名称)
(5)最高价氧化物对应的水化物碱性最强的是___________ (填化学式)
(6)MgO和 中,属于两性氧化物的是
中,属于两性氧化物的是_________________
(7)P、S、Cl的最高价氧化物对应水化物酸性最强的是___________ (填物质名称)
(8)可用来制造计算机芯片的物质是______ ,晶体硅的主要用途是___________ (写出一种)。
(9)在S与Cl的单质中,化学性质较活泼的单质是______________ (填化学式)可用什么化学反应说明该事实(写出反应的化学方程式):______________ 。
| 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | P | S | Cl |
(1)地壳中含量最多的元素是
(2)化学性质最不活泼的元素是
(3)Cl的离子结构示意图为
(4)C与N相比,原子半径较小的是
(5)最高价氧化物对应的水化物碱性最强的是
(6)MgO和
 中,属于两性氧化物的是
中,属于两性氧化物的是(7)P、S、Cl的最高价氧化物对应水化物酸性最强的是
(8)可用来制造计算机芯片的物质是
(9)在S与Cl的单质中,化学性质较活泼的单质是
您最近一年使用:0次
名校
7 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年,元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题。

(1)元素Ga在元素周期表中的位置为:___ (写明周期和族)。
(2)Sn的最高正价为______ ,Cl的最高价氧化物对应水化物的化学式为______ ,As的气态氢化物为_______ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是_______ (填化学式)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4______ H2SeO4(填“>”、“<”或“=”)。
③氢化物的还原性:H2O__ H2S(填“>”、“<”或“=”)。
(4)可在图中分界线(虚线部分)附近寻找________ (填序号)。
A. 优良的催化剂 B. 半导体材料 C. 合金材料 D. 农药
(5)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。

(1)元素Ga在元素周期表中的位置为:
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③氢化物的还原性:H2O
(4)可在图中分界线(虚线部分)附近寻找
A. 优良的催化剂 B. 半导体材料 C. 合金材料 D. 农药
(5)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。
| 实验步骤 | 实验现象与结论 |
| 在试管中加入 | 现象: |
您最近一年使用:0次
2020-05-26更新
|
64次组卷
|
2卷引用:福建省莆田八中2020-2021学年高一下学期第二次月考化学(A卷) 试题
名校
解题方法
8 . 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答:
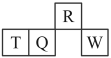
(1)T的原子结构示意图为___________
(2)元素的非金属性:Q_________ W(填“强于”或“弱于”)
(3)R有多种氧化物,其中相对分子质量最小的氧化物为_____________
(4)原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是___________
(5)T的最高价氧化物对应的水化物和强碱溶液反应的离子方程式为___________
(6)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为_________

(1)T的原子结构示意图为
(2)元素的非金属性:Q
(3)R有多种氧化物,其中相对分子质量最小的氧化物为
(4)原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是
(5)T的最高价氧化物对应的水化物和强碱溶液反应的离子方程式为
(6)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为
您最近一年使用:0次
2020-05-20更新
|
69次组卷
|
2卷引用:福建省泉州第十六中学2019-2020学年高一下学期5月月考化学试题
名校
9 . 下表是现行中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题:

(1)②表示的元素是______ (填元素符号)。
(2)①与⑤两种元素相比较,原子半径较大的是______ (填元素符号),其非金属性较强的是 ______ (填元素符号),其最高正价氧化物水化物酸性较强的酸是 ______ (填分子式)。
(3)⑥元素的单质可以用来制取漂白粉,其有效成分是______ (填化学式)。
(4)②与⑥元素的氢化物的稳定性:______ 大于______ (填分子式)。

(1)②表示的元素是
(2)①与⑤两种元素相比较,原子半径较大的是
(3)⑥元素的单质可以用来制取漂白粉,其有效成分是
(4)②与⑥元素的氢化物的稳定性:
您最近一年使用:0次
2020-02-15更新
|
848次组卷
|
3卷引用:福建省建瓯市芝华中学2021-2022学年高一下学期第一次月考化学试题
名校
解题方法
10 . 氟及其化合物在生产生活中被广泛使用,造福人类。
(1)氟在元素周期表中的位置是___________ 。
(2)氢氟酸具有刻蚀玻璃的特性,写出该反应的化学方程式____________ 。已知25℃时,氢氟酸的电离平衡常数Ka=3.6×10-4,若将0.01 mol·L-1的HF溶液与pH=12的NaOH溶液等体积混合,则溶液中离子浓度由大到小的顺序为_____ 。
(3)次氟酸(HOF)由科学家在1971年首次制得,次氟酸的电子式为_______ 。
(4)四氟肼(N2F4)用作高能燃料的氧化剂,1 mol N2F4分子中含有的共价键数目是________ NA。N2F4气体可用Fe3+氧化二氟胺(HNF2)制得,写出该反应的离子方程式______________ 。
(5)六氟化铀(UF6)是铀的稳定气态化合物,用作核燃料,由U3O8制取UF6的三步反应原理如下:
①U3O8+H2 →UO2+H2O (未配平) ②UO2+4HF=UF4+2H2O ③UF4+ F2 = UF6
则下列说法正确的是_____________ 。
A.反应①②③都是氧化还原反应
B.反应③中U元素被氧化
C.反应①中氧化剂和还原剂的物质的量之比为2:1
(6)六氟磷酸锂(LiPF6)是锂离子电池广泛使用的电解质。LiPF6与极少量水反应可生成POF3等三种含氟化合物,写出该反应的化学方程式:________ 。
(1)氟在元素周期表中的位置是
(2)氢氟酸具有刻蚀玻璃的特性,写出该反应的化学方程式
(3)次氟酸(HOF)由科学家在1971年首次制得,次氟酸的电子式为
(4)四氟肼(N2F4)用作高能燃料的氧化剂,1 mol N2F4分子中含有的共价键数目是
(5)六氟化铀(UF6)是铀的稳定气态化合物,用作核燃料,由U3O8制取UF6的三步反应原理如下:
①U3O8+H2 →UO2+H2O (未配平) ②UO2+4HF=UF4+2H2O ③UF4+ F2 = UF6
则下列说法正确的是
A.反应①②③都是氧化还原反应
B.反应③中U元素被氧化
C.反应①中氧化剂和还原剂的物质的量之比为2:1
(6)六氟磷酸锂(LiPF6)是锂离子电池广泛使用的电解质。LiPF6与极少量水反应可生成POF3等三种含氟化合物,写出该反应的化学方程式:
您最近一年使用:0次
2020-01-23更新
|
243次组卷
|
4卷引用:福建省宁德市2019-2020学年高三上学期期末质量检测理综化学试题
福建省宁德市2019-2020学年高三上学期期末质量检测理综化学试题(已下线)2020届高三《新题速递·化学》2月第01期(考点01-06)(已下线)考点05 元素周期表和元素周期律-2020年高考化学命题预测与模拟试题分类精编河南省郑州市第一中学2021届高三上学期开学测试化学试题



