2023·全国·模拟预测
1 . 中科院福建物质结构研究所陈学元团队将 掺杂
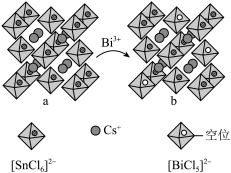
掺杂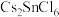 (晶胞结构为a)获得空位有序型双钙钛矿纳米晶体(晶胞结构为b),过程如图所示。若a和b的晶胞参数均为x nm,下列说法错误的是
(晶胞结构为a)获得空位有序型双钙钛矿纳米晶体(晶胞结构为b),过程如图所示。若a和b的晶胞参数均为x nm,下列说法错误的是
 掺杂
掺杂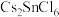 (晶胞结构为a)获得空位有序型双钙钛矿纳米晶体(晶胞结构为b),过程如图所示。若a和b的晶胞参数均为x nm,下列说法错误的是
(晶胞结构为a)获得空位有序型双钙钛矿纳米晶体(晶胞结构为b),过程如图所示。若a和b的晶胞参数均为x nm,下列说法错误的是
A.a中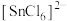 的配位数为8 的配位数为8 |
B.a中两个最近的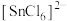 的距离为 的距离为 |
C.掺杂后的晶体的化学式为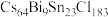 |
D.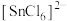 和 和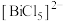 的中心原子的价层电子对数不相同 的中心原子的价层电子对数不相同 |
您最近一年使用:0次
2 . 下列符号或表征错误的是
A.聚丙烯的链节: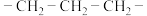 |
B.基态Cl原子的价电子轨道表示式: |
C. 的VSEPR模型: 的VSEPR模型: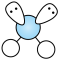 |
D.HClO的空间填充模型: |
您最近一年使用:0次
名校
解题方法
3 . 从微粒结构角度分析,下列说法正确的是
A. 中,阴离子空间结构为正四面体形,S原子的杂化方式为 中,阴离子空间结构为正四面体形,S原子的杂化方式为 |
B.根据价层电子对互斥理论, 、 、 、 、 的中心原子价层电子对数相同 的中心原子价层电子对数相同 |
C. 的空间结构为V形,其中心原子的杂化方式为 的空间结构为V形,其中心原子的杂化方式为 |
D.三氧化硫有单分子气体和三聚分子固体( )两种存在形式,两种分子中S原子的杂化轨道类型相同 )两种存在形式,两种分子中S原子的杂化轨道类型相同 |
您最近一年使用:0次
2023-04-19更新
|
389次组卷
|
3卷引用:东北育才学校高中部2023届高三下学期适应性考试化学试题
名校
4 . 下列“类比”结果正确的是
A.N2分子中存在N N键,化学性质稳定,则 N键,化学性质稳定,则  的化学性质稳定 的化学性质稳定 |
| B.SO2的空间构型为V 形,则O3的空间构型也为V 形 |
| C.聚乙烯不能使溴水褪色,则聚乙炔也不能使溴水褪色 |
| D.甲苯能使酸性高锰酸钾溶液褪色,则苯的同系物(除苯)都能使酸性高锰酸钾溶液褪色 |
您最近一年使用:0次
2023-04-19更新
|
451次组卷
|
3卷引用:东北育才学校高中部2023届高三下学期适应性考试化学试题
2023·云南·二模
解题方法
5 . X、Y、Z、W是原子序数依次增大的前四周期元素,X元素的简单氢化物能与其最高价氧化物对应水化物反应生成盐; Y元素原子的核外电子只有8种运动状态;Z为短周期金属元素,其简单离子的半径在同周期中最小;基态W原子的未成对电子数为6。下列说法错误的是
| A.第一电离能: X>Y> Z |
B.键角 > > |
| C.W为第四周期d区元素 |
| D.X和Y的最简单气态氢化物中,前者更易液化 |
您最近一年使用:0次
解题方法
6 . 室温下,某种催化剂能高效催化空气中甲醛的氧化,快速实现室内空气的净化,发生的反应如下:HCHO+O2 CO2+H2O。下列有关说法正确的是
CO2+H2O。下列有关说法正确的是
 CO2+H2O。下列有关说法正确的是
CO2+H2O。下列有关说法正确的是| A.反应物和生成物都是极性分子 | B.HCHO分子中σ键与π键的比值为3:1 |
| C.HCHO、CO2分子的中心原子杂化类型相同 | D.H2O分子的VSEPR模型名称为平面三角形 |
您最近一年使用:0次
2023·全国·模拟预测
名校
解题方法
7 . 一种由四种短周期主族元素组成的化合物(结构如图所示)可用于制化肥、药物、木材防火剂,其中W、X、Y、Z的原子序数依次增大,且X与Y、Z均相邻。下列有关说法错误的是


| A.原子半径:Z>X>Y |
| B.XW3和ZW3的键角前者大于后者 |
| C.该化合物的阴离子中除W元素外,所有原子最外层均满足8电子结构| |
| D.W、X、Y三种元素形成的化合物中可能既含离子键,又含共价键 |
您最近一年使用:0次
名校
解题方法
8 . 回答下列问题:
(1)根据价层电子对互斥理论,H2S、SO2、SO3的气态分中,中心原子价层电子对数不同于其他分子的是___________ 。气态三氧化硫以单分子形式存在,其分子的空间结构为___________ 形;固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为___________ 。

(2)分子中的大π键可用符号 表示,其中m代表参与形成大键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),已知SO2分子中含有5对孤电子对,则SO2中的大π键应表示为
),已知SO2分子中含有5对孤电子对,则SO2中的大π键应表示为___________ 。SO2分子中键角∠OSO___________  中键角∠ONO(填“>”、“<”、“=”)。
中键角∠ONO(填“>”、“<”、“=”)。
(3)乙烯酮在室温下可聚合成二聚乙烯酮(结构简式为 ),二聚乙烯酮分子中含有的π键与σ键的数目之比为
),二聚乙烯酮分子中含有的π键与σ键的数目之比为___________ 。下图中表示的碳原子能量最高的是___________ (填字母)。
A. B.
B.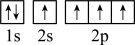
C. D.
D.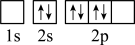
(4)三甲胺 和乙二胺
和乙二胺 均属于胺,但三甲胺比乙二胺的沸点低得多,原因是
均属于胺,但三甲胺比乙二胺的沸点低得多,原因是___________ 。C60的熔点比金刚石、石墨熔点低的原因是___________ 。
(5)在冰晶体中除氢键外,还存在范德华力 。已知冰的升华热是
。已知冰的升华热是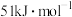 ,请估算冰中氢键的作用能为多少
,请估算冰中氢键的作用能为多少___________  。
。
(1)根据价层电子对互斥理论,H2S、SO2、SO3的气态分中,中心原子价层电子对数不同于其他分子的是

(2)分子中的大π键可用符号
 表示,其中m代表参与形成大键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),已知SO2分子中含有5对孤电子对,则SO2中的大π键应表示为
),已知SO2分子中含有5对孤电子对,则SO2中的大π键应表示为 中键角∠ONO(填“>”、“<”、“=”)。
中键角∠ONO(填“>”、“<”、“=”)。(3)乙烯酮在室温下可聚合成二聚乙烯酮(结构简式为
 ),二聚乙烯酮分子中含有的π键与σ键的数目之比为
),二聚乙烯酮分子中含有的π键与σ键的数目之比为A.
 B.
B.
C.
 D.
D.
(4)三甲胺
 和乙二胺
和乙二胺 均属于胺,但三甲胺比乙二胺的沸点低得多,原因是
均属于胺,但三甲胺比乙二胺的沸点低得多,原因是(5)在冰晶体中除氢键外,还存在范德华力
 。已知冰的升华热是
。已知冰的升华热是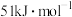 ,请估算冰中氢键的作用能为多少
,请估算冰中氢键的作用能为多少 。
。
您最近一年使用:0次
名校
9 . 下列各组微粒的空间结构不相同的是
A.NH 和H3O+ 和H3O+ | B.H2O和SO2 | C.CO2和C2H2 | D.SiO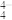 和SO 和SO |
您最近一年使用:0次
2023-04-06更新
|
220次组卷
|
4卷引用:辽宁省凌源市高中2022-2023学年高二4月联考化学试题
名校
10 . 下列有关化合物结构与性质的论述错误的是
| A.B3N3H6(无机苯)的结构与苯相似,其中形成大π键的电子全部由N提供 |
| B.根据原子半径推知,F-F键的键能大于Cl-Cl键,F2化学性质更稳定 |
| C.NH3的成键电子对间排斥力较大,所以NH3的键角比PH3大 |
| D.BF3和SO3中B、S杂化轨道类型相同,二者VSEPR模型均为平面三角形 |
您最近一年使用:0次
2023-04-02更新
|
491次组卷
|
4卷引用:辽宁省凌源市实验中学2022-2023学年高二下学期4月月考化学试题



