1 .  、
、 、
、 、
、 为原子序数依次增大的四种短周期主族元素,
为原子序数依次增大的四种短周期主族元素, 、
、 、
、 为其中三种元素最高价氧化物的水化物,转化关系如图。
为其中三种元素最高价氧化物的水化物,转化关系如图。 单质与
单质与 单质在不同条件下反应会生成两种不同化合物,
单质在不同条件下反应会生成两种不同化合物, 简单离子半径是同周期元素简单离子中最小的,
简单离子半径是同周期元素简单离子中最小的, 与
与 同主族。
同主族。

回答下列问题:
(1) 、
、 、
、 、
、 形成的简单离子半径由大到小的顺序是
形成的简单离子半径由大到小的顺序是_______ (用离子符号来表示)。
(2) 、
、 、
、 、
、 元素的电负性由大到小的顺序为
元素的电负性由大到小的顺序为_______ (用元素符号来表示)。
(3) 与
与 形成的一种化合物常用作供氧剂,其电子式为
形成的一种化合物常用作供氧剂,其电子式为_______ 。
(4) 与
与 形成的两种常见的化合物中,属于极性分子的是
形成的两种常见的化合物中,属于极性分子的是_______ (填化学式),写出 的简单气态氢化物
的简单气态氢化物 模型为
模型为_______ 。
(5)写出 与
与 反应的离子方程式为
反应的离子方程式为_______ 。
 、
、 、
、 、
、 为原子序数依次增大的四种短周期主族元素,
为原子序数依次增大的四种短周期主族元素, 、
、 、
、 为其中三种元素最高价氧化物的水化物,转化关系如图。
为其中三种元素最高价氧化物的水化物,转化关系如图。 单质与
单质与 单质在不同条件下反应会生成两种不同化合物,
单质在不同条件下反应会生成两种不同化合物, 简单离子半径是同周期元素简单离子中最小的,
简单离子半径是同周期元素简单离子中最小的, 与
与 同主族。
同主族。
回答下列问题:
(1)
 、
、 、
、 、
、 形成的简单离子半径由大到小的顺序是
形成的简单离子半径由大到小的顺序是(2)
 、
、 、
、 、
、 元素的电负性由大到小的顺序为
元素的电负性由大到小的顺序为(3)
 与
与 形成的一种化合物常用作供氧剂,其电子式为
形成的一种化合物常用作供氧剂,其电子式为(4)
 与
与 形成的两种常见的化合物中,属于极性分子的是
形成的两种常见的化合物中,属于极性分子的是 的简单气态氢化物
的简单气态氢化物 模型为
模型为(5)写出
 与
与 反应的离子方程式为
反应的离子方程式为
您最近一年使用:0次
2 .  原子在形成
原子在形成 分子时,
分子时, 、
、 轨道和1个
轨道和1个 轨道参与形成
轨道参与形成 杂化,
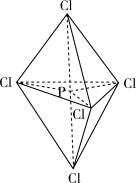
杂化, 的空间构型为三角双锥形(如下图所示)。下列关于
的空间构型为三角双锥形(如下图所示)。下列关于 分子的说法不正确的是
分子的说法不正确的是
 原子在形成
原子在形成 分子时,
分子时, 、
、 轨道和1个
轨道和1个 轨道参与形成
轨道参与形成 杂化,
杂化, 的空间构型为三角双锥形(如下图所示)。下列关于
的空间构型为三角双锥形(如下图所示)。下列关于 分子的说法不正确的是
分子的说法不正确的是
A. 分子中价电子对数为5 分子中价电子对数为5 |
B. 分子中没有形成 分子中没有形成 键 键 |
C. 分子中所有的 分子中所有的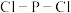 键角都相等 键角都相等 |
D. 分子中 分子中 原子也采用 原子也采用 杂化 杂化 |
您最近一年使用:0次
名校
解题方法
3 . 用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型或推测键角大小,下列判断正确的是
| A.SO2的分子构型类似CO2为直线形 | B.SO3是三角锥形分子 |
| C.BF3的键角为120° | D.PCl3是平面三角形分子 |
您最近一年使用:0次
2022-05-06更新
|
172次组卷
|
3卷引用:福建省漳州市正兴学校等三校2021-2022学年高二下学期期中联考化学试题
名校
4 . 甲烷在一定条件下可生成碳正离子(CH )、碳负离子(CH
)、碳负离子(CH )、甲基(-CH3)等,下列说法正确的是
)、甲基(-CH3)等,下列说法正确的是
 )、碳负离子(CH
)、碳负离子(CH )、甲基(-CH3)等,下列说法正确的是
)、甲基(-CH3)等,下列说法正确的是A.CH 与NH3、H3O+具有相似的空间构型 与NH3、H3O+具有相似的空间构型 |
B.两个甲基-CH3或一个CH 和一个CH 和一个CH 结合可得到不同化合物 结合可得到不同化合物 |
C.CH 和CH 和CH 空间构型均为平面三角形 空间构型均为平面三角形 |
D.CH 与OH-形成离子化合物 与OH-形成离子化合物 |
您最近一年使用:0次
2022-05-06更新
|
119次组卷
|
3卷引用:福建省泉州师范学院附属鹏峰中学、广海中学、泉港区第五中学2021-2022学年高二下学期期中联考化学试题
名校
解题方法
5 . 下列叙述正确的是
A.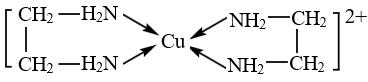 该配合物中配体是H2NCH2CH2NH2,配位数是2 该配合物中配体是H2NCH2CH2NH2,配位数是2 |
B. 离子的空间构型为V形,中心原子的杂化形式为sp2 离子的空间构型为V形,中心原子的杂化形式为sp2 |
C. 与 与 互为等电子体 互为等电子体 |
| D.HNO3分子的中心原子的价层电子对数为4,该分子的VSEPR模型是正四面体形 |
您最近一年使用:0次
名校
解题方法
6 . 下列判断正确的是
| A.H2O2、CS2、HI都是直线形分子 |
| B.C6H6、OF2、S2Cl2都是平面形分子 |
| C.CH2O、BF3、SO3都是平面三角形分子 |
| D.NCl3、NH3、CCl4都是三角锥形分子 |
您最近一年使用:0次
名校
解题方法
7 . 一种新催化剂能在室温下催化空气氧化甲醛:HCHO+O2→CO2+H2O,下列说法正确的是
| A.反应物和生成物均为分子 |
| B.反应物和生成物都为直线形分子 |
| C.反应时旧键断裂放出能量,新键形成吸收能量 |
| D.产物中CO2的键能大于H2O,所以沸点高于H2O |
您最近一年使用:0次
解题方法
8 . 下列分子的VSEPR模型不是四面体的是
| A.BeCl2 | B.NH3 | C.CH4 | D.H2O |
您最近一年使用:0次
解题方法
9 . 根据价层电子对互斥模型,判断下列分子的空间结构和极性正确的是
| 选项 | 分子式 | 价层电子对互斥模型 | 分子或离子的空间结构 | 分子极性 |
| A | SO2 | 三角形 | 角形 | 极性 |
| B | HCHO | 三角形 | 三角锥形 | 极性 |
| C | PCl3 | 四面体形 | 正三角形 | 非极性 |
| D | SiF4 | 四面体形 | 正四面体形 | 极性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 下列说法错误 的是
A. 与 与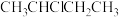 都含一个手性碳原子 都含一个手性碳原子 |
B. 和 和 的空间构型相似 的空间构型相似 |
C. 与 与 都是平面型分子 都是平面型分子 |
D. 和乙醚( 和乙醚( )都是直线型非极性分子 )都是直线型非极性分子 |
您最近一年使用:0次
2022-05-01更新
|
211次组卷
|
7卷引用:福建省莆田锦江中学2022-2023学年高二下学期期中考试化学试题



