2024高三下·全国·专题练习
解题方法
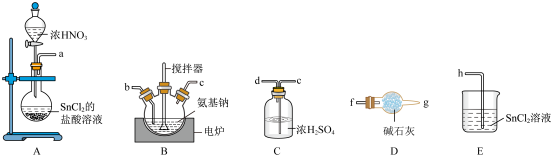
1 . 叠氮化钠(NaN3)可用作汽车安全气囊的气体发生剂。某小组对叠氮化钠的制备和产品纯度测定进行相关探究。
查阅资料:①叠氮化钠可以由氨基钠(NaNH2)和N2O为原料加热制得,其中N2O的制备反应为 。
。
②氨基钠易氧化、易潮解;NaN3能与强酸反应生成HN3,HN3不稳定,易爆炸。
③N2O有强氧化性,不与酸、碱反应。
回答下列问题:
Ⅰ.制备NaN3_______ →h。
查阅资料:①叠氮化钠可以由氨基钠(NaNH2)和N2O为原料加热制得,其中N2O的制备反应为
 。
。②氨基钠易氧化、易潮解;NaN3能与强酸反应生成HN3,HN3不稳定,易爆炸。
③N2O有强氧化性,不与酸、碱反应。
回答下列问题:
Ⅰ.制备NaN3
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
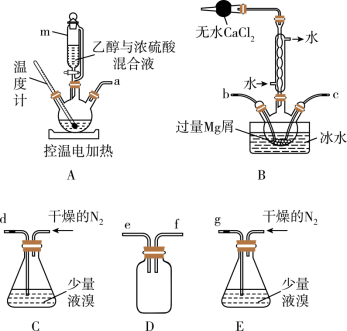
2 . 无水溴化镁常常做催化剂。选用如图所示装置(夹持装置略)采用镁屑与液溴为原料制备无水MgBr2。
①乙醚的熔点为34.6℃,沸点为132℃。
②Mg和Br2剧烈反应,放出大量的热;MgBr2具有强吸水性;MgBr2能与乙醚发生反应MgBr2+3C2H5OC2H5→MgBr2•3C2H5OC2H5。
实验主要步骤如下:
Ⅰ.选用上述部分装置,正确连接,检查装置的气密性。向装置中加入药品。
Ⅱ.加热装置A,迅速升温至140℃,并保持140℃加热一段时间,停止加热。
Ⅲ.通入干燥的氮气,让液溴缓慢进入装置B中,直至完全加入。
IV.装置B中反应完毕后恢复至室温,过滤反应物,将得到的滤液转移至干燥的烧瓶中,在冰水中冷却,析出晶体,再过滤得三乙醚合溴化镁粗产品。
V.用苯洗涤粗产品,减压过滤,得三乙醚合溴化镁,将其加热至160℃分解得无水MgBr2。回答下列问题:
(1)装置D的作用是_______ 。
(2)装置A中使用仪器m的优点是_______ 。
(3)步骤V采用减压过滤(使容器内压强降低,以达到固液快速分离)。下列装置可用作减压过滤的是_______ (填序号)。_______ 。
①乙醚的熔点为34.6℃,沸点为132℃。
②Mg和Br2剧烈反应,放出大量的热;MgBr2具有强吸水性;MgBr2能与乙醚发生反应MgBr2+3C2H5OC2H5→MgBr2•3C2H5OC2H5。
实验主要步骤如下:
Ⅰ.选用上述部分装置,正确连接,检查装置的气密性。向装置中加入药品。
Ⅱ.加热装置A,迅速升温至140℃,并保持140℃加热一段时间,停止加热。
Ⅲ.通入干燥的氮气,让液溴缓慢进入装置B中,直至完全加入。
IV.装置B中反应完毕后恢复至室温,过滤反应物,将得到的滤液转移至干燥的烧瓶中,在冰水中冷却,析出晶体,再过滤得三乙醚合溴化镁粗产品。
V.用苯洗涤粗产品,减压过滤,得三乙醚合溴化镁,将其加热至160℃分解得无水MgBr2。回答下列问题:
(1)装置D的作用是
(2)装置A中使用仪器m的优点是
(3)步骤V采用减压过滤(使容器内压强降低,以达到固液快速分离)。下列装置可用作减压过滤的是
您最近半年使用:0次
3 . 环己烯是一种有机合成的原料,还可用作溶剂、萃取剂等。实验室由环己醇制备环己烯的反应化学方程式如下: 。
。
| 物质 | 用量 | 熔点/℃ | 沸点/℃ | 密度/(g·cm-3) | 与水的共沸物 |
| 环己醇 | 10.0mL | 22.0 | 161.0 | 0.9624 | 水80%,沸点97.8℃ |
| 环己烯 | -104.0 | 83.0 | 0.8098 | 水10%,沸点70.8℃ | |
| 85%磷酸 | 5.0mL | 12.4 | 1.8340 |
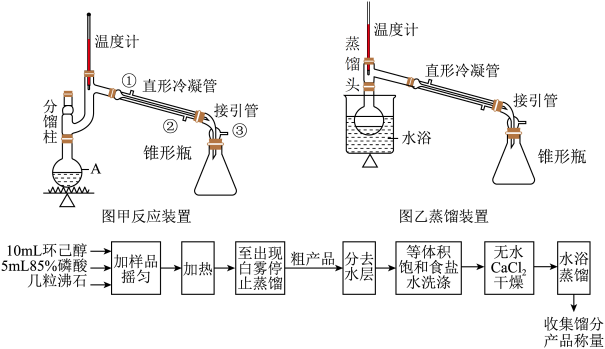
(1)装置甲明火受热时,最适宜
a.直接 b.隔石棉网 c.隔陶土网
(2)直形冷凝管中通入冷水时,冷水从
(3)对反应装置“加热”时,分馏柱侧管处温度要控制在90℃左右,不能太低,也不能太高的原因是
(4)该环己烯制备实验中使用浓磷酸作催化剂,而不用浓硫酸的优点是
(5)用饱和食盐水洗涤粗产品的作用是

a.82.0% b.84.1% c.85.2% d.91.3%
您最近半年使用:0次
解题方法
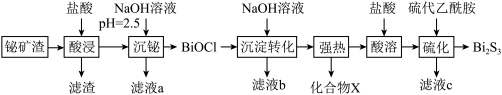
4 . 硫化铋(Bi2S3)广泛应用于太阳能电池、光电二极管及红外光谱学等。以铋矿渣(含Bi2O3、Fe2O3、CuO、Ag2O、Al2O3等)为原料制备Bi2S3的一种工艺流程如下。
②该工艺条件下,部分金属离子形成氢氧化物沉淀的pH如下表:
③常温下,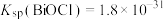 、
、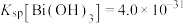 。
。
请回答下列问题:
(1)提高“酸浸”反应速率的措施是___________ (任答1条);“酸浸”中,形成“滤渣”的主要反应的离子方程式是___________ 。
(2)“滤液a”中主要的金属阳离有Fe3+、Cu2+___________ 。
(3)“沉铋”后所得BiOCl固体中含 杂质,设计实验去除BiOCl固体中含有的
杂质,设计实验去除BiOCl固体中含有的 杂质:
杂质:___________ 。
(4)“酸溶”时需加入过量的盐酸,盐酸过量的目的是___________ 、___________ 。
(5)已知常温时,BiOCl在水溶液中存在平衡: ,该反应的平衡常数为K,达到平衡时测得溶液pH=13,
,该反应的平衡常数为K,达到平衡时测得溶液pH=13,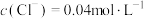 ,则K=
,则K=___________ 。
(6)化合物X的VSEPR模型是___________ 。
(7)已知 (硫代乙酰胺)
(硫代乙酰胺)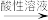
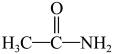 (乙酰胺)+H2S,则“硫化”的离子方程式为
(乙酰胺)+H2S,则“硫化”的离子方程式为___________ 。
②该工艺条件下,部分金属离子形成氢氧化物沉淀的pH如下表:
| 离子 | Fe3+ | Al3+ | Cu2+ |
| 开始沉淀时的pH | 1.5 | 3.6 | 4.5 |
| 沉淀完全时的pH | 3.2 | 4.7 | 6.7 |
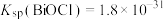 、
、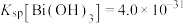 。
。请回答下列问题:
(1)提高“酸浸”反应速率的措施是
(2)“滤液a”中主要的金属阳离有Fe3+、Cu2+
(3)“沉铋”后所得BiOCl固体中含
 杂质,设计实验去除BiOCl固体中含有的
杂质,设计实验去除BiOCl固体中含有的 杂质:
杂质:(4)“酸溶”时需加入过量的盐酸,盐酸过量的目的是
(5)已知常温时,BiOCl在水溶液中存在平衡:
 ,该反应的平衡常数为K,达到平衡时测得溶液pH=13,
,该反应的平衡常数为K,达到平衡时测得溶液pH=13,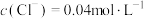 ,则K=
,则K=(6)化合物X的VSEPR模型是
(7)已知
 (硫代乙酰胺)
(硫代乙酰胺)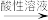
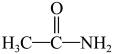 (乙酰胺)+H2S,则“硫化”的离子方程式为
(乙酰胺)+H2S,则“硫化”的离子方程式为
您最近半年使用:0次
2024高三下·全国·专题练习
5 . 盐湖卤水(主要含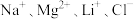 、
、 和硼酸根等)是锂盐的重要来源。一种以高镁卤水为原料经两段除镁制备
和硼酸根等)是锂盐的重要来源。一种以高镁卤水为原料经两段除镁制备 的工艺流程如下:
的工艺流程如下: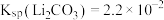 。相关化合物的溶解度与温度的关系如图所示。
。相关化合物的溶解度与温度的关系如图所示。
(1)含硼固体中的 在水中存在平衡:
在水中存在平衡: (常温下,
(常温下,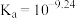 );
); 与
与 溶液反应可制备硼砂
溶液反应可制备硼砂 。常温下,在
。常温下,在 硼砂溶液中,
硼砂溶液中, 水解生成等物质的量浓度的
水解生成等物质的量浓度的 和
和 ,该水解反应的离子方程式为
,该水解反应的离子方程式为_____ ,该溶液
_____ 。
(2)滤渣Ⅰ的主要成分是_____ (填化学式);精制Ⅰ后溶液中 的浓度为
的浓度为 ,则常温下精制Ⅱ过程中
,则常温下精制Ⅱ过程中 浓度应控制在
浓度应控制在_____  以下。若脱硼后直接进行精制Ⅰ,除无法回收
以下。若脱硼后直接进行精制Ⅰ,除无法回收 外,还将增加
外,还将增加_____ 的用量(填化学式)。
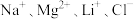 、
、 和硼酸根等)是锂盐的重要来源。一种以高镁卤水为原料经两段除镁制备
和硼酸根等)是锂盐的重要来源。一种以高镁卤水为原料经两段除镁制备 的工艺流程如下:
的工艺流程如下:
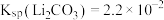 。相关化合物的溶解度与温度的关系如图所示。
。相关化合物的溶解度与温度的关系如图所示。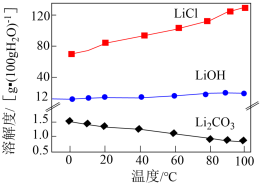
(1)含硼固体中的
 在水中存在平衡:
在水中存在平衡: (常温下,
(常温下,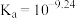 );
); 与
与 溶液反应可制备硼砂
溶液反应可制备硼砂 。常温下,在
。常温下,在 硼砂溶液中,
硼砂溶液中, 水解生成等物质的量浓度的
水解生成等物质的量浓度的 和
和 ,该水解反应的离子方程式为
,该水解反应的离子方程式为
(2)滤渣Ⅰ的主要成分是
 的浓度为
的浓度为 ,则常温下精制Ⅱ过程中
,则常温下精制Ⅱ过程中 浓度应控制在
浓度应控制在 以下。若脱硼后直接进行精制Ⅰ,除无法回收
以下。若脱硼后直接进行精制Ⅰ,除无法回收 外,还将增加
外,还将增加
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
6 . 粗铜精炼的副产品铜阳极泥中含有Au、Ag、Ag2Se、Cu2Se等物质,其含量远高于常规开采的矿石,是提取稀贵金属和硒的重要原料,其中一种分离提取的工艺流程如下: 的溶度积常数
的溶度积常数
②常温下,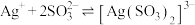 的平衡常数
的平衡常数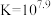
(1) 的作用为
的作用为___________ ;将滤液2返回“分银”工序循环使用,发现循环多次后银的浸出率降低,可能的原因是___________ 。

 的溶度积常数
的溶度积常数
②常温下,
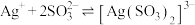 的平衡常数
的平衡常数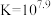
(1)
 的作用为
的作用为
您最近半年使用:0次
2024高三下·全国·专题练习
7 . 镓是优良的半导体材料。氮化镓是制作发光二极管的新材料,用于雷达、卫星通信设备等。某工厂利用铝土矿(主要成分为 、
、 ,还有少量
,还有少量 等杂质)制备氮化镓流程如下:
等杂质)制备氮化镓流程如下:
②当溶液中可溶组分浓度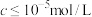 时,可认为已除尽。
时,可认为已除尽。
③金属离子氢氧化物的溶度积(25℃)
④ 、
、 均为两性,
均为两性, 的酸性略强于
的酸性略强于 。
。
回答下列问题:
(1)“二次酸化”中 与足量
与足量 发生反应的离子方程式为
发生反应的离子方程式为______ 。
(2)“电解”可得金属镓(铝不干扰镓盐的电解),写出阴极电极反应式______ 。
(3)“合成”得到的三甲基镓与氨反应得到氮化镓,写出此反应的化学方程式______ 。
 、
、 ,还有少量
,还有少量 等杂质)制备氮化镓流程如下:
等杂质)制备氮化镓流程如下:
②当溶液中可溶组分浓度
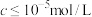 时,可认为已除尽。
时,可认为已除尽。③金属离子氢氧化物的溶度积(25℃)
 |  |  | |
 | 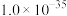 | 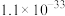 |  |
 、
、 均为两性,
均为两性, 的酸性略强于
的酸性略强于 。
。回答下列问题:
(1)“二次酸化”中
 与足量
与足量 发生反应的离子方程式为
发生反应的离子方程式为(2)“电解”可得金属镓(铝不干扰镓盐的电解),写出阴极电极反应式
(3)“合成”得到的三甲基镓与氨反应得到氮化镓,写出此反应的化学方程式
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
8 . 超纯 是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯
是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯 方面取得了显著成果,工业上以粗镓为原料,制备超纯
方面取得了显著成果,工业上以粗镓为原料,制备超纯 的工艺流程如下:
的工艺流程如下: 的化学性质和
的化学性质和 相似,
相似, 的熔点为
的熔点为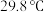 ;
;
② (乙醚)和
(乙醚)和 (三正辛胺)在上述流程中可作为配体;
(三正辛胺)在上述流程中可作为配体;
③相关物质的沸点:
回答下列问题:
(1)“电解精炼”装置如图所示,电解池温度控制在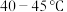 的原因是
的原因是_______ ,阴极的电极反应式为_______ ;
 是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯
是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯 方面取得了显著成果,工业上以粗镓为原料,制备超纯
方面取得了显著成果,工业上以粗镓为原料,制备超纯 的工艺流程如下:
的工艺流程如下: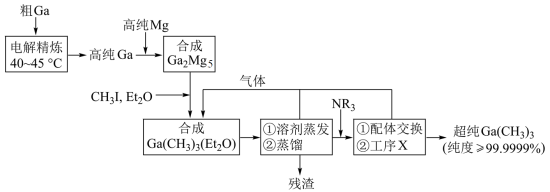
 的化学性质和
的化学性质和 相似,
相似, 的熔点为
的熔点为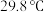 ;
;②
 (乙醚)和
(乙醚)和 (三正辛胺)在上述流程中可作为配体;
(三正辛胺)在上述流程中可作为配体;③相关物质的沸点:
| 物质 | 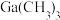 |  | 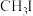 |  |
沸点/ | 55.7 | 34.6 | 42.4 | 365.8 |
(1)“电解精炼”装置如图所示,电解池温度控制在
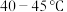 的原因是
的原因是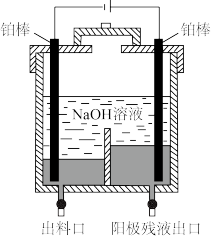
您最近半年使用:0次
2024高三下·全国·专题练习
9 . 稀土( )包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
)包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下: 熔点为
熔点为 ;月桂酸和
;月桂酸和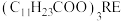 均难溶于水。该工艺条件下,稀土离子保持
均难溶于水。该工艺条件下,稀土离子保持 价不变;
价不变;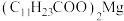 的
的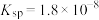 ,
, 开始溶解时的pH为8.8;有关金属离子沉淀的相关pH见下表。
开始溶解时的pH为8.8;有关金属离子沉淀的相关pH见下表。
(1)“氧化调pH”中,化合价有变化的金属离子是_______ 。
(2)“过滤1”前,用 溶液调pH至
溶液调pH至_______ 的范围内,该过程中 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(3)①“加热搅拌”有利于加快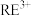 溶出、提高产率,其原因是
溶出、提高产率,其原因是_______ 。
②“操作X”的过程为:先_______ ,再固液分离。
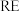 )包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
)包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下: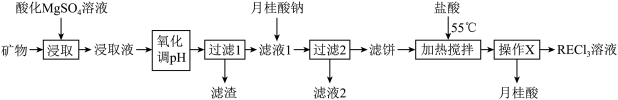
 熔点为
熔点为 ;月桂酸和
;月桂酸和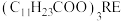 均难溶于水。该工艺条件下,稀土离子保持
均难溶于水。该工艺条件下,稀土离子保持 价不变;
价不变;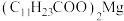 的
的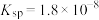 ,
, 开始溶解时的pH为8.8;有关金属离子沉淀的相关pH见下表。
开始溶解时的pH为8.8;有关金属离子沉淀的相关pH见下表。| 离子 |  |  |  | 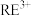 |
| 开始沉淀时的pH | 8.8 | 1.5 | 3.6 | 6.2~7.4 |
| 沉淀完全时的pH | / | 3.2 | 4.7 | / |
(1)“氧化调pH”中,化合价有变化的金属离子是
(2)“过滤1”前,用
 溶液调pH至
溶液调pH至 发生反应的离子方程式为
发生反应的离子方程式为(3)①“加热搅拌”有利于加快
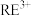 溶出、提高产率,其原因是
溶出、提高产率,其原因是②“操作X”的过程为:先
您最近半年使用:0次
2024高三下·全国·专题练习
10 . 学习小组利用废银催化剂制备乙炔银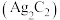 和酸性乙炔银
和酸性乙炔银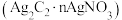 。已知乙炔银和酸性乙炔银在受热时均易发生分解。
。已知乙炔银和酸性乙炔银在受热时均易发生分解。
①制取乙炔。利用如图装置制取纯净的乙炔。 的溶液中通入乙炔可得到乙炔银沉淀。
的溶液中通入乙炔可得到乙炔银沉淀。
(1)将过滤所得滤渣置于小烧杯中,利用丙酮反复多次冲洗沉淀。检验滤渣已经洗净的实验方案是_______ 。
(2)准确称取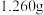 样品,用浓硝酸完全溶解后,定容得
样品,用浓硝酸完全溶解后,定容得 溶液,取
溶液,取 于锥形瓶中,以
于锥形瓶中,以 作指示剂,用
作指示剂,用 标准溶液进行滴定
标准溶液进行滴定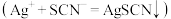 ,终点时消耗标准溶液的体积为
,终点时消耗标准溶液的体积为 。
。
滴定终点的现象为_______ 。通过计算确定n的数值_______ (写出计算过程)。
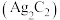 和酸性乙炔银
和酸性乙炔银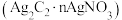 。已知乙炔银和酸性乙炔银在受热时均易发生分解。
。已知乙炔银和酸性乙炔银在受热时均易发生分解。①制取乙炔。利用如图装置制取纯净的乙炔。
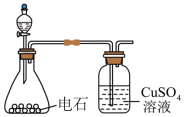
 的溶液中通入乙炔可得到乙炔银沉淀。
的溶液中通入乙炔可得到乙炔银沉淀。(1)将过滤所得滤渣置于小烧杯中,利用丙酮反复多次冲洗沉淀。检验滤渣已经洗净的实验方案是
(2)准确称取
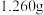 样品,用浓硝酸完全溶解后,定容得
样品,用浓硝酸完全溶解后,定容得 溶液,取
溶液,取 于锥形瓶中,以
于锥形瓶中,以 作指示剂,用
作指示剂,用 标准溶液进行滴定
标准溶液进行滴定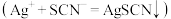 ,终点时消耗标准溶液的体积为
,终点时消耗标准溶液的体积为 。
。滴定终点的现象为
您最近半年使用:0次



