21. 研究氮、硫、碳及其化合物的转化对于环境的改善有重大意义,可减少如雾霾天气、酸雨、酸雾等环境污染问题。
(1)在一定条件下,CH
4可与NO
x反应除去NO
x ,已知有下列热化学方程式:
①CH
4(g)+2O
2(g) = CO
2(g)+2H
2O(l) Δ
H1 =-890.3 kJ·mol
-1②N
2(g)+2O
2(g)

2NO
2(g) Δ
H2 =+67.0 kJ·mol
-1③H
2O(g)=H
2O(l)
Δ
H3 =-41.0 kJ·mol
-1则CH
4(g)+2NO
2(g)

CO
2(g)+2H
2O(g)+N
2(g) Δ
H =
____kJ·mol
-1。
(2) SO
2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO
2发生催化氧化的反应为2SO
2(g)+O
2(g)

2SO
3(g)。在恒温恒容下,往一密闭容器通入SO
2和O
2[
n(SO
2)∶
n(O
2)=2∶1],测得容器内总压强在不同温度下与反应时间的关系如图所示。

①图中
C点时,SO
2的转化率为
________________________________________。
②图中
B点的
Kp=
________(
Kp为压强平衡常数,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3) 已知4NH
3(g)+6NO(g)

5N
2(g)+6H
2O(g) Δ
H1=-1800 kJ·mol
-1。将2 mol NH
3、3 mol NO的混合气体分别置于a、b、c三个10 L恒容密闭容器中,使反应在不同条件下进行,反应过程中
c(N
2)随时间的变化如图所示。
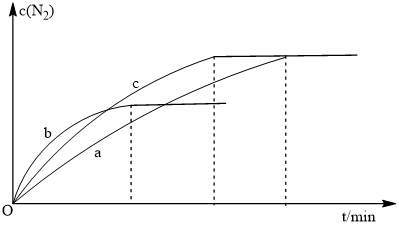
①与容器a中的反应相比,容器b中反应改变的实验条件可能是
_________,判断的依据是
__________________________________________________________。
②一定温度下,下列能说明反应已达到平衡状态的是
____(填字母)。
A.H
2O(g)与NO的生成速率相等
B.混合气体的密度保持不变
C.Δ
H保持不变
D.容器的总压强保持不变
(4)利用人工光合作用,借助太阳能使CO
2和H
2O转化为HCOOH,如图所示。在催化剂b表面发生的电极反应为
______________________________________