18. 甲烷和水蒸气催化制氢主要有如下两个反应:
①
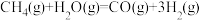
Δ
H=+206kJ/mol
②
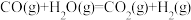
Δ
H=-41kJ/mol
恒定压强为

时,将
n(CH
4)∶
n(H
2O)=1∶3的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。
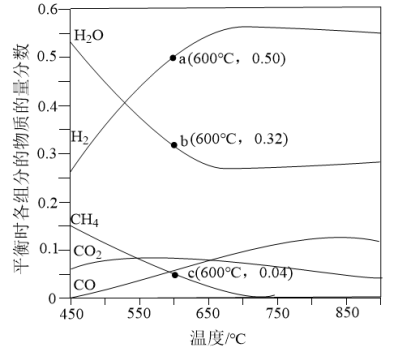
回答下列问题:
(1)写出

与

生成

和

的热化学方程式:
_______。
(2)关于甲烷和水蒸气催化制氢反应,下列叙述正确的是
_______(填标号)。
A.恒温、恒容条件下,加入惰性气体,压强增大,反应速率加快
B.恒温、恒容条件下,加入水蒸气,活化分子百分数增大,反应速率加快
C.升高温度,活化分子百分数增大,有效碰撞频率增大,反应速率加快
D.加入合适的催化剂,降低反应温度也能实现平衡转化率不变
(3)系统中

的含量,在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
①低于700℃,
_______;
②高于700℃,
_______。
(4)已知投料比为
n(CH
4)∶
n(H
2O)=1∶3的混合气体,
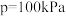
。600℃时,

的平衡转化率为
_______,反应①的平衡常数的计算式为
 _______
_______(

是以分压表示的平衡常数,分压=总压×物质的量分数)。