1 . 光伏材料是指能将太阳能直接转换成电能的材料,又称太阳电池材料,只有半导体材料具有这种功能。可作太阳电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe、CuInSe等。
(1)已知As在元素周期表中的位置为___________ ,根据As的价层电子排布可知As在_______ 区;与As同周期且核外未成对电子数最多的元素的价层电子的轨道表示式为____________ ,该元素核外电子占据的最高能级的形状为__________ 。
(2)P、S、Al电负性从大到小的顺序为___________ ,其中Al元素原子核外有________ 种空间运动状态不同的电子。
(3)As元素的第一电离能________ Se元素的第一电离能(填“大于”“小于”或“等于”),原因是____________ 。
(4)太阳电池材料中的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:____________ 。
(1)已知As在元素周期表中的位置为
(2)P、S、Al电负性从大到小的顺序为
(3)As元素的第一电离能
(4)太阳电池材料中的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:
您最近一年使用:0次
2 . 我国科学家研发的水系可逆Zn﹣CO2电池可吸收利用CO2,将两组阴离子、阳离子复合膜反向放置分隔两室。电解液充、放电时,复合膜间的H2O解离成H+和OH﹣,工作原理如图所示。下列说法正确的是
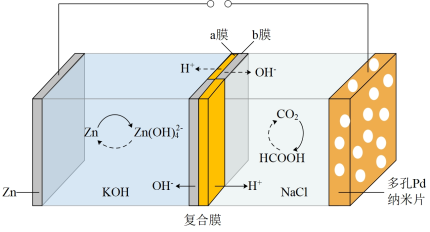
| A.放电时负极反应式是Zn﹣2e﹣=Zn2+ |
| B.标况下,11.2LCO2被吸收时转移2mol电子 |
| C.充电时复合膜中向Zn极移动的离子是H+ |
| D.放电时多孔Pd纳米片上有少量的氯气产生 |
您最近一年使用:0次
3 . 实验室以工业废渣(主要含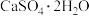 ,还含少量
,还含少量 、
、 、FeO、
、FeO、 )为原料制取(NH4)2SO4晶体和轻质CaCO3,其实验流程如下:
)为原料制取(NH4)2SO4晶体和轻质CaCO3,其实验流程如下:
②溶液中离子浓度≤1.0×10-5mol/L时可认为该离子已经完全沉淀。
回答下列问题:
(1)请写出一条“浸取”时加快速率的措施_______ 。
(2)“浸取”时,CaSO4转化为CaCO3,离子方程式为____________ 。
(3)废渣粉末“浸取”时,反应温度需控制在60~70℃,若温度过高将会使(NH4)2CO3分解而导致CaSO4的转化率下降,合适的加热方式为_______ 。
(4)“滤渣1”成分是_____ (填化学式),加适量H2O2的作用是___________ 。
(5)“调pH”除铁和铝时,应调节溶液的pH≥_______ ;Ksp[Fe(OH)3]=____________ 。
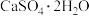 ,还含少量
,还含少量 、
、 、FeO、
、FeO、 )为原料制取(NH4)2SO4晶体和轻质CaCO3,其实验流程如下:
)为原料制取(NH4)2SO4晶体和轻质CaCO3,其实验流程如下: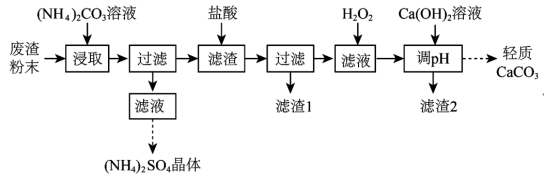
| 金属离子 | Al3+ | Fe3+ | Fe2+ | Ca2+ |
| 开始沉淀时pH | 3.4 | 2.7 | 7.6 | 11.3 |
| 完全沉淀时pH | 4.7 | 3.7 | 9.6 | / |
回答下列问题:
(1)请写出一条“浸取”时加快速率的措施
(2)“浸取”时,CaSO4转化为CaCO3,离子方程式为
(3)废渣粉末“浸取”时,反应温度需控制在60~70℃,若温度过高将会使(NH4)2CO3分解而导致CaSO4的转化率下降,合适的加热方式为
(4)“滤渣1”成分是
(5)“调pH”除铁和铝时,应调节溶液的pH≥
您最近一年使用:0次
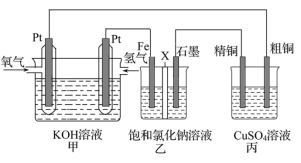
4 . 某同学设计了一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
(1)通入氢气的电极为__________ (填“正极”或 “负极”),负极的电极反应式为___________ 。
(2)石墨电极为__________ (填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入酚酞溶液,__________ (填“铁极”或“石墨极”)区的溶液变红;精铜电极上的电极反应式为________ 。
(3)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的___________ 腐蚀,正极反应为________ 。利用如图装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应置于_________ 处。若X为锌,开关K置于M处,该电化学防护法称为___________ 。
(1)通入氢气的电极为
(2)石墨电极为
(3)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的

您最近一年使用:0次
5 . 丙烯是重要的有机化工原料,丙烷脱氢是工业生产丙烯的重要途径,其化学方程式为C3H8(g) C3H6(g)+H2(g),回答下列相关问题:
C3H6(g)+H2(g),回答下列相关问题:
(1)已知:
Ⅰ.2C3H8(g)+O2(g) 2C3H6(g)+2H2O(g) ΔH1=-238 kJ·mol-1
2C3H6(g)+2H2O(g) ΔH1=-238 kJ·mol-1
Ⅱ.2H2(g)+O2(g) 2H2O(g) ΔH2=-484 kJ·mol-1
2H2O(g) ΔH2=-484 kJ·mol-1
则丙烷脱氢制丙烯的反应C3H8(g) C3H6(g)+H2(g)的ΔH为
C3H6(g)+H2(g)的ΔH为__________ kJ·mol-1
(2)一定温度下,向1 L的密闭容器中充入1 mol C3H8发生脱氢反应,经过10 min达到平衡状态,测得氢气的物质的量为0.5mol。
①0~10 min丙烯的化学反应速率v(C3H6)=__________ mol·L-1·min-1。
②下列情况能说明该反应达到平衡状态的是____________ 。
A.ΔH不变 B.C3H6与H2的物质的量之比保持不变
C.混合气体的总压强不变 D.v正(C3H6)=v逆(C3H8)
③欲提高丙烷转化率,应采取的措施是________ (填字母标号)。
A.降低温度 B.升高温度 C.加催化剂 D.及时分离出H2
④丙烷的平衡转化率是______________ 。
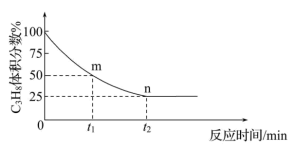
(3)一定温度下,向恒容密闭容器中充入1 mol C3H8,开始压强为p kPa,C3H8的气体体积分数与反应时间的关系如图所示:___________ 。(用含字母p的代数式表示,Kp是用反应体系中气体物质的分压表示的平衡常数,平衡分压=总压×体积分数)。
②已知该反应过程中,v正=k正p(C3H8),v逆=k逆p(C3H6)·p(H2),其中k正、k逆为速率常数,只与温度有关,则图中m点处 =
=_____________ 。
 C3H6(g)+H2(g),回答下列相关问题:
C3H6(g)+H2(g),回答下列相关问题:(1)已知:
Ⅰ.2C3H8(g)+O2(g)
 2C3H6(g)+2H2O(g) ΔH1=-238 kJ·mol-1
2C3H6(g)+2H2O(g) ΔH1=-238 kJ·mol-1Ⅱ.2H2(g)+O2(g)
 2H2O(g) ΔH2=-484 kJ·mol-1
2H2O(g) ΔH2=-484 kJ·mol-1则丙烷脱氢制丙烯的反应C3H8(g)
 C3H6(g)+H2(g)的ΔH为
C3H6(g)+H2(g)的ΔH为(2)一定温度下,向1 L的密闭容器中充入1 mol C3H8发生脱氢反应,经过10 min达到平衡状态,测得氢气的物质的量为0.5mol。
①0~10 min丙烯的化学反应速率v(C3H6)=
②下列情况能说明该反应达到平衡状态的是
A.ΔH不变 B.C3H6与H2的物质的量之比保持不变
C.混合气体的总压强不变 D.v正(C3H6)=v逆(C3H8)
③欲提高丙烷转化率,应采取的措施是
A.降低温度 B.升高温度 C.加催化剂 D.及时分离出H2
④丙烷的平衡转化率是
(3)一定温度下,向恒容密闭容器中充入1 mol C3H8,开始压强为p kPa,C3H8的气体体积分数与反应时间的关系如图所示:
②已知该反应过程中,v正=k正p(C3H8),v逆=k逆p(C3H6)·p(H2),其中k正、k逆为速率常数,只与温度有关,则图中m点处
 =
=
您最近一年使用:0次
6 . 某温度下,饱和溶液中-lg[c(S )]、-lg[c(C2
)]、-lg[c(C2 )]与-lg[c(Ca2+)]的关系如图所示。已知:该温度下,Ksp(CaC2O4)<Ksp(CaSO4)。下列说法错误的是
)]与-lg[c(Ca2+)]的关系如图所示。已知:该温度下,Ksp(CaC2O4)<Ksp(CaSO4)。下列说法错误的是
 )]、-lg[c(C2
)]、-lg[c(C2 )]与-lg[c(Ca2+)]的关系如图所示。已知:该温度下,Ksp(CaC2O4)<Ksp(CaSO4)。下列说法错误的是
)]与-lg[c(Ca2+)]的关系如图所示。已知:该温度下,Ksp(CaC2O4)<Ksp(CaSO4)。下列说法错误的是 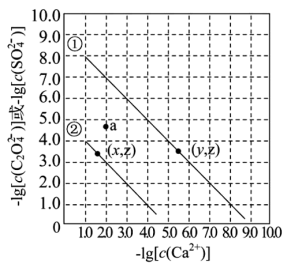
| A.曲线①表示CaC2O4的沉淀溶解平衡曲线 |
| B.a点可表示CaSO4的不饱和溶液 |
C.CaC2O4与CaSO4共沉淀时,溶液中c(S )∶c(C2 )∶c(C2 )=10y-x )=10y-x |
| D.将浓度均为0.001 mol·L-1的CaCl2溶液和Na2C2O4溶液等体积混合(忽略溶液体积变化),无沉淀产生 |
您最近一年使用:0次
7 . 下列各组离子在相应的条件下一定能大量共存的是
A.能使pH试纸变红的溶液中:CO 、K+、Cl-、Na+ 、K+、Cl-、Na+ |
B.在含Fe3+的溶液中:SO 、NH 、NH 、CO 、CO 、Cl- 、Cl- |
C.澄清透明溶液:Na+、Cu2+、Cl-、SO |
D.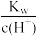 =10-10mol·L-1的溶液中:Na+、HCO =10-10mol·L-1的溶液中:Na+、HCO 、Cl-、K+ 、Cl-、K+ |
您最近一年使用:0次
8 . 短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的2p轨道上有3个电子,Z是元素周期表中电负性最大的元素,W与Y同主族。下列说法正确的是
| A.原子半径:r(W)>r(Z)>r(Y)>r(X) |
| B.X的氧化物的水化物一定是强酸 |
| C.非金属性:Z>Y>X>W |
| D.W的简单氢化物的热稳定性比Y的强 |
您最近一年使用:0次
9 . 由N2O和NO反应生成N2和NO2的能量变化如图所示。下列说法正确的是
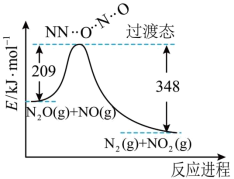
| A.该反应为吸热反应 |
| B.反应物的总键能小于生成物的总键能 |
| C.加入催化剂,可以减少反应热,加快反应速率 |
| D.升高温度,正反应速率增大逆反应速率减小 |
您最近一年使用:0次
解题方法
10 . 下列排列顺序正确的是
A.沸点: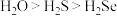 | B.离子半径: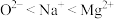 |
| C.金属性:K>Na>Rb | D.热稳定性:HF>HCl>HBr |
您最近一年使用:0次



