名校
解题方法
1 . 甲醇作为燃料,在化石能源和可再生能源时期均有广泛的应用前景。
(1)甲醇可以替代汽油和柴油作为内燃机燃料。汽油的主要成分之一是辛烷[C8H18(l)]。已知:25°C、101 kPa 时,1 molC8H18(l)完全燃烧生成气态二氧化碳和液态水,放出5518kJ热量。该反应燃烧热的热化学方程式为_______ 。
(2)甲醇的合成以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。_________ 。
②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的ΔH______ 。(填“变大”“变小”或“不变”)
(3)已知下列反应的焓变
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1= -870.3kJ/mol
②C(s)+O2(g) =CO2(g) ΔH2= -393.5kJ/mol
③2H2(g)+O2(g) =2H2O(l) ΔH3= -285.8kJ/mol
试计算反应2C(s)+2H2(g)+O2(g) =CH3COOH(l)的焓变ΔH=__________ 。
(1)甲醇可以替代汽油和柴油作为内燃机燃料。汽油的主要成分之一是辛烷[C8H18(l)]。已知:25°C、101 kPa 时,1 molC8H18(l)完全燃烧生成气态二氧化碳和液态水,放出5518kJ热量。该反应燃烧热的热化学方程式为
(2)甲醇的合成以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。
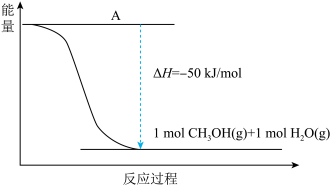
②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的ΔH
(3)已知下列反应的焓变
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1= -870.3kJ/mol
②C(s)+O2(g) =CO2(g) ΔH2= -393.5kJ/mol
③2H2(g)+O2(g) =2H2O(l) ΔH3= -285.8kJ/mol
试计算反应2C(s)+2H2(g)+O2(g) =CH3COOH(l)的焓变ΔH=
您最近一年使用:0次
名校
解题方法
2 . 下列实验方案或装置能达到目的的是
| 选项 | 目的 | 实验方案或装置 |
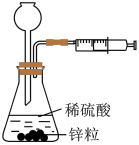
| A | 定量测量化学反应速率 |
|
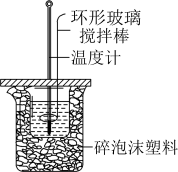
| B | 测定酸碱中和热 |
|
| C | 探究浓度影响化学平衡移动的因素 | 水煤气的反应C(s)+H2O(g) CO(g)+ H2(g),增加碳的量,平衡向正反应方向移动。 CO(g)+ H2(g),增加碳的量,平衡向正反应方向移动。 |
| D | 探究浓度对反应速率的影响 | 分别向两支盛有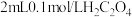 溶液的试管中分别加入 溶液的试管中分别加入 和 和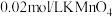 溶液,比较溶液褪色快慢 溶液,比较溶液褪色快慢 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . N2(g)+3H2(g) 2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是
2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是
①降温 ②恒压通入惰性气体 ③增加N2的浓度 ④加压 ⑤催化剂
 2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是
2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是①降温 ②恒压通入惰性气体 ③增加N2的浓度 ④加压 ⑤催化剂
| A.①④ | B.①②③⑤ | C.②③⑤ | D.③④ |
您最近一年使用:0次
名校
4 . 在密闭容器中A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示。已知v(A)、v(B)、v(C)之间有以下关系:2v(B)=3v(A)、3v(C)=2v(B),则此反应可表示为
| A.2A+3B=2C | B.3A+B=2C | C.A+3B=2C | D.A+B=C |
您最近一年使用:0次
名校
解题方法
5 . 现有五种元素A、B、C、D、E,其中A、B、C为三个不同周期的短周期元素,E为第四周期元素。请根据下列相关信息,回答下列问题:
(1)C基态原子中能量最高的电子,其电子云在空间有___________ 个伸展方向,C简单离子核外有___________ 种运动状态不同的电子。
(2)A2B2难溶于CS2,简要说明理由:______________ 。
(3)ED3分子的VSEPR模型名称为____________ ,空间构型为____________ 。
(4)下列气态分子BCl3、CCl4、H2O和BeCl2中,其键角由大到小的顺序为_____________ 。
(5)键的极性对物质的化学性质有重要影响。已知一些常见电子基团的吸电子效应的强度:RCO﹣>﹣F>﹣Cl>﹣Br>﹣I>﹣C≡CH>﹣C6H5>﹣H,则下列物质酸性由强到弱的顺序是___________ (填序号)。
A.CH3COOH B.ClCH2COOH C.HC≡CCH2COOH D.C6H5CH2COOH
元素 | 相关信息 |
A | 核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
B | 原子核外p电子数与s电子数相等 |
C | 基态原子的价电子排布为nsn-1npn+1 |
D | 能层数与C相同,且电负性比C大 |
E | 元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
(2)A2B2难溶于CS2,简要说明理由:
(3)ED3分子的VSEPR模型名称为
(4)下列气态分子BCl3、CCl4、H2O和BeCl2中,其键角由大到小的顺序为
(5)键的极性对物质的化学性质有重要影响。已知一些常见电子基团的吸电子效应的强度:RCO﹣>﹣F>﹣Cl>﹣Br>﹣I>﹣C≡CH>﹣C6H5>﹣H,则下列物质酸性由强到弱的顺序是
A.CH3COOH B.ClCH2COOH C.HC≡CCH2COOH D.C6H5CH2COOH
您最近一年使用:0次
名校
6 . 恒温下,反应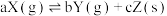 达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是
达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是
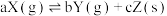 达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是
达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是| A.a>b | B.a<b+c | C.a=b+c | D.a<b |
您最近一年使用:0次
2024-04-21更新
|
71次组卷
|
2卷引用:宁夏回族自治区石嘴山市平罗县平罗中学2023-2024学年高二下学期5月期中化学试题
名校
7 . 回答下列问题:
(1)碳是形成化合物种类最多的元素。
①C元素是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是___________ (填字母)。 )与二甲醚(
)与二甲醚( )的分子式均为
)的分子式均为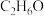 ,但
,但 的沸点高于
的沸点高于 的沸点,其原因是
的沸点,其原因是______________ 。
(2)肼的性质与氨气相似,易溶于水,可发生两步电离过程,第一步电离过程 ,试写出第二步电离过程
,试写出第二步电离过程_______________ 。常温下,某浓度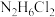 溶液的pH为4,则该溶液中水电离出的
溶液的pH为4,则该溶液中水电离出的
___________ 。
(3)液氨中存在平衡: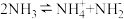 。如图1所示为电解池装置,以
。如图1所示为电解池装置,以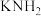 的液氨溶液为电解液,电解过程中a、b两个惰性电极上都有气泡产生。b电极连接的是电源的
的液氨溶液为电解液,电解过程中a、b两个惰性电极上都有气泡产生。b电极连接的是电源的___________ (填“正”或“负”)极;a电极的反应为____________ 。电解过程中,阴极附近 浓度
浓度__________ (填“增大”“减小”或“不变”);理论上阴、阳极产生的气体物质的量之比为_____________ 。 键的数目为
键的数目为___________ 。
(1)碳是形成化合物种类最多的元素。
①C元素是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是
a.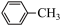 b.
b. c.
c. d.
d.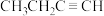
 )与二甲醚(
)与二甲醚( )的分子式均为
)的分子式均为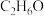 ,但
,但 的沸点高于
的沸点高于 的沸点,其原因是
的沸点,其原因是(2)肼的性质与氨气相似,易溶于水,可发生两步电离过程,第一步电离过程
 ,试写出第二步电离过程
,试写出第二步电离过程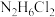 溶液的pH为4,则该溶液中水电离出的
溶液的pH为4,则该溶液中水电离出的
(3)液氨中存在平衡:
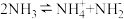 。如图1所示为电解池装置,以
。如图1所示为电解池装置,以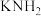 的液氨溶液为电解液,电解过程中a、b两个惰性电极上都有气泡产生。b电极连接的是电源的
的液氨溶液为电解液,电解过程中a、b两个惰性电极上都有气泡产生。b电极连接的是电源的 浓度
浓度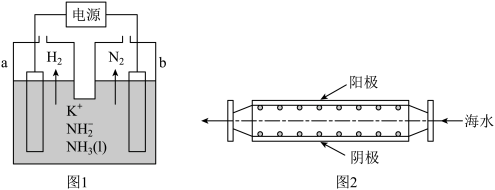
 键的数目为
键的数目为
您最近一年使用:0次
名校
8 . 如图是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
(2)元素①和②可形成原子个数比为 的共价化合物,该分子的空间结构为
的共价化合物,该分子的空间结构为___________ ,中心原子轨道杂化形式为___________ ,该分子为___________ (填“极性分子”或“非极性分子”)。
(3)基态⑧原子中,核外电子占据最高能层的符号是___________ ,基态⑧离子占据的最高能级共有___________ 个原子轨道,其形状是___________ 。
(4)元素⑨的在周期表中的位置____________ ,属于_____ 区,元素⑩的价电子轨道表示式是________________ 。
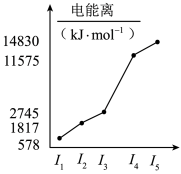
(5)表中所列的某主族元素的电离能情况如下图所示,则该元素是___________ (填元素符号)。

A. | B.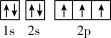 | C. | D. |
(2)元素①和②可形成原子个数比为
 的共价化合物,该分子的空间结构为
的共价化合物,该分子的空间结构为(3)基态⑧原子中,核外电子占据最高能层的符号是
(4)元素⑨的在周期表中的位置
(5)表中所列的某主族元素的电离能情况如下图所示,则该元素是
| A.电负性:③>⑥ | B.最简单的氢化物的稳定性:③<⑥ |
| C.第一电离能:⑤<⑥<⑦ | D.最简单的氢化物的沸点:③>⑥ |
您最近一年使用:0次
名校
9 . 现有下列几种常见物质:①CH3Cl、②O3、③P4、④C60、⑤CO2、⑥HCN、⑦H2O、⑧NH3、⑨BF3、⑩CH4。
(1)这几种物质中,含非极性共价键形成的是______________ (填序号,下同);属于非极性分子的是_______________ 。
(2)属于极性键形成的非极性分子是_______________ ;
(3)将 溶于水,破坏
溶于水,破坏 中的
中的_______________ 键,写出其电离方程式_______________ 。
(4)已知铁的电离能数据如下:
则,铁的第四电离能( )大于第三电离能(
)大于第三电离能( )的可能原因是:
)的可能原因是:_______________ 。
(1)这几种物质中,含非极性共价键形成的是
(2)属于极性键形成的非极性分子是
(3)将
 溶于水,破坏
溶于水,破坏 中的
中的(4)已知铁的电离能数据如下:
电离能/( |
|
|
|
| …… |
Fe | 759 | 1561 | 2597 | 5290 | …… |
 )大于第三电离能(
)大于第三电离能( )的可能原因是:
)的可能原因是:
您最近一年使用:0次
名校
10 . 若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的变化。在变化的各阶段被破坏的粒子间主要的相互作用依次是
| A.分子间作用力;分子间作用力;非极性键 |
| B.分子间作用力;分子间作用力;极性键 |
| C.分子间作用力;极性键;分子间作用力 |
| D.分子间作用力;非极性键;分子间作用力 |
您最近一年使用:0次

 )
)



