解题方法
1 . I.欲配制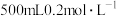 的
的 溶液,可供选用的仪器有①烧杯②托盘天平③药匙④玻璃棒⑤胶头滴管⑥量筒,请回答下列问题:
溶液,可供选用的仪器有①烧杯②托盘天平③药匙④玻璃棒⑤胶头滴管⑥量筒,请回答下列问题:
(1)需要称量 固体的质量为
固体的质量为___________ g。
(2)配制溶液,还缺少的仪器是___________ 。
(3)从下面的操作中,排列正确的操作顺序:___________ (填标号)。
①称量固体
②用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,将洗涤液也注入容量瓶
③固体在烧杯中溶解,恢复至室温,并将溶液注入容量瓶
④容量瓶验漏
⑤将配制好的溶液倒入试剂瓶,并贴上标签
⑥注入蒸馏水,当液面离容量瓶颈部的刻度线1~2cm时,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相切将配制好的溶液倒入试剂瓶,并贴上标签,标签是___________ 。
(4)下列某些操作会导致所配溶液浓度有误差:
①所用的容量瓶未干燥
②所用的烧杯、玻璃棒未洗涤
③定容后,摇匀时发现溶液液面低于刻度线,再滴加蒸馏水
④定容时俯视刻度线
⑤定容时超过刻度线,用胶头滴管吸出溶液
以上操作对所配溶液浓度无影响的是___________ (填标号,以下同),以上操作导致所配溶液浓度偏低的是___________ 。
II.对是否可用 溶液鉴别
溶液鉴别 溶液和
溶液和 溶液有争议,本实验为解决这个问题而设计,如图所示:把
溶液有争议,本实验为解决这个问题而设计,如图所示:把 的
的 溶液滴加到配制好的
溶液滴加到配制好的 的
的 溶液中,结果发现,装置A、B中均有白色沉淀产生,同时装置A烧瓶中产生气体。请回答:
溶液中,结果发现,装置A、B中均有白色沉淀产生,同时装置A烧瓶中产生气体。请回答:
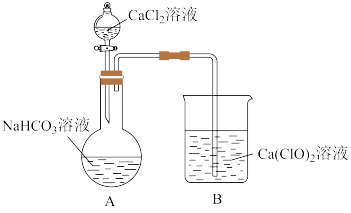
(5)向烧瓶中滴加 溶液的操作是
溶液的操作是___________ 。
(6)烧杯中发生反应的化学方程式为___________ 。
(7)烧瓶中发生反应的离子方程式为___________ 。
结论:三者浓度较大时,不能根据是否有沉淀生成鉴别 溶液和
溶液和 溶液。
溶液。
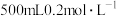 的
的 溶液,可供选用的仪器有①烧杯②托盘天平③药匙④玻璃棒⑤胶头滴管⑥量筒,请回答下列问题:
溶液,可供选用的仪器有①烧杯②托盘天平③药匙④玻璃棒⑤胶头滴管⑥量筒,请回答下列问题:(1)需要称量
 固体的质量为
固体的质量为(2)配制溶液,还缺少的仪器是
(3)从下面的操作中,排列正确的操作顺序:
①称量固体
②用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,将洗涤液也注入容量瓶
③固体在烧杯中溶解,恢复至室温,并将溶液注入容量瓶
④容量瓶验漏
⑤将配制好的溶液倒入试剂瓶,并贴上标签
⑥注入蒸馏水,当液面离容量瓶颈部的刻度线1~2cm时,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相切将配制好的溶液倒入试剂瓶,并贴上标签,标签是
(4)下列某些操作会导致所配溶液浓度有误差:
①所用的容量瓶未干燥
②所用的烧杯、玻璃棒未洗涤
③定容后,摇匀时发现溶液液面低于刻度线,再滴加蒸馏水
④定容时俯视刻度线
⑤定容时超过刻度线,用胶头滴管吸出溶液
以上操作对所配溶液浓度无影响的是
II.对是否可用
 溶液鉴别
溶液鉴别 溶液和
溶液和 溶液有争议,本实验为解决这个问题而设计,如图所示:把
溶液有争议,本实验为解决这个问题而设计,如图所示:把 的
的 溶液滴加到配制好的
溶液滴加到配制好的 的
的 溶液中,结果发现,装置A、B中均有白色沉淀产生,同时装置A烧瓶中产生气体。请回答:
溶液中,结果发现,装置A、B中均有白色沉淀产生,同时装置A烧瓶中产生气体。请回答:
(5)向烧瓶中滴加
 溶液的操作是
溶液的操作是(6)烧杯中发生反应的化学方程式为
(7)烧瓶中发生反应的离子方程式为
结论:三者浓度较大时,不能根据是否有沉淀生成鉴别
 溶液和
溶液和 溶液。
溶液。
您最近一年使用:0次
名校
解题方法
2 . 某化学兴趣小组用如图装置制取并探究氯气的性质。[A装置中发生反应的化学方程式:
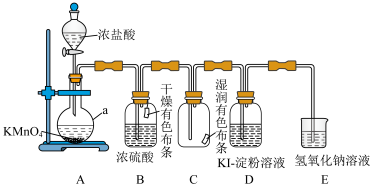
(1)A装置中a仪器的名称是___________ 。
(2)制取氯气反应中 所起的作用是
所起的作用是___________ (填“氧化剂”或“还原剂”)。
(3)实验进行一段时间后,可观察到___________ (填“B”或“C”)装置中有色布条褪色,其褪色原因是___________ 。
(4)当氯气进入D装置后,可观察到溶液颜色变为___________ 填(“红色”或“蓝色”),写出相关反应的化学方程式___________ 。
(5)E装置中发生的反应方程式是___________ 。
(6)实验室常用 与浓盐酸制氯气,写出反应方程式
与浓盐酸制氯气,写出反应方程式___________ 。若已知盐酸浓度小于10 mol/L时则不易被 氧化,现用浓度为12 mol/L的浓盐酸与8.7 g
氧化,现用浓度为12 mol/L的浓盐酸与8.7 g  反应,要使
反应,要使 全部反应掉生成最多氯气,则至少加入这种盐酸
全部反应掉生成最多氯气,则至少加入这种盐酸___________ 毫升?


(1)A装置中a仪器的名称是
(2)制取氯气反应中
 所起的作用是
所起的作用是(3)实验进行一段时间后,可观察到
(4)当氯气进入D装置后,可观察到溶液颜色变为
(5)E装置中发生的反应方程式是
(6)实验室常用
 与浓盐酸制氯气,写出反应方程式
与浓盐酸制氯气,写出反应方程式 氧化,现用浓度为12 mol/L的浓盐酸与8.7 g
氧化,现用浓度为12 mol/L的浓盐酸与8.7 g  反应,要使
反应,要使 全部反应掉生成最多氯气,则至少加入这种盐酸
全部反应掉生成最多氯气,则至少加入这种盐酸
您最近一年使用:0次
解题方法
3 . 过氧化钠可以在呼吸面具和潜水艇中作供氧剂,某小组设计了如下实验装置:
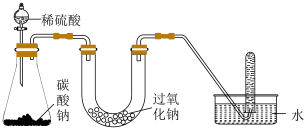
(1)加入药品之前,应该___________ 。打开活塞滴入稀硫酸,锥形瓶、U形管、试管处能观察到的现象分别有___________ 。
(2)实验初期U形管内的生成物除了O2外,还有___________ ,反应中作氧化剂、还原剂的物质分别是___________ 、___________ 。
(3)气体充满试管后,先关闭活塞,再___________ ;然后用大拇指堵住试管口,再把试管移出水面。检验试管中氧气的方法是___________ 。
(4)检验氧气时发现:带火星的木条不会复燃反而熄灭,请结合装置设计的缺陷来进行解释:___________ 。

(1)加入药品之前,应该
(2)实验初期U形管内的生成物除了O2外,还有
(3)气体充满试管后,先关闭活塞,再
(4)检验氧气时发现:带火星的木条不会复燃反而熄灭,请结合装置设计的缺陷来进行解释:
您最近一年使用:0次
名校
解题方法
4 . 1810年,英国化学家戴维以大量事实为依据,确认一种黄绿色气体是一种新元素组成的单质——氯气。某化学兴趣小组同学利用以下装置制备干燥的氯气并对氯气的性质进行探究。
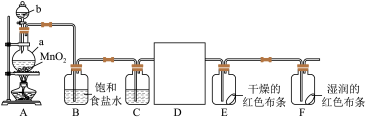
(1)仪器b的名称为___________ 。某同学认为该实验装置存在一处明显的不足,其改进措施为___________ 。
(2)仪器a中发生反应的化学方程式为___________ 。根据氯气的性质D中的收集装置可以选择___________ (填序号)。
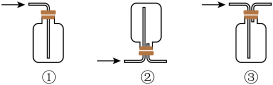
(3)下列有关该实验的说法中不正确 的是___________(填字母)。
(4)实验室还可用等物质的量的 与
与 的水溶液反应制取
的水溶液反应制取 ,同时生成
,同时生成 和NaCl,反应的化学方程式为
和NaCl,反应的化学方程式为___________ 。

(1)仪器b的名称为
(2)仪器a中发生反应的化学方程式为

(3)下列有关该实验的说法中
| A.将b中溶液换为稀盐酸,同样可以产生氯气 |
| B.C中试剂是浓硫酸,目的是干燥氯气 |
| C.F中红色布条褪色,证明氯气具有漂白性 |
| D.可用湿润的淀粉碘化钾试纸检验氯气是否收集满 |
(4)实验室还可用等物质的量的
 与
与 的水溶液反应制取
的水溶液反应制取 ,同时生成
,同时生成 和NaCl,反应的化学方程式为
和NaCl,反应的化学方程式为
您最近一年使用:0次
2023-11-22更新
|
216次组卷
|
2卷引用:浙江省温州市新力量联盟2023-2024学年高一上学期11月期中联考化学试题
名校
解题方法
5 . 过氧化钠常作漂白剂、消毒剂。过氧化钠经常因为保存不当容易吸收空气中 而变质。某课外小组欲用以下装置探究过氧化钠与
而变质。某课外小组欲用以下装置探究过氧化钠与 反应后的产物。试回答下列问题:
反应后的产物。试回答下列问题:

(1)写出A中反应的化学方程式___________ 。
(2)B装置的作用是___________ 。
(3)观察到的实验现象:双球干燥管内淡黄色粉末逐渐转变为白色,点燃的蚊香燃烧更加剧烈。请根据实验现象写出C装置的化学方程式,并用双线桥标出电子转移的方向和数目:___________
(4)该课外小组欲探究某过组化钠样品是否已经变质,取少量样品,溶解,加入___________ 溶液,充分振荡后有白色沉淀,证明 已经变质。
已经变质。
(5)超氧化钾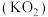 与过氧化钠一样能吸收
与过氧化钠一样能吸收 生成碳酸盐及
生成碳酸盐及 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。
 而变质。某课外小组欲用以下装置探究过氧化钠与
而变质。某课外小组欲用以下装置探究过氧化钠与 反应后的产物。试回答下列问题:
反应后的产物。试回答下列问题:
(1)写出A中反应的化学方程式
(2)B装置的作用是
(3)观察到的实验现象:双球干燥管内淡黄色粉末逐渐转变为白色,点燃的蚊香燃烧更加剧烈。请根据实验现象写出C装置的化学方程式,并用双线桥标出电子转移的方向和数目:
(4)该课外小组欲探究某过组化钠样品是否已经变质,取少量样品,溶解,加入
 已经变质。
已经变质。(5)超氧化钾
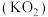 与过氧化钠一样能吸收
与过氧化钠一样能吸收 生成碳酸盐及
生成碳酸盐及 ,写出该反应的化学方程式
,写出该反应的化学方程式
您最近一年使用:0次
解题方法
6 . 请分别写出鉴别以下各组固体物质详细的实验操作及现象:
(1)氯化钠和碳酸钠:___________ 。
(2)碳酸钠和碳酸氢钠:___________ 。
(3)氯化钠和氯化钾:___________ 。
(1)氯化钠和碳酸钠:
(2)碳酸钠和碳酸氢钠:
(3)氯化钠和氯化钾:
您最近一年使用:0次
7 . 为了从海带中制取碘,某学习小组将海带灼烧后,加水溶解配成海带浸取原液(浸取原液中的碘元素主要以I-形式存在),并设计了如下甲、乙两种实验方案:
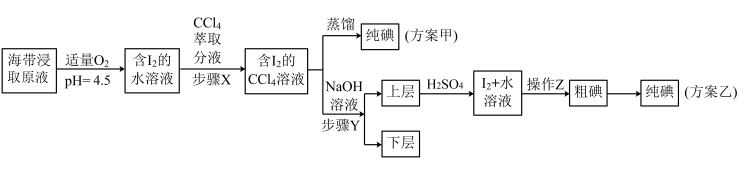
已知:①步骤Y中加NaOH时发生反应:3I2+6NaOH=5NaI+NaIO3+3H2O;
②碘单质常温为紫黑色固体,在通常状况下,100g水中约溶解0.02g碘单质。
请回答:
(1)灼烧海带应该在___________ (填仪器名称)中进行。
(2)分液漏斗使用前须先___________ ;步骤X中,萃取后分液漏斗内观察到的现象是___________ 。
(3)步骤Y中需要控制加入的NaOH溶液的量不宜过多,原因是___________ 。
(4)操作Z的名称是___________ 。
(5)方案甲中采用蒸馏不合理,理由是___________ 。

已知:①步骤Y中加NaOH时发生反应:3I2+6NaOH=5NaI+NaIO3+3H2O;
②碘单质常温为紫黑色固体,在通常状况下,100g水中约溶解0.02g碘单质。
请回答:
(1)灼烧海带应该在
(2)分液漏斗使用前须先
(3)步骤Y中需要控制加入的NaOH溶液的量不宜过多,原因是
(4)操作Z的名称是
(5)方案甲中采用蒸馏不合理,理由是
您最近一年使用:0次
名校
解题方法
8 . “碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用。某兴趣小组对于现有碳捕捉技术进行了研究学习。
(1)利用NaOH溶液来“捕捉”CO2的基本过程如图所示(部分条件及物质未标出)。在流程中可以循环利用的物质有___________ 、___________ (均填化学式)。
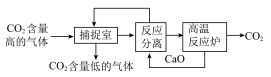
(2)反应分离室中,发生反应的化学方程式为CaO+H2O=Ca(OH)2和___________ (写出一个即可),地球上最高效的碳捕捉过程就是叶绿素催化的光合作用合成葡萄糖。葡萄糖是生物体内的主要供能物质,具有良好的水溶性。20℃时,甲、乙两份葡萄糖饱和溶液的质量分别为200g和300g,在下列条件中,析出晶体质量相同的为___________ (填字母)。
A.两份溶液都降温至10℃ B.甲溶液降温至10℃,乙液降温至0℃
C.两份溶液都蒸发掉20g水 D.甲溶液蒸发掉30g水,乙液蒸发掉20g
(1)利用NaOH溶液来“捕捉”CO2的基本过程如图所示(部分条件及物质未标出)。在流程中可以循环利用的物质有

(2)反应分离室中,发生反应的化学方程式为CaO+H2O=Ca(OH)2和
A.两份溶液都降温至10℃ B.甲溶液降温至10℃,乙液降温至0℃
C.两份溶液都蒸发掉20g水 D.甲溶液蒸发掉30g水,乙液蒸发掉20g
您最近一年使用:0次
名校
解题方法
9 . 某校化学兴趣小组的同学,对一氧化碳还原氧化铁实验作了绿色化改进后制取单质铁( ,
, 是活塞):
是活塞):

(1)关闭 、开启
、开启 ,可以验证CO还原
,可以验证CO还原 的产物。
的产物。
①这是关于气体的实验,实验前必须对装置进行___________ 。
②澄清的石灰水中发生反应的离子方程式为___________ 。
③在e处点燃气体的目的是___________ 。
(2)关闭 ,开启
,开启 ,可以将d口出来的气体再从a通入装置而循环使用。
,可以将d口出来的气体再从a通入装置而循环使用。
①c瓶中应装___________ (填序号)。
A.澄清石灰水 B.水 C.石蕊溶液 D.浓硫酸
②该实验这样改进的主要优点是_______ 。
 ,
, 是活塞):
是活塞):
(1)关闭
 、开启
、开启 ,可以验证CO还原
,可以验证CO还原 的产物。
的产物。①这是关于气体的实验,实验前必须对装置进行
②澄清的石灰水中发生反应的离子方程式为
③在e处点燃气体的目的是
(2)关闭
 ,开启
,开启 ,可以将d口出来的气体再从a通入装置而循环使用。
,可以将d口出来的气体再从a通入装置而循环使用。①c瓶中应装
A.澄清石灰水 B.水 C.石蕊溶液 D.浓硫酸
②该实验这样改进的主要优点是
您最近一年使用:0次
名校
10 . 有A、B、C、D四种化合物,分别由 、
、 、
、 、
、 、
、 中的两种组成,它们具有下列性质:
中的两种组成,它们具有下列性质:
①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(1)推断A、D的化学式。
A:___________ ,D:___________ 。
(2)写出下列反应的离子方程式。
①:B与盐酸反应:____________________________________________ ,
②:C与硫酸反应:____________________________________________ ,
③:E(少量)与澄清石灰水反应:________________________________ 。
④:C与碳酸氢钠(过量)反应:__________________________________ 。
 、
、 、
、 、
、 、
、 中的两种组成,它们具有下列性质:
中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(1)推断A、D的化学式。
A:
(2)写出下列反应的离子方程式。
①:B与盐酸反应:
②:C与硫酸反应:
③:E(少量)与澄清石灰水反应:
④:C与碳酸氢钠(过量)反应:
您最近一年使用:0次



