1 . 下列实验操作、现象和所得结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向盛有2mL0.1mol。L-1AgNO3溶液的试管中滴加4滴0.1mol。L-1NaCl溶液;振荡试管,然后再向其中滴加4滴0.1mol·L-1KI溶液 | 先生成白色沉淀,后沉淀由白色变为黄色 | Ksp(AgCl)>Ksp(AgI) |
| B | 在稀硫酸中加入少量Cu2O(s) | 溶液由无色变为蓝色,并有红色固体生成 | 反应中Cu2O既作氧化剂又作还原剂 |
| C | 在灼热木炭中加入浓硫酸,将生成的气体依次通过品红溶液、饱和NaHCO3溶液、澄清石灰水 | 品红溶液褪色,澄清石灰水变浑浊 | 浓硫酸和木炭反应产生SO2和CO2气体 |
| D | 向CuSO4溶液中滴加浓氨水至过量 | 先生成蓝色沉淀,后逐渐溶解 | Cu(OH)2是两性氢氧化物 |
A. | B. | C. | D. |
您最近一年使用:0次
名校
2 . 某种抗结核候选药物的重要中间体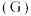 可通过如下过程制得。下列有关说法正确的是
可通过如下过程制得。下列有关说法正确的是
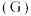 可通过如下过程制得。下列有关说法正确的是
可通过如下过程制得。下列有关说法正确的是
A. 中含有两个手性碳原子 中含有两个手性碳原子 |
B. 最多可消耗 最多可消耗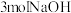 |
C. 与 与 互为同系物 互为同系物 |
D.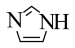 可消耗反应生成的酸,提高反应转化率 可消耗反应生成的酸,提高反应转化率 |
您最近一年使用:0次
2024-03-19更新
|
171次组卷
|
2卷引用:重庆市云阳盘石中学校2023-2024学年高三上学期12月月考化学试题
名校
3 . 肼 是一种应用广泛的化工原料,可用作火箭和燃料电池的燃料。实验室制取肼的化学方程式为:
是一种应用广泛的化工原料,可用作火箭和燃料电池的燃料。实验室制取肼的化学方程式为: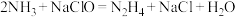 。已知
。已知 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 是一种应用广泛的化工原料,可用作火箭和燃料电池的燃料。实验室制取肼的化学方程式为:
是一种应用广泛的化工原料,可用作火箭和燃料电池的燃料。实验室制取肼的化学方程式为: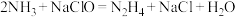 。已知
。已知 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.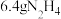 分子中含有的电子数为 分子中含有的电子数为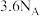 |
B.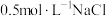 溶液中含有的氯原子数为 溶液中含有的氯原子数为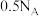 |
C.每消耗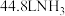 ,理论上转移电子数为 ,理论上转移电子数为 |
D.标准状况下,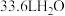 含有水分子数为 含有水分子数为 |
您最近一年使用:0次
2024-03-19更新
|
184次组卷
|
3卷引用:重庆市云阳盘石中学校2023-2024学年高三上学期12月月考化学试题
名校
解题方法
4 . 反应 可用于氯气管道的检测,下列表示反应中相关微粒的化学用语正确的是
可用于氯气管道的检测,下列表示反应中相关微粒的化学用语正确的是
 可用于氯气管道的检测,下列表示反应中相关微粒的化学用语正确的是
可用于氯气管道的检测,下列表示反应中相关微粒的化学用语正确的是A.中子数为18的氯原子: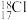 | B. 分子的结构式: 分子的结构式: |
C. 的电子式: 的电子式: | D. 的结构示意图: 的结构示意图: |
您最近一年使用:0次
2024-03-18更新
|
275次组卷
|
4卷引用:重庆市育才中学校2022-2023学年高一下学期3月月考化学试题
5 . 酸碱滴定和氧化还原滴定是常见的两种滴定方法。
I.氧化还原滴定:化学兴趣小组欲准确测定某市售双氧水中 的含量:取双氧水
的含量:取双氧水 至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准液滴定,其反应的离子方程式为
至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准液滴定,其反应的离子方程式为 。
。
(1)滴定时,将高锰酸钾标准溶液注入___________ (填“酸”或“碱”)式滴定管中。
(2)滴定到达终点的现象是___________ 。
(3)根据实验测得,消耗 溶液,那么
溶液,那么 的浓度为
的浓度为___________ 。
Ⅱ.酸碱中和滴定:常温下,用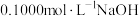 溶液分别滴定
溶液分别滴定 等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:
等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:

(4)滴定盐酸的曲线是图___________ (填“1”或“2”)。
(5)滴定前 的电离度为
的电离度为___________ 。[电离度
 ×100%]
×100%]
(6)达到B、D状态时,反应消耗的 溶液的体积图1
溶液的体积图1___________ (填“>”“<”或“=”)图2;当 时,解释E点为碱性的原因
时,解释E点为碱性的原因___________ 。(离子方程式)
I.氧化还原滴定:化学兴趣小组欲准确测定某市售双氧水中
 的含量:取双氧水
的含量:取双氧水 至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准液滴定,其反应的离子方程式为
至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准液滴定,其反应的离子方程式为 。
。(1)滴定时,将高锰酸钾标准溶液注入
(2)滴定到达终点的现象是
(3)根据实验测得,消耗
 溶液,那么
溶液,那么 的浓度为
的浓度为Ⅱ.酸碱中和滴定:常温下,用
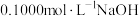 溶液分别滴定
溶液分别滴定 等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:
等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:
(4)滴定盐酸的曲线是图
(5)滴定前
 的电离度为
的电离度为
 ×100%]
×100%](6)达到B、D状态时,反应消耗的
 溶液的体积图1
溶液的体积图1 时,解释E点为碱性的原因
时,解释E点为碱性的原因
您最近一年使用:0次
6 . 盐类水解在实验室和生产生活中有广泛的应用。
I.25℃时, 和
和 两溶液的pH均为11。
两溶液的pH均为11。
(1)两溶液中,由水电离的 分别是:
分别是: 溶液中
溶液中___________ ; 溶液中
溶液中___________ 。
(2)各取 上述两种溶液,分别加水稀释到
上述两种溶液,分别加水稀释到 ,pH变化较大的是
,pH变化较大的是___________ (填化学式)溶液。
(3)为探究纯碱溶液呈碱性是由 引起的,请你设计一个简单的实验方案
引起的,请你设计一个简单的实验方案___________ 。
Ⅱ.现有25℃时 的氨水溶液。
的氨水溶液。
(4)若向氨水中加入稀硫酸,使其恰好完全中和,写出反应的离子方程式:___________ ;所得溶液的pH___________ (填“<”“>”或“=”)7,用离子方程式表示其原因:___________ 。
(5)若向该氨水中加入稀硫酸至溶液的 ,此时
,此时 ,则
,则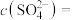
___________  。
。
(6)现有浓度均为 的氢氧化钠和氯化铵溶液,按体积比
的氢氧化钠和氯化铵溶液,按体积比 混合后的溶液
混合后的溶液 中各离子的浓度由大到小的顺序是
中各离子的浓度由大到小的顺序是___________ 。
(7) 的水溶液呈
的水溶液呈___________ (填“酸”“中”或“碱”)性,原因是___________ (用离子方程式表示);实验室在配制 的溶液时,常将
的溶液时,常将 固体先溶于较浓的硝酸中,然后用蒸馏水稀释到所需浓度,目的是
固体先溶于较浓的硝酸中,然后用蒸馏水稀释到所需浓度,目的是___________ 。
(8) 净水的原理是(用离子方程式表示)
净水的原理是(用离子方程式表示)___________ 。
(9)泡沫灭火器内装有 饱和溶液和
饱和溶液和 溶液,当意外失火时,使泡沫灭火器倒过来摇动即可使药液混合,喷出大量的白色泡沫,阻止火势蔓延,其相关的离子方程式为
溶液,当意外失火时,使泡沫灭火器倒过来摇动即可使药液混合,喷出大量的白色泡沫,阻止火势蔓延,其相关的离子方程式为___________ 。
(10)已知草酸是二元弱酸,常温下测得 的
的 的pH为4.8,则
的pH为4.8,则 溶液中
溶液中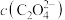
___________  (填>,<或=)。
(填>,<或=)。
I.25℃时,
 和
和 两溶液的pH均为11。
两溶液的pH均为11。(1)两溶液中,由水电离的
 分别是:
分别是: 溶液中
溶液中 溶液中
溶液中(2)各取
 上述两种溶液,分别加水稀释到
上述两种溶液,分别加水稀释到 ,pH变化较大的是
,pH变化较大的是(3)为探究纯碱溶液呈碱性是由
 引起的,请你设计一个简单的实验方案
引起的,请你设计一个简单的实验方案Ⅱ.现有25℃时
 的氨水溶液。
的氨水溶液。(4)若向氨水中加入稀硫酸,使其恰好完全中和,写出反应的离子方程式:
(5)若向该氨水中加入稀硫酸至溶液的
 ,此时
,此时 ,则
,则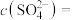
 。
。(6)现有浓度均为
 的氢氧化钠和氯化铵溶液,按体积比
的氢氧化钠和氯化铵溶液,按体积比 混合后的溶液
混合后的溶液 中各离子的浓度由大到小的顺序是
中各离子的浓度由大到小的顺序是(7)
 的水溶液呈
的水溶液呈 的溶液时,常将
的溶液时,常将 固体先溶于较浓的硝酸中,然后用蒸馏水稀释到所需浓度,目的是
固体先溶于较浓的硝酸中,然后用蒸馏水稀释到所需浓度,目的是(8)
 净水的原理是(用离子方程式表示)
净水的原理是(用离子方程式表示)(9)泡沫灭火器内装有
 饱和溶液和
饱和溶液和 溶液,当意外失火时,使泡沫灭火器倒过来摇动即可使药液混合,喷出大量的白色泡沫,阻止火势蔓延,其相关的离子方程式为
溶液,当意外失火时,使泡沫灭火器倒过来摇动即可使药液混合,喷出大量的白色泡沫,阻止火势蔓延,其相关的离子方程式为(10)已知草酸是二元弱酸,常温下测得
 的
的 的pH为4.8,则
的pH为4.8,则 溶液中
溶液中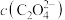
 (填>,<或=)。
(填>,<或=)。
您最近一年使用:0次
7 . 常温下,下列溶液中各组离子可能大量共存的是
A. 的 的 溶液: 溶液: 、 、 、 、 、 、 |
B. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C.在能与Al反应生成 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.由水电离产生的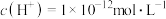 的溶液: 的溶液: 、 、 、 、 、 、 |
您最近一年使用:0次
8 .  为阿伏加德罗常数,下列说法正确的是
为阿伏加德罗常数,下列说法正确的是
 为阿伏加德罗常数,下列说法正确的是
为阿伏加德罗常数,下列说法正确的是A.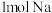 与足量 与足量 反应,生成 反应,生成 和 和 的混合物,钠失去电子数为 的混合物,钠失去电子数为 |
B. 粉与足量S粉加热充分反应转移的电子数为 粉与足量S粉加热充分反应转移的电子数为 |
C. 溶液中含有 溶液中含有 的数目为 的数目为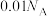 |
D.常温下, 的 的 溶液中,体系中 溶液中,体系中 的数目为 的数目为 |
您最近一年使用:0次
9 . 下列离子方程式书写不正确的是
A.稀硫酸与氢氧化钡溶液混合: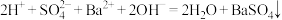 |
B.向碳酸氢钠溶液中加入稀硫酸: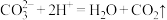 |
C.将一小块钠放入水中: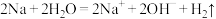 |
D.氧化铁粉末溶于稀盐酸: |
您最近一年使用:0次
10 . 下列说法中正确的是
| A.将硫酸钡放入水中不能导电,所以硫酸钡是非电解质 |
| B.氨气溶于水得到的溶液氨水能导电,所以氨水是电解质 |
C.固态 不导电,熔融的 不导电,熔融的 可以导电 可以导电 |
| D.电解质的水溶液一定能导电,非电解质的水溶液一定不导电 |
您最近一年使用:0次



