名校
1 . 氧化还原反应、离子反应在生产生活中应用广泛。
I.现有 两种溶液,经测定这两种溶液中含有下列10种离子:
两种溶液,经测定这两种溶液中含有下列10种离子: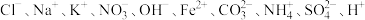 。
。
(1)完成下列表格中实验①的结论和实验②的实验内容以及现象:
(2)已知:酸性环境中, 被
被 氧化,生成
氧化,生成 和
和 气体,请写出对应离子方程式:
气体,请写出对应离子方程式:_______ ;结合(1)可判断出, 存在于
存在于_______ (填“M”或“N”)溶液中。
(3)根据(1)和(2)可以确定,M溶液中含有的离子为______________ 。
Ⅱ.氮氧化物 储存还原的工作原理
储存还原的工作原理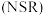 如下图所示,柴油发动机工作时在稀燃(
如下图所示,柴油发动机工作时在稀燃( 充足、柴油较少)和富燃(
充足、柴油较少)和富燃( 不足、柴油较多)条件下交替进行,通过
不足、柴油较多)条件下交替进行,通过 和
和 的相互转化实现
的相互转化实现 的储存和还原。
的储存和还原。 吸收
吸收 的反应中氧化剂与还原剂的粒子个数之比为
的反应中氧化剂与还原剂的粒子个数之比为_______ 。
(5)富燃条件下 表面反应的化学方程式是
表面反应的化学方程式是______________ 。
(6)若柴油中硫含量较高,在稀燃过程中, 吸收氮氧化物的能力下降至很低水平,用化学方程式解释其原因
吸收氮氧化物的能力下降至很低水平,用化学方程式解释其原因______________ 。
(7)研究 对
对 吸收氮氧化物的影响。一定温度下测得气体中
吸收氮氧化物的影响。一定温度下测得气体中 的体积分数与氮氧化物吸收率的关系如图所示。下列分析中正确的是
的体积分数与氮氧化物吸收率的关系如图所示。下列分析中正确的是_______ (填字母序号)。 体积分数的增大而下降,原因可能是
体积分数的增大而下降,原因可能是 与
与 反应生成
反应生成 ,覆盖在
,覆盖在 表面
表面
B.当 体积分数达到
体积分数达到 时,氮氧化物吸收率依然较高,其原因可能是
时,氮氧化物吸收率依然较高,其原因可能是 在一定程度上也能吸收
在一定程度上也能吸收
C.以上分析均不对
I.现有
 两种溶液,经测定这两种溶液中含有下列10种离子:
两种溶液,经测定这两种溶液中含有下列10种离子: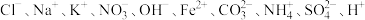 。
。(1)完成下列表格中实验①的结论和实验②的实验内容以及现象:
实验内容以及现象 | 结论 |
①取少量N溶液滴加足量的硝酸钡溶液,无沉淀产生 | |
② | 确定M溶液中含有 |
③取M溶液少量加酚酞试液,溶液变红 |
(2)已知:酸性环境中,
 被
被 氧化,生成
氧化,生成 和
和 气体,请写出对应离子方程式:
气体,请写出对应离子方程式: 存在于
存在于(3)根据(1)和(2)可以确定,M溶液中含有的离子为
Ⅱ.氮氧化物
 储存还原的工作原理
储存还原的工作原理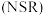 如下图所示,柴油发动机工作时在稀燃(
如下图所示,柴油发动机工作时在稀燃( 充足、柴油较少)和富燃(
充足、柴油较少)和富燃( 不足、柴油较多)条件下交替进行,通过
不足、柴油较多)条件下交替进行,通过 和
和 的相互转化实现
的相互转化实现 的储存和还原。
的储存和还原。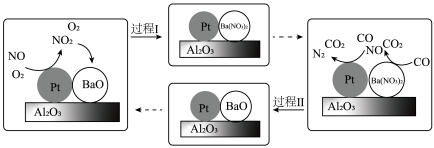
 吸收
吸收 的反应中氧化剂与还原剂的粒子个数之比为
的反应中氧化剂与还原剂的粒子个数之比为(5)富燃条件下
 表面反应的化学方程式是
表面反应的化学方程式是(6)若柴油中硫含量较高,在稀燃过程中,
 吸收氮氧化物的能力下降至很低水平,用化学方程式解释其原因
吸收氮氧化物的能力下降至很低水平,用化学方程式解释其原因(7)研究
 对
对 吸收氮氧化物的影响。一定温度下测得气体中
吸收氮氧化物的影响。一定温度下测得气体中 的体积分数与氮氧化物吸收率的关系如图所示。下列分析中正确的是
的体积分数与氮氧化物吸收率的关系如图所示。下列分析中正确的是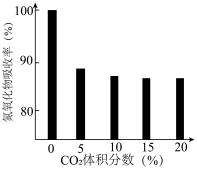
 体积分数的增大而下降,原因可能是
体积分数的增大而下降,原因可能是 与
与 反应生成
反应生成 ,覆盖在
,覆盖在 表面
表面B.当
 体积分数达到
体积分数达到 时,氮氧化物吸收率依然较高,其原因可能是
时,氮氧化物吸收率依然较高,其原因可能是 在一定程度上也能吸收
在一定程度上也能吸收
C.以上分析均不对
您最近一年使用:0次
名校
2 . 侯德榜先生对索尔维制碱法进行了改进,将氨碱法和合成氨联合起来,这就是联合制碱法,也称侯氏制碱法。
Ⅰ、侯氏制碱法的生产流程如下图所示:_______ ,产品Z的化学式为_______ ,操作1的名称是_______ 。
(2)该法通入 的反应原理是
的反应原理是_______ (用化学方程式表示)。
Ⅱ、制得的碳酸钠样品中往往含有少量的 ,某探究性学习小组设计如下图所示装置,测定该样品中
,某探究性学习小组设计如下图所示装置,测定该样品中 的质量分数。
的质量分数。
①检查装置的气密性 ②取 样品装入广口瓶中 ③打开止水夹 ④缓慢鼓入空气数分钟 ⑤关闭止水夹 ⑥在干燥管内装满碱石灰,称量其质量为
样品装入广口瓶中 ③打开止水夹 ④缓慢鼓入空气数分钟 ⑤关闭止水夹 ⑥在干燥管内装满碱石灰,称量其质量为 ⑦缓慢加入稀硫酸至不再产生气体为止 ⑧打开止水夹
⑦缓慢加入稀硫酸至不再产生气体为止 ⑧打开止水夹
⑨缓慢鼓入空气数分钟,再称量干燥管质量为
(3)装置A的作用是_______ ;操作④中,鼓入空气的作用是_______ 。
(4)如果将步骤⑥提前到与步骤②一同进行,会导致测定结果_______ (填“偏大”、“偏小”或“不变”)。
(5)根据实验数据列出样品中 的质量分数表达式
的质量分数表达式_______ 。
Ⅰ、侯氏制碱法的生产流程如下图所示:
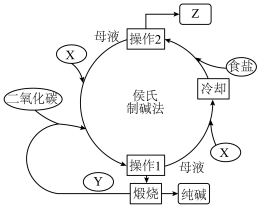
(2)该法通入
 的反应原理是
的反应原理是Ⅱ、制得的碳酸钠样品中往往含有少量的
 ,某探究性学习小组设计如下图所示装置,测定该样品中
,某探究性学习小组设计如下图所示装置,测定该样品中 的质量分数。
的质量分数。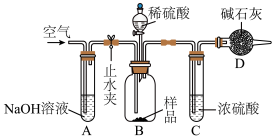
①检查装置的气密性 ②取
 样品装入广口瓶中 ③打开止水夹 ④缓慢鼓入空气数分钟 ⑤关闭止水夹 ⑥在干燥管内装满碱石灰,称量其质量为
样品装入广口瓶中 ③打开止水夹 ④缓慢鼓入空气数分钟 ⑤关闭止水夹 ⑥在干燥管内装满碱石灰,称量其质量为 ⑦缓慢加入稀硫酸至不再产生气体为止 ⑧打开止水夹
⑦缓慢加入稀硫酸至不再产生气体为止 ⑧打开止水夹⑨缓慢鼓入空气数分钟,再称量干燥管质量为

(3)装置A的作用是
(4)如果将步骤⑥提前到与步骤②一同进行,会导致测定结果
(5)根据实验数据列出样品中
 的质量分数表达式
的质量分数表达式
您最近一年使用:0次
3 . 饮用水质量是关系人类健康的重要问题。
(1) 是一种广谱型的消毒剂,将逐渐取代
是一种广谱型的消毒剂,将逐渐取代 成为生产自来水的消毒剂。工业上
成为生产自来水的消毒剂。工业上 常用
常用 和
和 溶液混合并加
溶液混合并加 酸化后反应制得,反应中氧化剂和还原剂的个数比为
酸化后反应制得,反应中氧化剂和还原剂的个数比为_______ 。
(2)高铁酸盐是一种新型、高效、多功能绿色水处理剂。
①干法制备高铁酸钠 的主要反应为:
的主要反应为: ,该反应中
,该反应中 是
是_______ (填“氧化剂”或“还原剂”);请写出 与
与 反应的化学方程式
反应的化学方程式____________ 。
②湿法制备高铁酸钾 的反应体系中有六种微粒:
的反应体系中有六种微粒: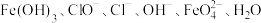 ,写出并配平在碱性条件下湿法制备高铁酸钾反应的离子方程式
,写出并配平在碱性条件下湿法制备高铁酸钾反应的离子方程式______________ 。
(3)实验室可向 溶液中通入
溶液中通入 模拟制备苏打水,若该反应中生成等个数的
模拟制备苏打水,若该反应中生成等个数的 和
和 ,写出其离子方程式
,写出其离子方程式______________ 。
(1)
 是一种广谱型的消毒剂,将逐渐取代
是一种广谱型的消毒剂,将逐渐取代 成为生产自来水的消毒剂。工业上
成为生产自来水的消毒剂。工业上 常用
常用 和
和 溶液混合并加
溶液混合并加 酸化后反应制得,反应中氧化剂和还原剂的个数比为
酸化后反应制得,反应中氧化剂和还原剂的个数比为(2)高铁酸盐是一种新型、高效、多功能绿色水处理剂。
①干法制备高铁酸钠
 的主要反应为:
的主要反应为: ,该反应中
,该反应中 是
是 与
与 反应的化学方程式
反应的化学方程式②湿法制备高铁酸钾
 的反应体系中有六种微粒:
的反应体系中有六种微粒: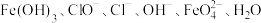 ,写出并配平在碱性条件下湿法制备高铁酸钾反应的离子方程式
,写出并配平在碱性条件下湿法制备高铁酸钾反应的离子方程式(3)实验室可向
 溶液中通入
溶液中通入 模拟制备苏打水,若该反应中生成等个数的
模拟制备苏打水,若该反应中生成等个数的 和
和 ,写出其离子方程式
,写出其离子方程式
您最近一年使用:0次
名校
解题方法
4 . I.按要求完成下列填空:
(1)盐酸和小苏打反应的离子方程式____________ 。
(2)向硫酸氢钠溶液中逐滴加入氢氧化钡溶液,溶液恰好显中性时反应的离子方程式____________ 。
(3)配平下列方程式,并用双线桥表示电子转移的方向与数目____________ :
 。
。
Ⅱ.过氧化氢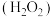 的水溶液,俗称双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列
的水溶液,俗称双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列 涉及
涉及 的反应,回答相关问题:
的反应,回答相关问题:
A.
B.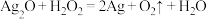
C.
D.
(4) 仅体现还原性的反应是
仅体现还原性的反应是_______ 。(填字母代号)
(5)上述反应说明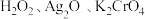 氧化性由强到弱的顺序是
氧化性由强到弱的顺序是_______ 。
(6)在稀硫酸中, 和
和 能发生氧化还原反应。已知该反应中
能发生氧化还原反应。已知该反应中 只发生过程:
只发生过程: ,写出该反应的离子方程式
,写出该反应的离子方程式______________ 。
(1)盐酸和小苏打反应的离子方程式
(2)向硫酸氢钠溶液中逐滴加入氢氧化钡溶液,溶液恰好显中性时反应的离子方程式
(3)配平下列方程式,并用双线桥表示电子转移的方向与数目
 。
。Ⅱ.过氧化氢
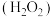 的水溶液,俗称双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列
的水溶液,俗称双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列 涉及
涉及 的反应,回答相关问题:
的反应,回答相关问题:A.

B.
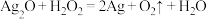
C.

D.

(4)
 仅体现还原性的反应是
仅体现还原性的反应是(5)上述反应说明
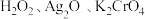 氧化性由强到弱的顺序是
氧化性由强到弱的顺序是(6)在稀硫酸中,
 和
和 能发生氧化还原反应。已知该反应中
能发生氧化还原反应。已知该反应中 只发生过程:
只发生过程: ,写出该反应的离子方程式
,写出该反应的离子方程式
您最近一年使用:0次
名校
5 . 现有八种物质:① ;②熔融
;②熔融 ;③
;③ ;④乙醇;⑤液态氯化氢;⑥澄清石灰水;⑦
;④乙醇;⑤液态氯化氢;⑥澄清石灰水;⑦ ;⑧
;⑧ ,回答下列问题:
,回答下列问题:
(1)上述物质中属于电解质的是_______ (填序号,下同),属于非电解质的是_______ ,属于盐的是_______ 。
(2)写出物质③溶于水的电离方程式____________ ;写出⑧加入③的水溶液中发生反应的离子方程式____________ 。
(3)写出过量⑦通入⑥中发生反应的离子方程式____________ 。
 ;②熔融
;②熔融 ;③
;③ ;④乙醇;⑤液态氯化氢;⑥澄清石灰水;⑦
;④乙醇;⑤液态氯化氢;⑥澄清石灰水;⑦ ;⑧
;⑧ ,回答下列问题:
,回答下列问题:(1)上述物质中属于电解质的是
(2)写出物质③溶于水的电离方程式
(3)写出过量⑦通入⑥中发生反应的离子方程式
您最近一年使用:0次
名校
解题方法
6 . 纳米铁粉具有较强的还原性和吸附性,能被水体中的 氧化。利用纳米铁粉除去水体中六价铬
氧化。利用纳米铁粉除去水体中六价铬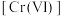 的反应机理如图所示:
的反应机理如图所示:
 氧化。利用纳米铁粉除去水体中六价铬
氧化。利用纳米铁粉除去水体中六价铬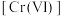 的反应机理如图所示:
的反应机理如图所示: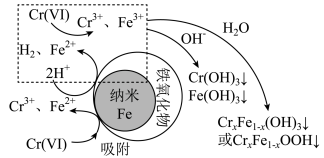
A.机理中生成 反应的离子方程式为: 反应的离子方程式为: |
B. 元素参与的反应均存在电子转移 元素参与的反应均存在电子转移 |
C.纳米铁粉除去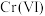 的机理主要包括吸附、还原和共沉淀 的机理主要包括吸附、还原和共沉淀 |
D.铁粉处理成纳米铁粉有利于提高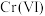 的处理效率 的处理效率 |
您最近一年使用:0次
7 . 《本草纲目》记载了利尿剂甘汞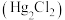 的制法:“用水银一两,白矾
的制法:“用水银一两,白矾 二两,食盐一两,同研不见星,铺于铁器内,以小乌盆覆之,筛灶灰,盐水和,封固盆口,以炭打二炷香取开,则粉升于盆上矣,其白如雪,轻盈可爱,一两汞,可升粉八钱。”下列叙述错误的是
二两,食盐一两,同研不见星,铺于铁器内,以小乌盆覆之,筛灶灰,盐水和,封固盆口,以炭打二炷香取开,则粉升于盆上矣,其白如雪,轻盈可爱,一两汞,可升粉八钱。”下列叙述错误的是
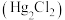 的制法:“用水银一两,白矾
的制法:“用水银一两,白矾 二两,食盐一两,同研不见星,铺于铁器内,以小乌盆覆之,筛灶灰,盐水和,封固盆口,以炭打二炷香取开,则粉升于盆上矣,其白如雪,轻盈可爱,一两汞,可升粉八钱。”下列叙述错误的是
二两,食盐一两,同研不见星,铺于铁器内,以小乌盆覆之,筛灶灰,盐水和,封固盆口,以炭打二炷香取开,则粉升于盆上矣,其白如雪,轻盈可爱,一两汞,可升粉八钱。”下列叙述错误的是| A.上述制法中,利用了甘汞容易升华的性质 |
B.甘汞中汞的化合价为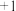 |
C.制备甘汞的反应中,氧化剂与还原剂的个数之比为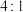 |
D.若题中1两等于10钱,则甘汞的产率约为 |
您最近一年使用:0次
名校
解题方法
8 . 某无色溶液中只含有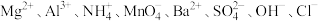 中的几种,向溶液中滴加酚酞,溶液变红,下列说法正确的是
中的几种,向溶液中滴加酚酞,溶液变红,下列说法正确的是
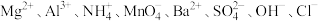 中的几种,向溶液中滴加酚酞,溶液变红,下列说法正确的是
中的几种,向溶液中滴加酚酞,溶液变红,下列说法正确的是A.一定存在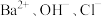 | B.一定存在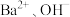 ,可能存在 ,可能存在 |
C.可能存在 | D.一定不存在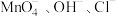 |
您最近一年使用:0次
名校
9 . 下列关于钠的化合物的说法中,正确的是
A.除去 固体中含有的 固体中含有的 ,可将固体混合物加热至恒重 ,可将固体混合物加热至恒重 |
B.除去 溶液中含有的 溶液中含有的 ,可加入适量 ,可加入适量 溶液,过滤 溶液,过滤 |
C.分别向 和 和 与水反应后的溶液立即滴入酚酞,两者现象相同 与水反应后的溶液立即滴入酚酞,两者现象相同 |
D.等质量 和 和 分别与足量盐酸反应,前者产生的 分别与足量盐酸反应,前者产生的 更多 更多 |
您最近一年使用:0次
名校
10 .  是精细磷化工产品,其工业制备原理如下:
是精细磷化工产品,其工业制备原理如下:
反应I:
反应Ⅱ: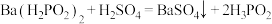 下列说法正确的是
下列说法正确的是
 是精细磷化工产品,其工业制备原理如下:
是精细磷化工产品,其工业制备原理如下:反应I:

反应Ⅱ:
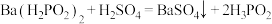 下列说法正确的是
下列说法正确的是| A.反应I、Ⅱ均属于氧化还原反应 |
B. 具有氧化性,在空气中可能被还原成磷酸 具有氧化性,在空气中可能被还原成磷酸 |
C.在反应I中氧化剂与还原剂的质量之比为 |
D.反应I中每生成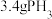 ,消耗 ,消耗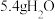 |
您最近一年使用:0次

 ,不含
,不含


