1 .  (四羰合镍,沸点43℃)可用于制备高纯镍,也是有机化合物羰基化反应的催化剂。回答下列问题:
(四羰合镍,沸点43℃)可用于制备高纯镍,也是有机化合物羰基化反应的催化剂。回答下列问题:
(1)Ni基态原子价电子的轨道表示式为_______ 。镍的晶胞结构类型与铜的相同,晶胞体积为 ,镍原子半径为
,镍原子半径为_______ 。
(2) 结构如图甲所示,其中含有σ键的数目为
结构如图甲所示,其中含有σ键的数目为_______ , 晶体的类型为
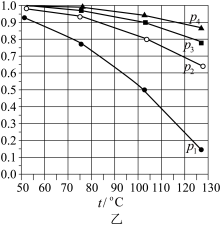
晶体的类型为_______ 。 体积分数x与温度的关系如图乙所示。反应
体积分数x与温度的关系如图乙所示。反应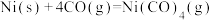 的ΔH
的ΔH_______ 0(填“大于”或“小于”)。从热力学角度考虑,_______ 有利于 的生成(写出两点)。
的生成(写出两点)。 、100℃时CO的平衡转化率α=
、100℃时CO的平衡转化率α=_______ ,该温度下平衡常数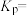
_______  。
。 ,20℃时反应物浓度随时间的变化关系为
,20℃时反应物浓度随时间的变化关系为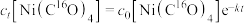 (k为反应速率常数),则
(k为反应速率常数),则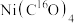 反应一半所需时间
反应一半所需时间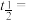
_______ (用k表示)。
 (四羰合镍,沸点43℃)可用于制备高纯镍,也是有机化合物羰基化反应的催化剂。回答下列问题:
(四羰合镍,沸点43℃)可用于制备高纯镍,也是有机化合物羰基化反应的催化剂。回答下列问题:(1)Ni基态原子价电子的轨道表示式为
 ,镍原子半径为
,镍原子半径为(2)
 结构如图甲所示,其中含有σ键的数目为
结构如图甲所示,其中含有σ键的数目为 晶体的类型为
晶体的类型为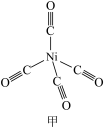
 体积分数x与温度的关系如图乙所示。反应
体积分数x与温度的关系如图乙所示。反应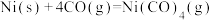 的ΔH
的ΔH 的生成(写出两点)。
的生成(写出两点)。 、100℃时CO的平衡转化率α=
、100℃时CO的平衡转化率α=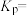
 。
。
 ,20℃时反应物浓度随时间的变化关系为
,20℃时反应物浓度随时间的变化关系为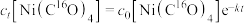 (k为反应速率常数),则
(k为反应速率常数),则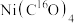 反应一半所需时间
反应一半所需时间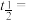
您最近一年使用:0次
真题
解题方法
2 . 钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等方面有着广泛应用。一种从湿法炼锌产生的废渣(主要含Co、Zn、Pb、Fe的单质或氧化物)中富集回收得到含锰高钴成品的工艺如下: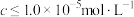 )时的pH:
)时的pH:
回答下列问题:
(1)“酸浸”前废渣需粉碎处理,目的是_______ ;“滤渣1”中金属元素主要为_______ 。
(2)“过滤1”后的溶液中加入 的作用是
的作用是_______ 。取少量反应后的溶液,加入化学试剂_______ 检验_______ ,若出现蓝色沉淀,需补加 。
。
(3)“氧化沉钴”中氧化还原反应的离子方程式为_______ 、_______ 。
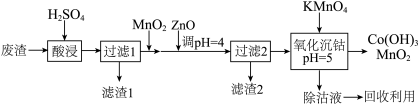
(4)“除钴液”中主要的盐有_______ (写化学式),残留的 浓度为
浓度为_______  。
。
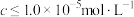 )时的pH:
)时的pH: |  | 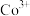 |  |  | |
| 开始沉淀的pH | 1.5 | 6.9 | — | 7.4 | 6.2 |
| 沉淀完全的pH | 2.8 | 8.4 | 1.1 | 9.4 | 8.2 |
(1)“酸浸”前废渣需粉碎处理,目的是
(2)“过滤1”后的溶液中加入
 的作用是
的作用是 。
。(3)“氧化沉钴”中氧化还原反应的离子方程式为
(4)“除钴液”中主要的盐有
 浓度为
浓度为 。
。
您最近一年使用:0次
解题方法
3 . 下列有关实验的离子方程式正确的是
A.将少量 加入蒸馏水中: 加入蒸馏水中: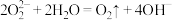 |
B.将铁粉加入足量稀硫酸中: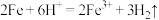 |
C.将 加入过量氢碘酸中: 加入过量氢碘酸中: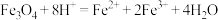 |
D.将少量 溶液加入 溶液加入 溶液中: 溶液中: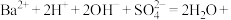 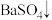 |
您最近一年使用:0次
名校
解题方法
4 . 电解质在水溶液中的反应属于离子反应。下列离子方程式正确的是
A.浓盐酸与 反应制取少量氯气: 反应制取少量氯气: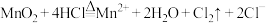 |
B. 溶液中加入过量的 溶液中加入过量的 溶液: 溶液: |
C.1L0.1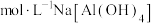 溶液中通入0.28molHCl气体: 溶液中通入0.28molHCl气体: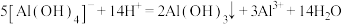 |
D. 通入 通入 溶液中至 溶液中至 恰好完全反应: 恰好完全反应: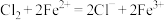 |
您最近一年使用:0次
名校
5 . 一种能捕获和释放 的电化学装置如下图所示。其中a、b均为惰性电极,电解质溶液均为KCl溶液。当K连接
的电化学装置如下图所示。其中a、b均为惰性电极,电解质溶液均为KCl溶液。当K连接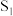 时,b极区溶液能捕获通入的
时,b极区溶液能捕获通入的 。
。
 的电化学装置如下图所示。其中a、b均为惰性电极,电解质溶液均为KCl溶液。当K连接
的电化学装置如下图所示。其中a、b均为惰性电极,电解质溶液均为KCl溶液。当K连接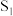 时,b极区溶液能捕获通入的
时,b极区溶液能捕获通入的 。
。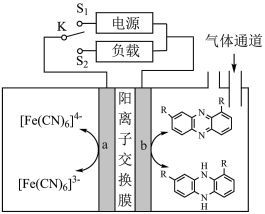
A.K连接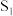 时,b极发生反应: 时,b极发生反应: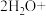 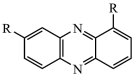  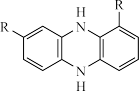 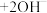 |
B.K连接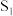 时,a连接电源的负极 时,a连接电源的负极 |
C.K连接 时,a极区 时,a极区 的值增大 的值增大 |
D.该装置通过“充电”和“放电”调控b极区溶液pH,捕获和释放 |
您最近一年使用:0次
7日内更新
|
57次组卷
|
2卷引用:山东省实验中学2024届高三下学期学业水平等级考试(模拟)化学试题
真题
解题方法
6 . 吡咯类化合物在导电聚合物、化学传感器及药物制剂上有着广泛应用。一种合成1-(4-甲氧基苯基)-2,5-二甲基吡咯(用吡咯X表示)的反应和方法如下: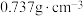 )与100 mmol 4-甲氧基苯胺(熔点:57℃)放入①中,搅拌。
)与100 mmol 4-甲氧基苯胺(熔点:57℃)放入①中,搅拌。
回答下列问题:
(1)量取己-2,5-二酮应使用的仪器为_______ (填名称)。
(2)仪器①用铁夹固定在③上,③的名称是_______ ;仪器②的名称是_______ 。
(3)“搅拌”的作用是_______ 。
(4)“加热”方式为_______ 。
(5)使用的“脱色剂”是_______ 。
(6)“趁热过滤”的目的是_______ ;用_______ 洗涤白色固体。
(7)若需进一步提纯产品,可采用的方法是_______ 。
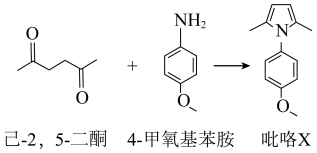
 )与100 mmol 4-甲氧基苯胺(熔点:57℃)放入①中,搅拌。
)与100 mmol 4-甲氧基苯胺(熔点:57℃)放入①中,搅拌。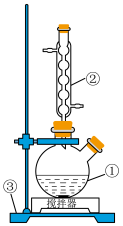
回答下列问题:
(1)量取己-2,5-二酮应使用的仪器为
(2)仪器①用铁夹固定在③上,③的名称是
(3)“搅拌”的作用是
(4)“加热”方式为
(5)使用的“脱色剂”是
(6)“趁热过滤”的目的是
(7)若需进一步提纯产品,可采用的方法是
您最近一年使用:0次
7 . 二氧化氯(ClO2)是一种高效、安全的杀菌消毒剂。一种制备ClO2的工艺流程及ClO2的分子结构(O-Cl-O的键角为117.6°)如图所示。
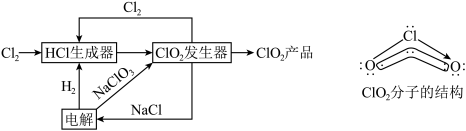
| A.等物质的量ClO2的消毒效率为Cl2的2.5倍 |
B. ClO2分子中含有大π键( ),Cl原子杂化方式为sp2杂化 ),Cl原子杂化方式为sp2杂化 |
C.“ClO2发生器”中发生的反应为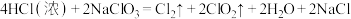 |
| D.“电解”时,阳极与阴极产物的物质的量之比为3∶1 |
您最近一年使用:0次
解题方法
8 . 钛(Ti)和钛合金被广泛应用于火箭、导弹、航天飞机等领域。工业上以钛铁矿(FeTiO3,其中Ti为+4价)为主要原料制备金属钛的工艺流程如下图所示:
下列说法错误 的是

下列说法
| A.步骤①的反应过程元素的化合价没有发生变化 |
| B.步骤③的操作名称是加热或高温煅烧 |
C.步骤④的反应方程式TiO2+2C+2Cl2 TiCl4+2CO TiCl4+2CO |
| D.由TiCl4制备Ti的过程中,可以加入氮气做保护气体 |
您最近一年使用:0次
7日内更新
|
245次组卷
|
3卷引用:湖南省部分校联考2024届高三下学期5月模拟考试化学试题
湖南省部分校联考2024届高三下学期5月模拟考试化学试题福建省部分优质高中2023-2024 学年高一第二学期期末模拟考试化学试卷(已下线)第05讲 氧化还原反应方程式的配平、书写及计算(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
9 . 一种利用含钴废料(主要成分为 ,还含有少量
,还含有少量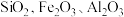 等杂质)制备
等杂质)制备 的工艺流程如下。
的工艺流程如下。 如下表:
如下表:
② 的
的 的
的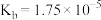 。
。
下列说法不正确的是
 ,还含有少量
,还含有少量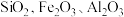 等杂质)制备
等杂质)制备 的工艺流程如下。
的工艺流程如下。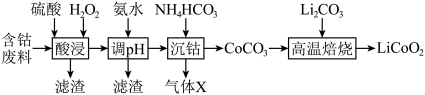
 如下表:
如下表:| 金属离子 |  |  |  |  |
开始沉淀的 | 8.5 | 2.2 | 3.4 | 7.8 |
完全沉淀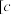 (金属离子) (金属离子)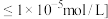 的的 的的 | 10.0 | 3.0 | 4.5 | 9.4 |
 的
的 的
的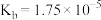 。
。下列说法不正确的是
A.由流程可知氧化性: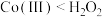 |
B.常温下加入的 溶液显碱性 溶液显碱性 |
C.气体 通入氨水至过量后所得溶液可循环利用 通入氨水至过量后所得溶液可循环利用 |
D.“高温焙烧”时的化学方程式: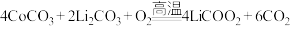 |
您最近一年使用:0次
名校
解题方法
10 . 用高分子吸附树脂提取卤水中的碘(主要以 形式存在)的工艺流程如下:
形式存在)的工艺流程如下:
 形式存在)的工艺流程如下:
形式存在)的工艺流程如下: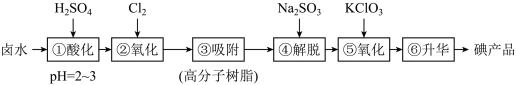
A.经①和④所得溶液中,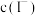 后者小于前者 后者小于前者 |
| B.④的作用是将吸附的碘还原而脱离高分子树脂 |
C.若②和⑤中分别得到等量 ,则消耗的 ,则消耗的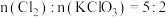 |
| D.由⑥能得到碘产品是因为碘分子为极性分子,与溶液中的其他微粒间的作用力较弱 |
您最近一年使用:0次
7日内更新
|
62次组卷
|
3卷引用:北京市海淀区第一零一中学2023-2024学年高三下学期三模化学试题
北京市海淀区第一零一中学2023-2024学年高三下学期三模化学试题 北京市第一○一中学2023-2024学年高三下学期三模化学 试题(已下线)第05讲 氧化还原反应方程式的配平、书写及计算(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)



