名校
1 . 下列实验方案、现象和结论都正确的是:
| 实验目的 | 实验方案 | 现象和结论 | |
| A | 探究乙醇消去反应的 产物 | C2H5OH与浓硫酸(体积比约为 1 : 3)的混合液,放入几块碎瓷片, 170°C共热,将产生的气体通入酸性 KMnO4溶液中 | 若酸性KMnO4溶液褪色,则乙醇消去反应的产物为乙烯 |
| B | 探究乙酰水杨酸(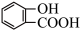 )样品中是否含有水杨酸 )样品中是否含有水杨酸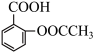 | 取少量样品,加入3mL蒸馏水和少量乙醇,振荡,再加入1-2滴FeCl3 溶液 | 若有紫色沉淀生成,则该样品中含有水杨酸 |
| C | 探究麦芽糖是否发生水解 | 取2mL20%的麦芽糖溶液于试管中,加入适量稀h2so4后水浴加热5min,冷却后加入适量新制Cu(OH)2悬浊液并加热煮沸 | 若没有砖红色沉淀生成,则麦芽糖没有水解 |
| D | 探究KI与FeCl3反应的限度 | 取5 mL 0.1 mol KI溶液于试管中,加入1 mL 0. 1 mol • L-1 FeCl3溶液,充分反应后滴入5滴15% KSCN溶液 | 若溶液变血红色,则 KI与FeCl3的反应有一定限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 已知木炭还原氧化铜实验中发生的主要反应:C+2CuO 2Cu+CO2↑,化学兴趣小组对该实验产物(假设反应物已完全反应)作如图探究:
2Cu+CO2↑,化学兴趣小组对该实验产物(假设反应物已完全反应)作如图探究:

探究一:检验产物的成分
提出问题:实验产物是暗红色固体,很难观察到紫红色固体。暗红色固体是什么?
查阅资料:氧化亚铜(Cu2O)为红色固体:Cu2O+H2SO4=CuSO4+Cu+H2O。
猜想与假设:暗红色固体除铜外还可能含有Cu2O。
(1)取少量暗红色固体,加入稀硫酸,如果观察到现象:____ ,说明暗红色固体含有Cu2O。用氢氧化钠可检验生成物中有Cu2+,该反应的方程式是____ 。
探究二:测定产物中Cu2O的含量
原理C+2CuO 2Cu+CO2↑,称取一定质量的固体样品,用如图装置进行实验(固定装置略去,碱石灰为氧化钙和氢氧化钠的混合物),通过测定反应前后装置d的质量达到实验目的。
2Cu+CO2↑,称取一定质量的固体样品,用如图装置进行实验(固定装置略去,碱石灰为氧化钙和氢氧化钠的混合物),通过测定反应前后装置d的质量达到实验目的。
(2)装置e的作用是____ ,若不加装置e,实验结果会偏____ (填“大”或“小”)。
(3)点燃酒精灯前涉及的部分操作如下,正确的顺序是____ 。
①打开K2:关闭K1②检查装置的气密性 ③连接仪器 ④关闭K2,打开K1,通氢气一段时间
(4)还可通过测定反应前后装置____ (填“a”、“b”或“c”)的质量达到实验目的。
 2Cu+CO2↑,化学兴趣小组对该实验产物(假设反应物已完全反应)作如图探究:
2Cu+CO2↑,化学兴趣小组对该实验产物(假设反应物已完全反应)作如图探究:
探究一:检验产物的成分
提出问题:实验产物是暗红色固体,很难观察到紫红色固体。暗红色固体是什么?
查阅资料:氧化亚铜(Cu2O)为红色固体:Cu2O+H2SO4=CuSO4+Cu+H2O。
猜想与假设:暗红色固体除铜外还可能含有Cu2O。
(1)取少量暗红色固体,加入稀硫酸,如果观察到现象:
探究二:测定产物中Cu2O的含量
原理C+2CuO
 2Cu+CO2↑,称取一定质量的固体样品,用如图装置进行实验(固定装置略去,碱石灰为氧化钙和氢氧化钠的混合物),通过测定反应前后装置d的质量达到实验目的。
2Cu+CO2↑,称取一定质量的固体样品,用如图装置进行实验(固定装置略去,碱石灰为氧化钙和氢氧化钠的混合物),通过测定反应前后装置d的质量达到实验目的。(2)装置e的作用是
(3)点燃酒精灯前涉及的部分操作如下,正确的顺序是
①打开K2:关闭K1②检查装置的气密性 ③连接仪器 ④关闭K2,打开K1,通氢气一段时间
(4)还可通过测定反应前后装置
您最近一年使用:0次
名校
3 . 㵘同学根据Mg与 反应的原理推测Na也能在
反应的原理推测Na也能在 中燃烧,为了确定其产物,在春老师的指导下他设计了如图所示装置进行实验。已知
中燃烧,为了确定其产物,在春老师的指导下他设计了如图所示装置进行实验。已知 能被CO还原得到黑色的金属Pd。请回答下列问题:
能被CO还原得到黑色的金属Pd。请回答下列问题:
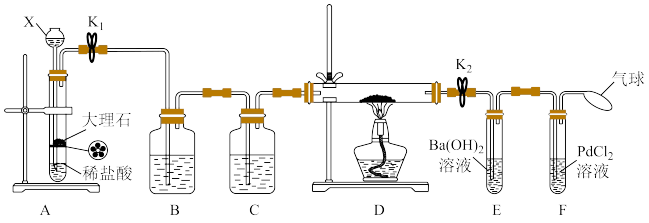
(1)仪器X的名称是___________ 。
(2)装置B中的试剂是___________ ,作用是___________ 。
(3)先称量硬质玻璃管的质量为 ,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是
,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是 。再按如下顺序进行实验操作。
。再按如下顺序进行实验操作。
①打开 和
和 ,通入
,通入 待E中出现
待E中出现___________ 时,再点燃酒,此操作的目的是___________ ;②熄灭酒精灯;③冷却到室温;④关闭 和
和 ;⑤称量硬质玻璃管。重复上述操作步骤,直至硬质玻璃管恒重,称得质量为
;⑤称量硬质玻璃管。重复上述操作步骤,直至硬质玻璃管恒重,称得质量为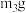 。
。
(4)加热D装置中硬质玻璃管一段时间,观察到以下现象:
①钠块表面变黑,熔融成金属小球;
②继续加热,钠燃烧产生黄色火焰,硬质玻璃管中有大量黑色和白色固体产生。
③F中试管内壁有黑色沉淀产生。
产生上述现象②中黑色固体的原因是___________ 。
(5)探究硬质玻璃管中固体产物中钠元素的存在形式:
假设一:白色固体是 ;假设二:白色固体是
;假设二:白色固体是 ;假设三:白色固体是
;假设三:白色固体是 和
和 的混合物。请完成下列实验设计,验证上述假设:
的混合物。请完成下列实验设计,验证上述假设:
步骤1:将硬质玻璃管中的固体产物溶于水后,过滤;
步骤2:往步骤1所得滤液中加入足量的___________ 溶液产生白色沉淀,过滤;
步骤3:往步骤2所得滤液中滴加几滴酚酞试液,滤液不变红色。
结论:假设一成立。
(6)根据上述实验现象及表格中的实验数据,写出Na与 反应的总化学方程式:
反应的总化学方程式:___________ 。
 反应的原理推测Na也能在
反应的原理推测Na也能在 中燃烧,为了确定其产物,在春老师的指导下他设计了如图所示装置进行实验。已知
中燃烧,为了确定其产物,在春老师的指导下他设计了如图所示装置进行实验。已知 能被CO还原得到黑色的金属Pd。请回答下列问题:
能被CO还原得到黑色的金属Pd。请回答下列问题:
(1)仪器X的名称是
(2)装置B中的试剂是
(3)先称量硬质玻璃管的质量为
 ,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是
,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是 。再按如下顺序进行实验操作。
。再按如下顺序进行实验操作。①打开
 和
和 ,通入
,通入 待E中出现
待E中出现 和
和 ;⑤称量硬质玻璃管。重复上述操作步骤,直至硬质玻璃管恒重,称得质量为
;⑤称量硬质玻璃管。重复上述操作步骤,直至硬质玻璃管恒重,称得质量为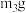 。
。(4)加热D装置中硬质玻璃管一段时间,观察到以下现象:
①钠块表面变黑,熔融成金属小球;
②继续加热,钠燃烧产生黄色火焰,硬质玻璃管中有大量黑色和白色固体产生。
③F中试管内壁有黑色沉淀产生。
产生上述现象②中黑色固体的原因是
(5)探究硬质玻璃管中固体产物中钠元素的存在形式:
假设一:白色固体是
 ;假设二:白色固体是
;假设二:白色固体是 ;假设三:白色固体是
;假设三:白色固体是 和
和 的混合物。请完成下列实验设计,验证上述假设:
的混合物。请完成下列实验设计,验证上述假设:步骤1:将硬质玻璃管中的固体产物溶于水后,过滤;
步骤2:往步骤1所得滤液中加入足量的
步骤3:往步骤2所得滤液中滴加几滴酚酞试液,滤液不变红色。
结论:假设一成立。
(6)根据上述实验现象及表格中的实验数据,写出Na与
 反应的总化学方程式:
反应的总化学方程式: |  |  |
| 66.70g | 69.00g | 72.15g |
您最近一年使用:0次
名校
解题方法
4 . 钪的价格昂贵,在地壳里的含量只有0.0005%。从铝土矿生产Al2O3的副产品“赤泥”(主要成分为Al2O3、Fe2O3、TiO2、Sc2O3)中回收钪,同时生产聚合硫酸铁铝[AlFe(OH)6-2n(SO4)n]具有极其重要的工业价值,一种工艺流程如图:
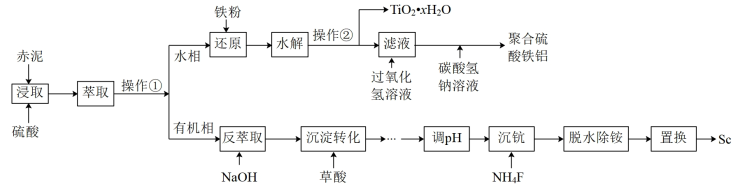
已知:钪离子可以在不同pH下生成[Sc(OH)n]3-n(n=1~6)。请回答以下问题:
(1)操作①和操作②中都使用的玻璃仪器是____ 。
(2)加入铁粉的作用:____ 。
(3)生成聚合硫酸铁铝[AlFe(OH)6-2n(SO4)n]沉淀,同时产生CO2,该反应的离子方程式为____ 。
(4)钪是一种重要的稀土金属,化学性质非常活泼,但发现较晚主要是因为____ 。
(5)“反萃取”时若加入的过量NaOH,则Sc(OH)3沉淀会溶解。写出Sc(OH)3与过量NaOH溶液反应生成n=6的含钪产物的化学方程式为____ 。
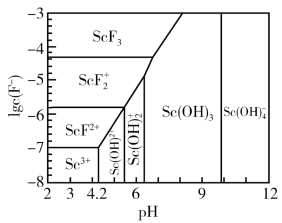
(6)常温下,三价Sc的部分存在形式与氟离子浓度的对数[1gc(F-)]、pH的关系如图所示。若溶液中c(F-)=5×10-6,“调pH”过程中控制pH=7,则调节pH后+3价Sc的存在形式为____ (填化学式)(lg5=0.7)。
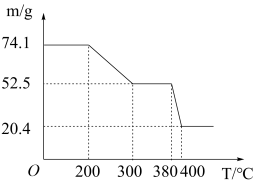
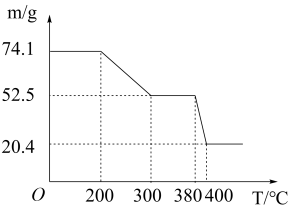
(7)“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O分解得到ScF3,某固体样品质量与温度的关系如图所示。加热至380-400℃产生白烟,400℃以上质量不再改变。则a=____ (填数字)。

已知:钪离子可以在不同pH下生成[Sc(OH)n]3-n(n=1~6)。请回答以下问题:
(1)操作①和操作②中都使用的玻璃仪器是
(2)加入铁粉的作用:
(3)生成聚合硫酸铁铝[AlFe(OH)6-2n(SO4)n]沉淀,同时产生CO2,该反应的离子方程式为
(4)钪是一种重要的稀土金属,化学性质非常活泼,但发现较晚主要是因为
(5)“反萃取”时若加入的过量NaOH,则Sc(OH)3沉淀会溶解。写出Sc(OH)3与过量NaOH溶液反应生成n=6的含钪产物的化学方程式为
(6)常温下,三价Sc的部分存在形式与氟离子浓度的对数[1gc(F-)]、pH的关系如图所示。若溶液中c(F-)=5×10-6,“调pH”过程中控制pH=7,则调节pH后+3价Sc的存在形式为

(7)“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O分解得到ScF3,某固体样品质量与温度的关系如图所示。加热至380-400℃产生白烟,400℃以上质量不再改变。则a=

您最近一年使用:0次
5 . NaNO2易溶于水,外观和食盐相似,有咸味,人误食会中毒。已知NaNO2能发生反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。请回答下列问题:
(1)上述反应中NaI____ (填序号)。
①是氧化产物
②是还原产物
③既不是氧化产物,又不是还原产物
④既是氧化产物,又是还原产物
(2)某厂废液中含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是____ (填序号)。
A.NaCl B.NH4C1 C.HNO3
(3)NaNO2也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留量均有严格规定。某实验小组欲用酸性KMnO4测定NaNO2样品纯度,所涉及到的反应有:
(a) +
+ +H+→
+H+→ +Mn2++H2O
+Mn2++H2O
(b) +H2C2O4+H+→Mn2++CO2↑+H2O
+H2C2O4+H+→Mn2++CO2↑+H2O
①配平反应(a)____ 。
②误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列分析错误的是____ (填序号)。
A.NaNO2被氧化B.维生素C具有还原性
C.还原性:维生素C>Fe2+D.NaNO2是氧化剂
(4)用含铬不锈钢废渣(含SiO2、Cr2O3、Fe2O3、Al2O3等)制取Cr2O3(铬绿)的工艺流程如图所示:
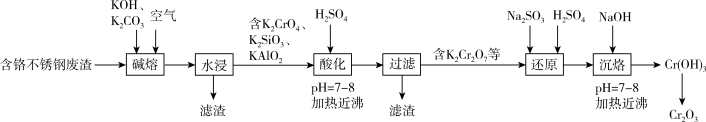
回答下列问题:
①Cr2O3、KOH、O2反应生成K2CrO4的化学方程式为____ 。
②“还原”时发生反应的离子方程式为____ 。
(1)上述反应中NaI
①是氧化产物
②是还原产物
③既不是氧化产物,又不是还原产物
④既是氧化产物,又是还原产物
(2)某厂废液中含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是
A.NaCl B.NH4C1 C.HNO3
(3)NaNO2也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留量均有严格规定。某实验小组欲用酸性KMnO4测定NaNO2样品纯度,所涉及到的反应有:
(a)
 +
+ +H+→
+H+→ +Mn2++H2O
+Mn2++H2O(b)
 +H2C2O4+H+→Mn2++CO2↑+H2O
+H2C2O4+H+→Mn2++CO2↑+H2O①配平反应(a)
②误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列分析错误的是
A.NaNO2被氧化B.维生素C具有还原性
C.还原性:维生素C>Fe2+D.NaNO2是氧化剂
(4)用含铬不锈钢废渣(含SiO2、Cr2O3、Fe2O3、Al2O3等)制取Cr2O3(铬绿)的工艺流程如图所示:

回答下列问题:
①Cr2O3、KOH、O2反应生成K2CrO4的化学方程式为
②“还原”时发生反应的离子方程式为
您最近一年使用:0次
2022-05-13更新
|
241次组卷
|
3卷引用:福建省龙岩第一中学2022-2023学年高三上学期第二次月考化学试题
名校
6 . 草酸(乙二酸)存在于自然界的植物中,其钙盐难溶于水。草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,175℃时分解。草酸及其盐在生产生活中有重要用途。某兴趣小组计划制备草酸并研究其性质。
(1)制备草酸。用含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为3:2)溶液氧化淀粉水解液制备草酸,其装置如图一所示。[已知:硝酸氧化淀粉水解液过程中主要反应:C6H12O6+HNO3→H2C2O4+NO2↑+NO↑+H2O(未配平)]

①该反应的温度需控制在55~60℃,适宜的加热方式为___________ 。
②仪器c的名称为___________ 。a为冷凝水的___________ 口。(填“进水”、“出水”)
③碳酸钠溶液用于尾气吸收。当尾气中n(NO2):n(NO)=1:1时,写出对应的的化学方程式:___________
(2)研究草酸热稳定性。
写出草酸晶体(H2C2O4·2H2O)加热分解生成气态产物的化学方程式:___________ ,最合适的分解装置是___________ (填标号)。
a. b.
b. c.
c. d.
d.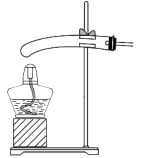
(3)草酸及其盐可用于测定血钙的含量。方法是:取10.00mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,充分反应。将沉淀过滤洗涤后用稀硫酸溶解,并稀释至100mL,取出25.00mL用标准KMnO4溶液滴定。
①溶解CaC2O4沉淀时不能用盐酸,原因是:___________
②滴定终点的现象为___________
③若最终消耗了1.250×10-4mol/L的KMnO4溶液20.00mL,则该血液样品中含钙量为___________ mmol/L。
(1)制备草酸。用含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为3:2)溶液氧化淀粉水解液制备草酸,其装置如图一所示。[已知:硝酸氧化淀粉水解液过程中主要反应:C6H12O6+HNO3→H2C2O4+NO2↑+NO↑+H2O(未配平)]

①该反应的温度需控制在55~60℃,适宜的加热方式为
②仪器c的名称为
③碳酸钠溶液用于尾气吸收。当尾气中n(NO2):n(NO)=1:1时,写出对应的的化学方程式:
(2)研究草酸热稳定性。
写出草酸晶体(H2C2O4·2H2O)加热分解生成气态产物的化学方程式:
a.
 b.
b. c.
c. d.
d.
(3)草酸及其盐可用于测定血钙的含量。方法是:取10.00mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,充分反应。将沉淀过滤洗涤后用稀硫酸溶解,并稀释至100mL,取出25.00mL用标准KMnO4溶液滴定。
①溶解CaC2O4沉淀时不能用盐酸,原因是:
②滴定终点的现象为
③若最终消耗了1.250×10-4mol/L的KMnO4溶液20.00mL,则该血液样品中含钙量为
您最近一年使用:0次
2022-01-12更新
|
99次组卷
|
2卷引用:福建省长汀县第一中学2021-2022学年高三上学期第三次月考化学试题
7 . 钪的价格昂贵,在地壳里的含量只有0.0005%。从铝土矿生产Al2O3的副产品“赤泥”(主要成分为Al2O3、Fe2O3、TiO2、Sc2O3)中回收钪,同时生产聚合硫酸铁铝[AlFe(OH)6-2n(SO4)n]具有极其重要的工业价值,一种工艺流程如下:
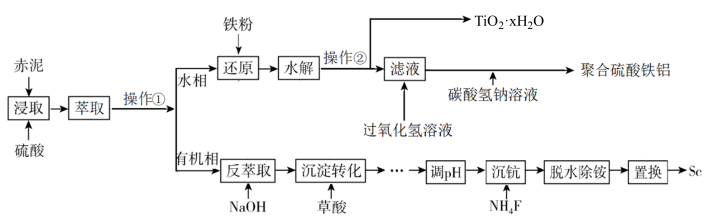
已知:钪离子可以在不同pH下生成[Sc(OH)n] 3-n(n=1~6)。请回答以下问题:
(1)操作②的名称:_______ ,操作①和操作②中都使用的玻璃仪器是_______ 。
(2)加入铁粉的作用:_______ 。
(3)生成聚合硫酸铁铝[AlFe(OH)6-2n(SO4)n]的离子方程式为_______ 。
(4)钪是一种重要的稀土金属,化学性质非常活泼,但发现较晚主要是因为_______ 。
(5)“反萃取”时若加入的氢氧化钠过量则 Sc(OH)3沉淀会溶解。写出Sc(OH)3与过量NaOH溶液反应生成 n=6 的含钪产物的化学方程式为_______ 。
(6)常温下,三价Sc的部分存在形式与氟离子浓度的对数[1gc(F- )]、pH 的关系如图所示。若溶液中c(F- )=5×10-6,“调 pH”过程中控制 pH=7,则调节pH后三价Sc的存在形式为_______ (填化学式)(lg5=0.7)。
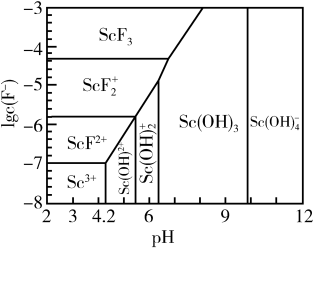
(7)“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O 分解得到ScF3,某固体样品质量与温度的关系如图所示。加热至 380-400℃产生白烟,400℃以上质量不再改变。则a=_______ (填数字)。

已知:钪离子可以在不同pH下生成[Sc(OH)n] 3-n(n=1~6)。请回答以下问题:
(1)操作②的名称:
(2)加入铁粉的作用:
(3)生成聚合硫酸铁铝[AlFe(OH)6-2n(SO4)n]的离子方程式为
(4)钪是一种重要的稀土金属,化学性质非常活泼,但发现较晚主要是因为
(5)“反萃取”时若加入的氢氧化钠过量则 Sc(OH)3沉淀会溶解。写出Sc(OH)3与过量NaOH溶液反应生成 n=6 的含钪产物的化学方程式为
(6)常温下,三价Sc的部分存在形式与氟离子浓度的对数[1gc(F- )]、pH 的关系如图所示。若溶液中c(F- )=5×10-6,“调 pH”过程中控制 pH=7,则调节pH后三价Sc的存在形式为

(7)“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O 分解得到ScF3,某固体样品质量与温度的关系如图所示。加热至 380-400℃产生白烟,400℃以上质量不再改变。则a=

您最近一年使用:0次
2022-04-22更新
|
1482次组卷
|
11卷引用:化学-2022年高考考前押题密卷(福建卷)
(已下线)化学-2022年高考考前押题密卷(福建卷)黑龙江省哈尔滨市第九中学2022届高三下学期第三次模拟考试理综化学试题(已下线)专项15 工艺流程综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)押江苏卷第15题 化学工业流程综合题 -备战2022年高考化学临考题号押题(江苏卷)山东师范大学附属中学2022届高三考前预测化学试题吉林市第一中学2021-2022学年高三下学期4月教学质量检测理科综合化学试题湖南省郴州市永兴县第一中学2021-2022学年高三下学期期中考试化学试题湖南省长沙市雅礼中学2022-2023学年高三上学期月考(三)化学试题山东省鄄城县第一中学2022-2023学年高二上学期期末考试化学试题湖南省攸县第一中学2022-2023学年高三第六次月考化学试题湖南省涟源市第一中学2023届高三第五次月考化学试题
名校
解题方法
8 . 亚氯酸钠(NaClO2)是一种应用广泛的高效氧化型漂白剂。以下是某小组模拟工业制法利用ClO2与H2O2在碱性条件下制备少量NaClO2的实验装置:

已知:
①硫酸作酸化剂时,甲醇(CH3OH)可将NaClO3还原为ClO2。
②ClO2沸点为9.9℃,可溶于水,有毒,气体中ClO2浓度较高时易发生爆炸。
③饱和NaClO2溶液在温度低于38℃时析出晶体NaClO2•3H2O,在温度高于38℃时析出晶体NaClO2,高于60℃时分解生成NaClO3和NaCl。
回答下列问题:
(1)实验前用浓硫酸与50%甲醇溶液配制混合溶液的操作是:___________ 。
(2)装置A中,若氧化产物为CO2,则氧化剂与还原剂的物质的量之比为___________ 。
(3)装置B中生成NaClO2的化学方程式是___________ 。
(4)装置C中ClO2与NaOH溶液反应生成等物质的量的两种钠盐,其中一种为NaClO2,装置C中ClO2与NaOH溶液反应的离子方程式是___________
(5)从反应后的B溶液中制得NaClO2晶体的操作步骤是:a.控制在38~60℃之间蒸发浓缩;b.___________ ;c.用38~60℃的热水洗涤;d.在低于60oC的真空中蒸发,干燥。
(6)NaClO2纯度测定:①称取所得NaClO2样品1.000g于烧杯中,加入适量蒸馏水与过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(C1O 的还原产物为Cl-),将所得混合液配成250mL待测溶液;②取25.00mL待测液,用0.2000mol/LNa2S2O3标准液滴定(I2+2S2O
的还原产物为Cl-),将所得混合液配成250mL待测溶液;②取25.00mL待测液,用0.2000mol/LNa2S2O3标准液滴定(I2+2S2O =2I-+S4O
=2I-+S4O ),以淀粉溶液做指示剂重复滴定3次,测得Na2S2O3标准液平均用量为18.00mL,则该样品中NaClO2的质量分数为
),以淀粉溶液做指示剂重复滴定3次,测得Na2S2O3标准液平均用量为18.00mL,则该样品中NaClO2的质量分数为___________ 。

已知:
①硫酸作酸化剂时,甲醇(CH3OH)可将NaClO3还原为ClO2。
②ClO2沸点为9.9℃,可溶于水,有毒,气体中ClO2浓度较高时易发生爆炸。
③饱和NaClO2溶液在温度低于38℃时析出晶体NaClO2•3H2O,在温度高于38℃时析出晶体NaClO2,高于60℃时分解生成NaClO3和NaCl。
回答下列问题:
(1)实验前用浓硫酸与50%甲醇溶液配制混合溶液的操作是:
(2)装置A中,若氧化产物为CO2,则氧化剂与还原剂的物质的量之比为
(3)装置B中生成NaClO2的化学方程式是
(4)装置C中ClO2与NaOH溶液反应生成等物质的量的两种钠盐,其中一种为NaClO2,装置C中ClO2与NaOH溶液反应的离子方程式是
(5)从反应后的B溶液中制得NaClO2晶体的操作步骤是:a.控制在38~60℃之间蒸发浓缩;b.
(6)NaClO2纯度测定:①称取所得NaClO2样品1.000g于烧杯中,加入适量蒸馏水与过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(C1O
 的还原产物为Cl-),将所得混合液配成250mL待测溶液;②取25.00mL待测液,用0.2000mol/LNa2S2O3标准液滴定(I2+2S2O
的还原产物为Cl-),将所得混合液配成250mL待测溶液;②取25.00mL待测液,用0.2000mol/LNa2S2O3标准液滴定(I2+2S2O =2I-+S4O
=2I-+S4O ),以淀粉溶液做指示剂重复滴定3次,测得Na2S2O3标准液平均用量为18.00mL,则该样品中NaClO2的质量分数为
),以淀粉溶液做指示剂重复滴定3次,测得Na2S2O3标准液平均用量为18.00mL,则该样品中NaClO2的质量分数为
您最近一年使用:0次
2021-09-28更新
|
449次组卷
|
4卷引用:福建省平潭翰英中学2021-2022学年高三上学期第一次月考化学试题
福建省平潭翰英中学2021-2022学年高三上学期第一次月考化学试题江西省上高二中2022届高三第二次月考化学试卷(已下线)期中试卷02-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)2020年全国卷Ⅱ化学真题变式题
名校
解题方法
9 . 已知: 是重要的硫-氮二元化合物,室温下为橙黄色的固体,178~187℃熔化并分解,可用氨气与
是重要的硫-氮二元化合物,室温下为橙黄色的固体,178~187℃熔化并分解,可用氨气与 反应制得。某同学利用下图装置制取
反应制得。某同学利用下图装置制取 ,然后制取
,然后制取 。已知:
。已知: 为红棕色液体,有刺激性臭味,熔点:
为红棕色液体,有刺激性臭味,熔点: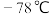 ,沸点:60℃,易水解。
,沸点:60℃,易水解。
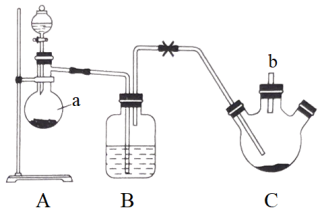
反应步骤:①反应时先向三颈烧瓶中通入干燥的氯气,使硫粉与氯气在50℃下反应生成 。
。
②待三颈烧瓶中的硫粉全部反应后,关闭B、C之间的止水夹,撤掉A、B装置。
③连接制氨气的装置,通入氨气,反应制得 。
。
试回答下列问题。
(1)仪器a的名称为_______ ,a中三氧化铬(还原产物中铬为+3价)可与浓盐酸快速反应制得氯气,写出反应的离子方程式_______ 。
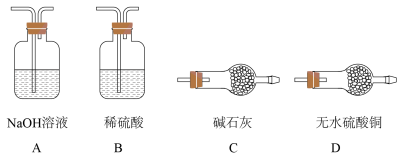
(2)B装置中应选择的试剂为_______ 。制取 过程中,b导管末端应连接下图中的
过程中,b导管末端应连接下图中的_______ (填序号)。
(3)向制得的 中通入
中通入 ,生成
,生成 的同时还生成一种常见固体单质和一种盐,写出反应的化学方程式
的同时还生成一种常见固体单质和一种盐,写出反应的化学方程式_______ 。所得产物分离后,检验所得盐中阳离子的具体操作步骤和现象_______ 。
(4) 在碱性条件下发生水解反应氮元素转化为氨气,用硼酸吸收,滴定氨气释放量可进一步测定
在碱性条件下发生水解反应氮元素转化为氨气,用硼酸吸收,滴定氨气释放量可进一步测定 的纯度。称取
的纯度。称取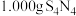 样品,加入NaOH溶液,并加热,释放出的氨气用足量
样品,加入NaOH溶液,并加热,释放出的氨气用足量 硼酸溶液吸收[反应方程式为
硼酸溶液吸收[反应方程式为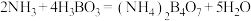 ,假定反应过程中溶液体积不变]。反应后的硼酸溶滚,以甲基红-亚甲蓝为指示剂,再用
,假定反应过程中溶液体积不变]。反应后的硼酸溶滚,以甲基红-亚甲蓝为指示剂,再用 的盐酸[滴定反应方程式为
的盐酸[滴定反应方程式为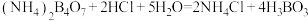 ]进行滴定,重复三次实验。实验数据记录如下表所示:
]进行滴定,重复三次实验。实验数据记录如下表所示:
则制得的 的纯度为
的纯度为_______ 。
 是重要的硫-氮二元化合物,室温下为橙黄色的固体,178~187℃熔化并分解,可用氨气与
是重要的硫-氮二元化合物,室温下为橙黄色的固体,178~187℃熔化并分解,可用氨气与 反应制得。某同学利用下图装置制取
反应制得。某同学利用下图装置制取 ,然后制取
,然后制取 。已知:
。已知: 为红棕色液体,有刺激性臭味,熔点:
为红棕色液体,有刺激性臭味,熔点: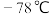 ,沸点:60℃,易水解。
,沸点:60℃,易水解。
反应步骤:①反应时先向三颈烧瓶中通入干燥的氯气,使硫粉与氯气在50℃下反应生成
 。
。②待三颈烧瓶中的硫粉全部反应后,关闭B、C之间的止水夹,撤掉A、B装置。
③连接制氨气的装置,通入氨气,反应制得
 。
。试回答下列问题。
(1)仪器a的名称为
(2)B装置中应选择的试剂为
 过程中,b导管末端应连接下图中的
过程中,b导管末端应连接下图中的
(3)向制得的
 中通入
中通入 ,生成
,生成 的同时还生成一种常见固体单质和一种盐,写出反应的化学方程式
的同时还生成一种常见固体单质和一种盐,写出反应的化学方程式(4)
 在碱性条件下发生水解反应氮元素转化为氨气,用硼酸吸收,滴定氨气释放量可进一步测定
在碱性条件下发生水解反应氮元素转化为氨气,用硼酸吸收,滴定氨气释放量可进一步测定 的纯度。称取
的纯度。称取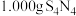 样品,加入NaOH溶液,并加热,释放出的氨气用足量
样品,加入NaOH溶液,并加热,释放出的氨气用足量 硼酸溶液吸收[反应方程式为
硼酸溶液吸收[反应方程式为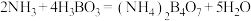 ,假定反应过程中溶液体积不变]。反应后的硼酸溶滚,以甲基红-亚甲蓝为指示剂,再用
,假定反应过程中溶液体积不变]。反应后的硼酸溶滚,以甲基红-亚甲蓝为指示剂,再用 的盐酸[滴定反应方程式为
的盐酸[滴定反应方程式为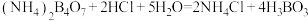 ]进行滴定,重复三次实验。实验数据记录如下表所示:
]进行滴定,重复三次实验。实验数据记录如下表所示:| 实验序号 | 初始读数 | 最终读数 |
| I | 0.10 | 20.14 |
| II | 0.50 | 24.75 |
| III | 1.00 | 20.96 |
 的纯度为
的纯度为
您最近一年使用:0次
2021-09-08更新
|
902次组卷
|
5卷引用:福建省部分名校2021-2022学年高三上学期11月联合测评化学试题
福建省部分名校2021-2022学年高三上学期11月联合测评化学试题辽宁省朝阳市建平县实验中学2022届高三上学期第一次联考化学试题河北省石家庄市第二中学2021-2022学年高三上学期期中考试化学试题河北省衡水市2021-2022学年高三上学期三调化学试题(已下线)一轮巩固卷7-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)
名校
10 . 氮化铝(AlN)是一种新型无机非金属材料。
Ⅰ、氮化铝可用以下两种方法制备:
(1)①氧化铝高温还原法:
_______Al2O3 +_______C+_______N2 _______AlN+_______CO
_______AlN+_______CO
②氯化铝与氨气高温合成法:AlCl3+NH3 AlN+3HCl
AlN+3HCl
配平方程式:_______ 。
(2)方法②比方法①在生产上更具优势。下列说法正确的是_______ 。
A.方法①中的Al2O3和C容易残留在氮化铝中
B.两种方法中氮化铝均为还原产物
Ⅱ、某AlN样品仅含有Al2O3杂质,为测定AlN的含量,设计如下二种实验方案。已知:AlN+NaOH+H2O═NaAlO2+NH3↑。
【方案1】取一定量母的样品,用图1装置测量样品中AlN的纯度(夹持装置已略去)。

(3)如图C装置中球形干燥管的作用是_______ 。
(4)完成以下实验步骤:组装好实验装置,首先_______ ,再加入实验药品,接下来的实验操作是_______ ,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体,打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是_______ 。
(5)由于装置存在缺陷,导致测定结果偏高,请提出改进意见_______ 。
【方案2】用如图2装置测定mg样品中AlN的纯度(部分夹持装置已略去)。
(6)导管a的主要作用是_______ 。
(7)为测定生成气体的体积,量气装置中的X液体可以是_______ (填选项序号)。
a.CCl4b.H2O c.稀硫酸d.苯
(8)若mg样品完全反应,测得生成气体的体积为VmL(已转换为标准状况),则AlN的质量分数是_______ (用含m、V的数学表达式表示)。
Ⅰ、氮化铝可用以下两种方法制备:
(1)①氧化铝高温还原法:
_______Al2O3 +_______C+_______N2
 _______AlN+_______CO
_______AlN+_______CO②氯化铝与氨气高温合成法:AlCl3+NH3
 AlN+3HCl
AlN+3HCl配平方程式:
(2)方法②比方法①在生产上更具优势。下列说法正确的是
A.方法①中的Al2O3和C容易残留在氮化铝中
B.两种方法中氮化铝均为还原产物
Ⅱ、某AlN样品仅含有Al2O3杂质,为测定AlN的含量,设计如下二种实验方案。已知:AlN+NaOH+H2O═NaAlO2+NH3↑。
【方案1】取一定量母的样品,用图1装置测量样品中AlN的纯度(夹持装置已略去)。

(3)如图C装置中球形干燥管的作用是
(4)完成以下实验步骤:组装好实验装置,首先
(5)由于装置存在缺陷,导致测定结果偏高,请提出改进意见
【方案2】用如图2装置测定mg样品中AlN的纯度(部分夹持装置已略去)。
(6)导管a的主要作用是
(7)为测定生成气体的体积,量气装置中的X液体可以是
a.CCl4b.H2O c.稀硫酸d.苯
(8)若mg样品完全反应,测得生成气体的体积为VmL(已转换为标准状况),则AlN的质量分数是
您最近一年使用:0次



