名校
1 . 绿矾是一种重要的硫酸盐,其化学式为FeSO4•7H2O。
(1)某化学兴趣小组通过实验探究来测定某绿矾样品中FeSO4•7H2O的含量,步骤如下:
i.称取上述样品9.0g,配成250mL准确浓度的FeSO4溶液:
ii.量取25.00mL上述溶液于锥形瓶中,用0.02000mol•L-1的酸性KMnO4溶液与之完全反应,消耗KMnO4溶液30.00mL(杂质不与KMnO4溶液反应)。
①配制FeSO4溶液时,需要的仪器有药匙、玻璃棒、_______ (从下列图中选择,写出名称)。
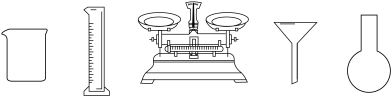
尚缺少的玻璃仪器为:_______ 。配制溶液过程中未洗涤烧杯、玻璃棒,会造成所配溶液浓度_______ ,定容时俯视液面会造成所配溶液浓度_______ (填“偏大”、“偏小“或“无影响”)。
②步骤ii中反应的离子方程式为_________ 。
③该样品中FeSO4•7H2O的质量百分含量为________ (计算结果保留1位小数)。
(2)硫酸亚铁晶体(FeSO4•7H2O)隔绝空气加热至高温会分解产生水、金属氧化物和非金属氧化物,某化学兴趣小组的同学对绿矾分解产物进行了探究:
①将硫酸亚铁晶体高温分解产生的气体通入足量的BaCl2溶液吸收后有白色沉淀产生,说明非金属氧化物中含有_______ 。
②取完全分解后的固体进行实验,实验操作及现象如下:
i将固体加入盛有足量稀硫酸的试管中,固体完全溶解,且无气体放出;
ii取i中溶液滴入适量KMnO4溶液中,KMnO4溶液不褪色;
iii取i中溶液滴入KSCN溶液中,溶液变红色。
由此得出结论:红色固体为________ 。
③硫酸亚铁晶体加热分解的化学方程式为________ 。
(1)某化学兴趣小组通过实验探究来测定某绿矾样品中FeSO4•7H2O的含量,步骤如下:
i.称取上述样品9.0g,配成250mL准确浓度的FeSO4溶液:
ii.量取25.00mL上述溶液于锥形瓶中,用0.02000mol•L-1的酸性KMnO4溶液与之完全反应,消耗KMnO4溶液30.00mL(杂质不与KMnO4溶液反应)。
①配制FeSO4溶液时,需要的仪器有药匙、玻璃棒、

尚缺少的玻璃仪器为:
②步骤ii中反应的离子方程式为
③该样品中FeSO4•7H2O的质量百分含量为
(2)硫酸亚铁晶体(FeSO4•7H2O)隔绝空气加热至高温会分解产生水、金属氧化物和非金属氧化物,某化学兴趣小组的同学对绿矾分解产物进行了探究:
①将硫酸亚铁晶体高温分解产生的气体通入足量的BaCl2溶液吸收后有白色沉淀产生,说明非金属氧化物中含有
②取完全分解后的固体进行实验,实验操作及现象如下:
i将固体加入盛有足量稀硫酸的试管中,固体完全溶解,且无气体放出;
ii取i中溶液滴入适量KMnO4溶液中,KMnO4溶液不褪色;
iii取i中溶液滴入KSCN溶液中,溶液变红色。
由此得出结论:红色固体为
③硫酸亚铁晶体加热分解的化学方程式为
您最近一年使用:0次
名校
2 . 已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体。他们之间有如图转化关系:
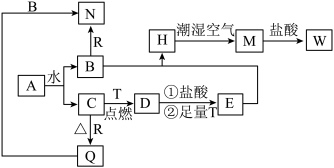
(1)写出下列反应离子方程式:
①B+R:_______ ,
②灵敏检验W中阳离子的原理:________ ,
③D→E:________ ,
④H→M:________ 。
(2)实验室保存E溶液时需向其中加入铁粉,原因为:________ (结合离子方程式说明)。
(3)将B溶液加入铵明矾[NH4Al(SO4)2]溶液至生成的沉淀全部溶解的离子方程式为:_______ 。
(4)现有一定量的RCl3和TCl3混合溶液,已知其中R3+、T3+的物质的量之和为0.10mol,若向此溶液中加入170mL2mol/L的NaOH溶液,设R3+物质的量与总物质的量(0.10mol)的比值为x,则当x=0.4时,沉淀的物质的量为________ mol。请在图中画出沉淀总量(y)随x(0→1.0)的变化曲线________ 。
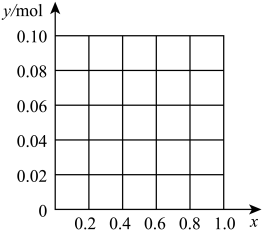

(1)写出下列反应离子方程式:
①B+R:
②灵敏检验W中阳离子的原理:
③D→E:
④H→M:
(2)实验室保存E溶液时需向其中加入铁粉,原因为:
(3)将B溶液加入铵明矾[NH4Al(SO4)2]溶液至生成的沉淀全部溶解的离子方程式为:
(4)现有一定量的RCl3和TCl3混合溶液,已知其中R3+、T3+的物质的量之和为0.10mol,若向此溶液中加入170mL2mol/L的NaOH溶液,设R3+物质的量与总物质的量(0.10mol)的比值为x,则当x=0.4时,沉淀的物质的量为

您最近一年使用:0次
名校
3 . ①液态醋酸;②液氨;③Ba(OH)2溶液;④熔融AlCl3;⑤Fe(OH)3胶体;⑥镁;⑦CO2;⑧HI溶液;⑨蔗糖(C12H22O11)
(1)以上物质中属于电解质的是_______ (填序号);以上纯净物中能导电的是_______ (填序号)。
(2)写出⑥⑦反应的化学方程式:________ 。
(3)将34.2g蔗糖完全燃烧后的产物通过足量Na2O2,Na2O2增重_______ 34.2g(填“>”、“<”或“=”)。
(4)写出⑤和足量⑧反应的离子方程式________ 。
(1)以上物质中属于电解质的是
(2)写出⑥⑦反应的化学方程式:
(3)将34.2g蔗糖完全燃烧后的产物通过足量Na2O2,Na2O2增重
(4)写出⑤和足量⑧反应的离子方程式
您最近一年使用:0次
名校
4 . 下列离子组在一定条件下能大量共存,且加入试剂后发生反应的离子方程式正确的是
| 选项 | 离子组 | 加入试剂 | 发生反应的离子方程式 |
| A | K+、 、 、 | 少量CO2 | CO2+2H2O+ =Al(OH)3↓+ =Al(OH)3↓+  |
| B | Fe3+、K+、I- | NaOH溶液 | Fe3++3OH-=Fe(OH)3↓ |
| C | Na+、K+、 | 少量盐酸 |  +H2O+H+=Al(OH)3↓ +H2O+H+=Al(OH)3↓ |
| D | Ba2+、Na+、OH- | NaHCO3溶液 |  +OH-= +OH-=  +H2O +H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
Ⅰ.现有以下物质:① ②Cu ③NaCl ④
②Cu ③NaCl ④ 胶体 ⑤乙醇 ⑥CO2 ⑦稀硫酸
胶体 ⑤乙醇 ⑥CO2 ⑦稀硫酸
(1)以上物质中属于混合物的是_______ (填序号,下同),属于电解质的是_______ 。
(2)向④中逐滴滴加⑦,可观察到的现象是_______ 。
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(3)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是_______ (填字母)。

(4)有同学认为所有酸碱中和反应均可表示为 。请举个例子反驳上述观点(用化学方程式表示)
。请举个例子反驳上述观点(用化学方程式表示)_______ 。
Ⅰ.现有以下物质:①
 ②Cu ③NaCl ④
②Cu ③NaCl ④ 胶体 ⑤乙醇 ⑥CO2 ⑦稀硫酸
胶体 ⑤乙醇 ⑥CO2 ⑦稀硫酸(1)以上物质中属于混合物的是
(2)向④中逐滴滴加⑦,可观察到的现象是
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(3)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(4)有同学认为所有酸碱中和反应均可表示为
 。请举个例子反驳上述观点(用化学方程式表示)
。请举个例子反驳上述观点(用化学方程式表示)
您最近一年使用:0次
6 . 把碎纸片b补充到a中,可得到一个完整的离子方程式(未配平)。下列说法正确的是


A.反应物微粒是S、 、 、 | B.氧化剂与还原剂的粒子个数比为2:1 |
| C.该反应可能在酸性条件下进行 | D.每生成2个 反应转移的电子数为6 反应转移的电子数为6 |
您最近一年使用:0次
2023-06-07更新
|
107次组卷
|
2卷引用:广东省揭阳市揭西县河婆中学2020-2021学年高一上学期第一次月考化学试题
名校
解题方法
7 . 表示下列反应的离子方程式正确的是
A.铁跟稀硫酸反应: |
B.氢氧化钡溶液和稀硫酸反应: |
C.向 溶液中加入NaOH溶液: 溶液中加入NaOH溶液: |
D.向 溶液通入HCl气体: 溶液通入HCl气体: |
您最近一年使用:0次
2023-06-07更新
|
250次组卷
|
2卷引用:广东省揭阳市揭西县河婆中学2020-2021学年高一上学期第一次月考化学试题
名校
8 . 元素①~⑧在元素周期表中的位置如图,回答有关问题:
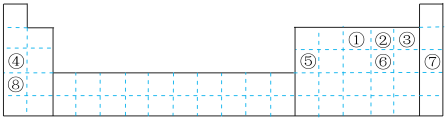
(1)画出⑥的离子结构示意图______ ;写出②含有10个中子的核素的化学符号_____ 。
(2)请写出①的氢化物发生催化氧化的化学方程式______ 。
(3)表中能形成两性氢氧化物的元素是______ (填元素符号),写出该元素的氧化物与⑧的最高价氧化物的水化物反应的离子方程式_____ 。
(4)由②④⑥三种元素组成的一种盐在空气中放置会变质,请用化学方程式表示变质的反应______ 。

(1)画出⑥的离子结构示意图
(2)请写出①的氢化物发生催化氧化的化学方程式
(3)表中能形成两性氢氧化物的元素是
(4)由②④⑥三种元素组成的一种盐在空气中放置会变质,请用化学方程式表示变质的反应
您最近一年使用:0次
名校
解题方法
9 . 下列离子方程式中,正确的是
| A.稀盐酸滴在铜片上:Cu + 2H+= Cu2+ + H2↑ |
| B.氧化铜加入稀硫酸中: O2- + 2H+=H2O |
| C.铁粉加入氯化铁溶液中:Fe + Fe3+=2Fe2+ |
D.盐酸滴入碳酸氢钠溶液中:H++ HCO =CO2↑ + H2O =CO2↑ + H2O |
您最近一年使用:0次
2023-05-03更新
|
190次组卷
|
6卷引用:2019年湖南省普通高中学业水平考试化学试题
名校
解题方法
10 . 下列解释事实的方程式不正确的是
| A.醋酸溶液显酸性:CH3COOH⇌H++CH3COO- |
| B.用氨水除去烟气中的SO2:SO2+2NH3•H2O=(NH4)2SO3+H2O |
| C.向盐碱地中施放硫酸钙,降低其碱性:Na2CO3+CaSO4=CaCO3+Na2SO4 |
| D.用三氯化铁溶液腐蚀线路板:Fe3++Cu=Fe2++Cu2+ |
您最近一年使用:0次



