14-15高三上·上海松江·期末
1 . 关于由 37Cl原子组成的氯气叙述正确的是
| A.71g该氯气样品含1mol氯气 |
| B.22.4L该氯气样品质量是74g |
| C.37g该氯气样品与足量浓热的NaOH溶液完全反应生成Na37Cl和Na37ClO3,氧化剂和还原剂的质量之比为5︰1 |
| D.0.1mol氯气分子溶于水形成1000mL溶液,溶液中c(Cl- )+ c(ClO- )=0.1mol/L |
您最近一年使用:0次
13-14高三上·上海·阶段练习
名校
解题方法
2 . 已知氧化性:Br2>Fe3+>I2,向含有a mol FeI2的溶液中加入含b mol Br2的溴水,下列判断或相应的离子方程式正确的是
| A.当a=2,b=1时,离子方程式为:2Fe2++Br2→2Fe3++2Br- |
| B.如果反应后的溶液中存在c(Fe2+)=c(Fe3+),则4/5<a/b<1 |
| C.当a=1,b=2时,离子方程式为:2Fe2++4I-+3Br2→2Fe3++2I2+6Br- |
| D.当a=2,2<b<3时,溶液中铁元素以两种离子形式存在,且一定是c(Fe3+)>c(Fe2+) |
您最近一年使用:0次
2013·上海闵行·三模
3 . 为了测定铜铁合金中铜的质量分数,在10.00g试样中加入200mL、0.6mol/L的稀硝酸,充分反应后剩余金属7.48g,再向其中加入50mL、0.4mol/L的稀硫酸,充分振荡后剩余金属6.60g。若硝酸的还原产物只有NO,下列说法正确的是
| A.上述测定不能达到实验目的 | B.剩余的7.48g金属为铜 |
| C.共生成NO气体 0.04mol | D.该合金中铜的质量分数为69.2% |
您最近一年使用:0次
名校
4 . 两种大气污染物NO2和SO2在一定条件下可以发生如下反应:NO2+SO2===NO+SO3,在体积为V L的密闭容器中通入3 mol NO2和5 mol SO2,反应后容器内氮原子和氧原子个数比为 ( )
| A.3∶10 | B.16∶3 | C.3∶16 | D.5∶16 |
您最近一年使用:0次
2016-12-09更新
|
340次组卷
|
8卷引用:上海市宝山中学2021-2022学年高一上学期10月考试化学试题
上海市宝山中学2021-2022学年高一上学期10月考试化学试题(已下线)2013-2014学年黑龙江省鹤岗一中高一上学期期末化学试卷2015-2016学年黑龙江省哈尔滨六中高一上期末化学试卷【全国百强校】新疆生产建设兵团第二中学2017-2018学年高二下学期期末考试化学试题(已下线)2019高考备考一轮复习精品资料 第一章 从实验学化学 第1讲 物质的量、气体摩尔体积【押题专练】重庆市缙云教育联盟2021-2022学年高二12月月考化学试题云南省龙陵县第一中学2022-2023学年高一下学期期末考试化学试题内蒙古自治区赤峰四中2021-2022学年高一上学期第一次月考化学试题
13-14高三上·上海·期中
5 . 闪锌矿(主要成分为ZnS)是含锌主要矿物之一,高温加热闪锌矿生成ZnO和SO2。ZnO用于冶炼金属锌,SO2可制亚硫酸盐或硫酸。计算回答下列问题(保留2位小数)
(1)取1.56 g闪锌矿样品,在空气中高温加热(杂质不反应),充分反应后,冷却,得到残留固体的质量为1.32 g,样品中含硫化锌的质量分数是_________ 。
(2)取1.95 g锌加入到12.00 mL 18.4 mol/L的浓硫酸中(假设生成的气体中无氢气,浓硫酸产生单一的还原产物),充分反应后,小心地将溶液稀释到1000 mL,取出15.00 mL,以酚酞为指示剂,用0.25 mol/L的NaOH溶液滴定,耗用NaOH溶液的体积为21.70 mL。通过计算确定浓硫酸被还原的产物是________ 。
(3)若将ZnS溶于强酸可产生硫化氢气体。在120℃、1 atm下,将100 mL硫化氢和氧气的混合气体点燃,恢复到原来状态,测得剩余气体为70 mL,求原混合气体中硫化氢的体积分数_________ 。(不考虑硫化氢气体自身受热分解)
(4)将标况下4.48 L SO2气体慢慢通入200 mL一定浓度NaOH溶液中,SO2气体全部被吸收,将反应后的溶液在空气中小心蒸干(不考虑酸式盐的分解),得到不超过两种物质的无水晶体26.8g。通过计算确定所得晶体的成分与物质的量________ 。
(1)取1.56 g闪锌矿样品,在空气中高温加热(杂质不反应),充分反应后,冷却,得到残留固体的质量为1.32 g,样品中含硫化锌的质量分数是
(2)取1.95 g锌加入到12.00 mL 18.4 mol/L的浓硫酸中(假设生成的气体中无氢气,浓硫酸产生单一的还原产物),充分反应后,小心地将溶液稀释到1000 mL,取出15.00 mL,以酚酞为指示剂,用0.25 mol/L的NaOH溶液滴定,耗用NaOH溶液的体积为21.70 mL。通过计算确定浓硫酸被还原的产物是
(3)若将ZnS溶于强酸可产生硫化氢气体。在120℃、1 atm下,将100 mL硫化氢和氧气的混合气体点燃,恢复到原来状态,测得剩余气体为70 mL,求原混合气体中硫化氢的体积分数
(4)将标况下4.48 L SO2气体慢慢通入200 mL一定浓度NaOH溶液中,SO2气体全部被吸收,将反应后的溶液在空气中小心蒸干(不考虑酸式盐的分解),得到不超过两种物质的无水晶体26.8g。通过计算确定所得晶体的成分与物质的量
您最近一年使用:0次
13-14高三上·上海·期中
6 . 某溶液中含有大量的Cl-、Br-、I-,若向l L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,原溶液中Cl-、Br-、I-的物质的量浓度之比为
| Cl2的体积(标准状况) | 5.6L | 11.2L | 22.4L |
| n(Cl-) | 1.5mol | 2.0mol | 3.0mol |
| n(Br-) | 3.0mol | 2.8mol | 1.8mol |
| n(I-) | xmol | 0 | 0 |
| A.5:15:4 | B.5:12:4 | C.15 : 30 : 8 | D.条件不足,无法计算 |
您最近一年使用:0次
13-14高三上·四川绵阳·阶段练习
名校
7 . 常温下,在某200mL的稀硫酸和稀硝酸的混合溶液中逐量地加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。(设硝酸只被还原为NO气体,Fe的相对原子质量为56)。下列有关分析错误的是
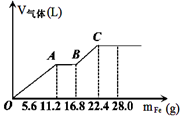

| A.原混合酸中NO3-的物质的量为0.2mol |
| B.原混合酸中H2SO4物质的量浓度为2mol/L |
| C.OA段与BC段反应中电子转移的物质的量之比为2:1 |
| D.取20mL原混合酸加水稀释至1L后溶液的pH=1 |
您最近一年使用:0次
2016-12-09更新
|
1163次组卷
|
5卷引用:上海市七校2013届3月联考化学试题
(已下线)上海市七校2013届3月联考化学试题(已下线)上海市建平七宝南模延安向明复兴上师大附中等七校2013届3月联考化学试题(已下线)2014届四川省绵阳中学高三上学期第三次月考理综化学试卷2017届江西省鹰潭一中高三上学期第二次月考化学试卷甘肃省兰州第一中学2018届高三上学期第二次月考(9月)化学试题
2013·上海普陀·二模
解题方法
8 . 实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:高温下使软锰矿与过量KOH(s)和KClO3(s)反应,生成K2MnO4(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,K2MnO4转化为MnO2和KMnO4;再滤去沉淀MnO2,浓缩结晶得到KMnO4晶体。
请回答:
(1)用软锰矿制备K2MnO4的化学方程式是_______________________________________ 。
(2)K2MnO4转化为KMnO4的反应中氧化剂和还原剂的物质的量之比为_____________ 。生成0.1mol还原产物时转移电子______________ 个。KMnO4、K2MnO4和MnO2的氧化性由强到弱的顺序是____________________________ 。
(3)KMnO4能与热的Na2C2O4(aq,硫酸酸化)反应生成Mn2+和CO2。若取用软锰矿制得的KMnO4产品0.165g,能与0.335g Na2C2O4恰好完全反应(假设杂质均不能参与反应),该产品中KMnO4的纯度为____________________ 。
请回答:
(1)用软锰矿制备K2MnO4的化学方程式是
(2)K2MnO4转化为KMnO4的反应中氧化剂和还原剂的物质的量之比为
(3)KMnO4能与热的Na2C2O4(aq,硫酸酸化)反应生成Mn2+和CO2。若取用软锰矿制得的KMnO4产品0.165g,能与0.335g Na2C2O4恰好完全反应(假设杂质均不能参与反应),该产品中KMnO4的纯度为
您最近一年使用:0次
13-14高三上·上海嘉定·期末
9 . (1)NA为阿伏加德罗常数。25℃时,1g水中含H+离子个数约为__________ NA。
(2)通过氨的催化氧化法制取硝酸,在此全过程中,理论上氨与所耗氧气的物质的量比为__________ ,这样所得硝酸的质量分数为_____________ 。
(3)往含0.2 mol NaOH和0.1 mol Ca(OH)2的混合溶液中持续稳定地通入CO2气体0.5 mol。请以CO2的量为横坐标,以溶液中离子的总量为横坐标,画出离子总量随CO2加入量变化的折线图。(不计弱电解质的电离和盐的水解)_____________

(4)某研究性学习小组拟用铜屑与氧化铜混合物与硫酸和硝酸组成的混酸反应来制取CuSO4·5H2O晶体,混酸中硝酸的还原产物为NO,反应过程中不产生SO2,反应后的溶液中不含Cu(NO3)2, 反应中固体完全溶解,两种酸均恰好完全反应。设固体混合物的总质量为480 g,其中铜屑的质量分数为0.4, 480g固体混合物与一定量混酸微热后,充分反应,冷却恰好只得到CuSO4·5H2O,试求原混酸中H2SO4的质量分数_____________ (写出计算过程)
(2)通过氨的催化氧化法制取硝酸,在此全过程中,理论上氨与所耗氧气的物质的量比为
(3)往含0.2 mol NaOH和0.1 mol Ca(OH)2的混合溶液中持续稳定地通入CO2气体0.5 mol。请以CO2的量为横坐标,以溶液中离子的总量为横坐标,画出离子总量随CO2加入量变化的折线图。(不计弱电解质的电离和盐的水解)

(4)某研究性学习小组拟用铜屑与氧化铜混合物与硫酸和硝酸组成的混酸反应来制取CuSO4·5H2O晶体,混酸中硝酸的还原产物为NO,反应过程中不产生SO2,反应后的溶液中不含Cu(NO3)2, 反应中固体完全溶解,两种酸均恰好完全反应。设固体混合物的总质量为480 g,其中铜屑的质量分数为0.4, 480g固体混合物与一定量混酸微热后,充分反应,冷却恰好只得到CuSO4·5H2O,试求原混酸中H2SO4的质量分数
您最近一年使用:0次
2013·上海闵行·三模
10 . 2013年初,雾霾天气多次肆虐我国中东部,该地区PM2.5严重超标。研究表明,PM2.5约60%来源于某些气体污染物在空气中转变而成的二次颗粒物。这些气体污染物主要有二氧化硫、氮氧化物、氨气、挥发性有机物。因此,控制、治理PM2.5污染源成为环保的重要课题。
(1)研究表明,TiO2在紫外线照射下会使空气中的某些分子产生活性基团OH,如图所示,OH与NO2的反应为NO2+OH HNO3。写出OH与NO反应的化学方程式:
HNO3。写出OH与NO反应的化学方程式:_____________ ,该反应中被氧化的元素是_______ 。

(2)如图所示的电解装置能吸收和转化NO2、NO和SO2。阴极排出的溶液中含S2O42-离子,能吸收NOx气体,生成的SO32-可在阴极区再生。请将S2O42-吸收NO2的离子方程式配平,并标明电子转移的方向和数目。
S2O42-+NO2+OH- SO32-+N2+
SO32-+N2+
____________ 。

(3)已知上述电解装置阳极反应为:SO2-2e-+2H2O SO42-+4H+,阴极生成的吸收液每吸收标准状况下7.84 L的气体,阳极区新生成质量分数为49%的硫酸100 g,则被吸收气体中NO2和NO的物质的量之比为
SO42-+4H+,阴极生成的吸收液每吸收标准状况下7.84 L的气体,阳极区新生成质量分数为49%的硫酸100 g,则被吸收气体中NO2和NO的物质的量之比为_____________ 。
(4)PM2.5产生的主要来源是日常发电、工业生产、汽车尾气排放等过程中经过燃烧而排放的残留物,大多含有重金属等有毒物质。一般而言,粒径2.5微米至10微米的粗颗粒物主要来自扬尘等;2.5微米以下的细颗粒物(PM2.5)则主要来自化石燃料的燃烧(如机动车尾气、燃煤)、挥发性有机物的排放等。请你结合信息,给出降低PM2.5排放的对策(至少两条):______________________ 。
(1)研究表明,TiO2在紫外线照射下会使空气中的某些分子产生活性基团OH,如图所示,OH与NO2的反应为NO2+OH
 HNO3。写出OH与NO反应的化学方程式:
HNO3。写出OH与NO反应的化学方程式:
(2)如图所示的电解装置能吸收和转化NO2、NO和SO2。阴极排出的溶液中含S2O42-离子,能吸收NOx气体,生成的SO32-可在阴极区再生。请将S2O42-吸收NO2的离子方程式配平,并标明电子转移的方向和数目。
S2O42-+NO2+OH-
 SO32-+N2+
SO32-+N2+

(3)已知上述电解装置阳极反应为:SO2-2e-+2H2O
 SO42-+4H+,阴极生成的吸收液每吸收标准状况下7.84 L的气体,阳极区新生成质量分数为49%的硫酸100 g,则被吸收气体中NO2和NO的物质的量之比为
SO42-+4H+,阴极生成的吸收液每吸收标准状况下7.84 L的气体,阳极区新生成质量分数为49%的硫酸100 g,则被吸收气体中NO2和NO的物质的量之比为(4)PM2.5产生的主要来源是日常发电、工业生产、汽车尾气排放等过程中经过燃烧而排放的残留物,大多含有重金属等有毒物质。一般而言,粒径2.5微米至10微米的粗颗粒物主要来自扬尘等;2.5微米以下的细颗粒物(PM2.5)则主要来自化石燃料的燃烧(如机动车尾气、燃煤)、挥发性有机物的排放等。请你结合信息,给出降低PM2.5排放的对策(至少两条):
您最近一年使用:0次



