名校
1 .  气体与足量
气体与足量 溶液完全反应后,再加入
溶液完全反应后,再加入 溶液,发生如下反应:①
溶液,发生如下反应:①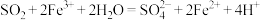 ;②
;② 。下列说法正确的是
。下列说法正确的是
 气体与足量
气体与足量 溶液完全反应后,再加入
溶液完全反应后,再加入 溶液,发生如下反应:①
溶液,发生如下反应:①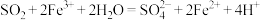 ;②
;② 。下列说法正确的是
。下列说法正确的是A.氧化性: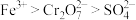 |
B.若有6.72L 完全反应,最终消耗0.2mol 完全反应,最终消耗0.2mol |
C.反应①中被还原的物质是 |
D.反应②中,1mol 参加反应,转移电子的数目为 参加反应,转移电子的数目为 |
您最近一年使用:0次
2024-02-03更新
|
164次组卷
|
3卷引用:四川省绵阳南山中学2023-2024学年高一下学期入学考试化学试题
2 . 在歌曲《青花瓷》中唱到“帘外芭蕉惹骤雨,门环惹铜绿”,其中“铜绿”的化学成分是碱式碳酸铜。铜在潮湿的空气中生锈的化学反应:2Cu + O2 + CO2 + H2O = Cu2(OH)2CO3。下列有关该反应说法正确的是
| A.该反应是氧化还原反应,发生化合价变化的有三种元素 |
| B.12.8 g Cu参与反应转移0.4 mol e- |
| C.由此反应可知,化合反应一定是氧化还原反应 |
| D.O2 得电子,发生的是氧化反应 |
您最近一年使用:0次
3 . 反应 3BrF3+5H2O=9HF+Br2+HBrO3+O2 ↑,下列说法中正确的是
| A.BrF3仅作氧化剂,H2O仅作还原剂 |
| B.还原剂与氧化剂的物质的量之比为3∶2 |
| C.若生成3.2 g O2,则反应中转移电子的物质的量为0.4 mol |
| D.若有 15 mol H2O 参加反应,被水还原的 BrF3的物质的量为8 mol |
您最近一年使用:0次
2024-02-02更新
|
192次组卷
|
2卷引用:四川省眉山市彭山区第一中学2023-2024学年高一上学期12月月考化学试题
名校
4 . 1.12g铜镁合金完全溶解于50mL63%的浓硝酸(密度为 )中,得到
)中,得到 和
和 的混合气体1120mL(换算为标准状况),(忽略反应前后溶液体积变化)。向反应后的溶液中逐滴加入
的混合气体1120mL(换算为标准状况),(忽略反应前后溶液体积变化)。向反应后的溶液中逐滴加入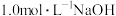 溶液,当金属离子刚好全部沉淀,得到2.14g沉淀。下列说法正确的是
溶液,当金属离子刚好全部沉淀,得到2.14g沉淀。下列说法正确的是
 )中,得到
)中,得到 和
和 的混合气体1120mL(换算为标准状况),(忽略反应前后溶液体积变化)。向反应后的溶液中逐滴加入
的混合气体1120mL(换算为标准状况),(忽略反应前后溶液体积变化)。向反应后的溶液中逐滴加入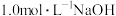 溶液,当金属离子刚好全部沉淀,得到2.14g沉淀。下列说法正确的是
溶液,当金属离子刚好全部沉淀,得到2.14g沉淀。下列说法正确的是A.该合金中 |
B.合金完全溶解时,溶液中 |
C.刚好得到2.14g沉淀时,加入 溶液的体积是640mL 溶液的体积是640mL |
D. 和 和 的混合气体中, 的混合气体中, 的体积分数是20% 的体积分数是20% |
您最近一年使用:0次
2024-02-02更新
|
889次组卷
|
3卷引用:四川省眉山市仁寿第一中学校(北校区)2023-2024学年高一下学期3月月考化学试题
名校
5 . Ⅰ.下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用相应化学用语回答下列问题:

(1)表中形成化合物种类最多的元素在周期表中的位置___________ ;写出它与原子半径最小的原子形成10电子且为正四面体结构的化合物的电子式___________ ,用电子式表示⑤和⑧形成化合物的过程___________ 。
(2)④⑤⑧形成的简单离子半径由大到小的顺序为___________ (填离子符号);③⑦⑨的最高价氧化物对应水化物的酸性由强到弱的顺序为___________ (填化学式)。
(3)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是___________ (填化学式),写出它与⑤的最高价氧化物对应水化物发生反应的离子方程式:___________ 。
(4)有两种化合物A和 都由①④⑤⑧四种元素组成。若A与
都由①④⑤⑧四种元素组成。若A与 在水溶液中能发生离子反应,则该反应的离子方程式为
在水溶液中能发生离子反应,则该反应的离子方程式为 ___________ 。
Ⅱ.铁的化学性质比较活泼,常温下铁可以与稀硝酸发生反应,反应的化学方程式为 。
。
(5)反应中氧化剂与还原剂的物质的量之比为___________ ,其中HNO3反应中显示出来的性质是___________ ,每生成11.2L(标准状况下)的NO,转移的电子数为___________ 。

(1)表中形成化合物种类最多的元素在周期表中的位置
(2)④⑤⑧形成的简单离子半径由大到小的顺序为
(3)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是
(4)有两种化合物A和
 都由①④⑤⑧四种元素组成。若A与
都由①④⑤⑧四种元素组成。若A与 在水溶液中能发生离子反应,则该反应的离子方程式为
在水溶液中能发生离子反应,则该反应的离子方程式为 Ⅱ.铁的化学性质比较活泼,常温下铁可以与稀硝酸发生反应,反应的化学方程式为
 。
。(5)反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
名校
6 . 水体中氨氮含量超标会造成水体富营养化,从而破坏水体生态平衡,导致水生生物的稳定性和多样性遭到破坏。用次氯酸钠除去水体中氨氮的原理如图所示。下列说法错误的是
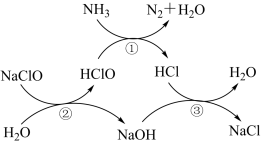

A.去除过程中,只有第①步反应是氧化还原反应,且 (氧化剂): (氧化剂): (还原剂)=3:2 (还原剂)=3:2 |
B.每生成 ,转移 ,转移 电子 电子 |
C. 投入过多,总氮去除率可能会降低 投入过多,总氮去除率可能会降低 |
D.去除过程的总反应方程式为: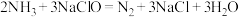 |
您最近一年使用:0次
名校
7 .  是实验室中一种常见的化学试剂,也是生产生活中常用的净水剂。
是实验室中一种常见的化学试剂,也是生产生活中常用的净水剂。 熔点为306℃,沸点为315℃,易吸收空气中的水分而潮解。巴中中学某化学兴趣设计以下装置,制备
熔点为306℃,沸点为315℃,易吸收空气中的水分而潮解。巴中中学某化学兴趣设计以下装置,制备 。
。
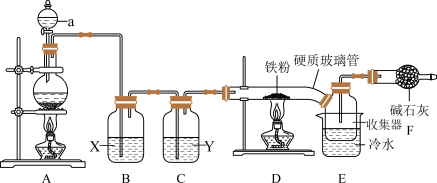
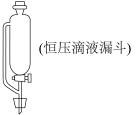
回答下列问题:
(1)A中发生的化学反应方程式是___________ 。为使实验顺利进行,可将仪器a更换为恒压滴液漏斗(如上图),更换后优点是___________ 。
(2)试剂“X”是___________ ,其作用是___________ 。
(3)硬质玻璃管直接连接收集器的优点___________ 。
(4)实验开始时,应先点燃A处酒精灯,当___________ 时,再点燃D处酒精灯。
(5)装置F作用是吸收多余氯气和___________ ,氯气和碱石灰反应时,若有0.71g氯气被氧化成次氯酸盐,1.42g氯气被氧化成氯酸盐,则被还原的氯原子的物质的量为___________ 。
 是实验室中一种常见的化学试剂,也是生产生活中常用的净水剂。
是实验室中一种常见的化学试剂,也是生产生活中常用的净水剂。 熔点为306℃,沸点为315℃,易吸收空气中的水分而潮解。巴中中学某化学兴趣设计以下装置,制备
熔点为306℃,沸点为315℃,易吸收空气中的水分而潮解。巴中中学某化学兴趣设计以下装置,制备 。
。

回答下列问题:
(1)A中发生的化学反应方程式是
(2)试剂“X”是
(3)硬质玻璃管直接连接收集器的优点
(4)实验开始时,应先点燃A处酒精灯,当
(5)装置F作用是吸收多余氯气和
您最近一年使用:0次
名校
解题方法
8 . 某工厂的工业废水中含有大量的 和较多的
和较多的 。为了减少污染并变废为宝,工厂计划从该废水中回收
。为了减少污染并变废为宝,工厂计划从该废水中回收 和金属铜。请根据以下流程图,回答下列问题:
和金属铜。请根据以下流程图,回答下列问题:

(1)操作a的名称为___________ 。
(2)②中物质为___________ ,试剂④为___________ ,鉴别溶液⑥中的金属阳离子时,应滴加的试剂依次是___________ ,请写出该鉴别过程中属于氧化还原反应的离子方程式___________ 。将FeSO4·7H2O溶于水配成溶液,并向该溶液中滴入稀H2SO4酸化的H2O2溶液,观察到溶液由浅绿色变成棕黄色,请写出该反应的离子方程式___________ 。
(3)若取2mL溶液⑥加入试管中,然后滴加氢氧化钠溶液,产生的现象是___________ 。
(4)工业上常用绿矾( )处理工业废水中有毒的重铬酸根离子(
)处理工业废水中有毒的重铬酸根离子( )。反应的离子方程式为
)。反应的离子方程式为 。该反应中
。该反应中___________ 是还原剂(填离子符号);若消耗 ,则转移电子的物质的量为
,则转移电子的物质的量为___________ 。
 和较多的
和较多的 。为了减少污染并变废为宝,工厂计划从该废水中回收
。为了减少污染并变废为宝,工厂计划从该废水中回收 和金属铜。请根据以下流程图,回答下列问题:
和金属铜。请根据以下流程图,回答下列问题:
(1)操作a的名称为
(2)②中物质为
(3)若取2mL溶液⑥加入试管中,然后滴加氢氧化钠溶液,产生的现象是
(4)工业上常用绿矾(
 )处理工业废水中有毒的重铬酸根离子(
)处理工业废水中有毒的重铬酸根离子( )。反应的离子方程式为
)。反应的离子方程式为 。该反应中
。该反应中 ,则转移电子的物质的量为
,则转移电子的物质的量为
您最近一年使用:0次
名校
9 . 设 表示阿伏加德罗常数的值。下列叙述正确的是
表示阿伏加德罗常数的值。下列叙述正确的是
 表示阿伏加德罗常数的值。下列叙述正确的是
表示阿伏加德罗常数的值。下列叙述正确的是| A.足量的MnO2与4mol浓盐酸加热充分反应,转移的电子数为2NA |
B.在常温常压下,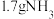 含有的原子数为 含有的原子数为 |
| C.18 g D2O所含的中子数为10NA |
| D.标准状况下,11.2L氦气含有的原子数为NA |
您最近一年使用:0次
名校
10 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.1mol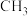 中所含电子数为 中所含电子数为 |
B.标准状况下,11.2LNO与11.2L 混合后的分子数目为 混合后的分子数目为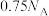 |
C.1.2gMg在空气中完全燃烧转移电子数为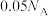 |
D.7.2g 和CaS的混合物中,含有的阴阳离子总数为 和CaS的混合物中,含有的阴阳离子总数为 |
您最近一年使用:0次



