名校
解题方法
1 . 某稀溶液中含有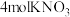 和
和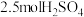 ,向其中加入
,向其中加入 ,充分反应(已知
,充分反应(已知 被还原为NO),最终溶液体积为1L。下列说法正确的是
被还原为NO),最终溶液体积为1L。下列说法正确的是
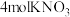 和
和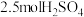 ,向其中加入
,向其中加入 ,充分反应(已知
,充分反应(已知 被还原为NO),最终溶液体积为1L。下列说法正确的是
被还原为NO),最终溶液体积为1L。下列说法正确的是A.所得溶液中的溶质只有 |
B.所得溶液中 |
| C.反应后生成NO的体积为33.6L(标准状况下) |
D.所得溶液中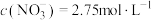 |
您最近一年使用:0次
2024-04-03更新
|
106次组卷
|
3卷引用:四川省射洪中学校2023-2024学年高一下学期4月第一次月考化学试题
2 . 氧化还原反应在生产生活中有很多实际应用。
I.高铁酸钾( )是一种新型绿色消毒剂,具有强氧化性,常用于处理饮用水。工业上有干法与湿法两种制备高铁酸钾的方法。
)是一种新型绿色消毒剂,具有强氧化性,常用于处理饮用水。工业上有干法与湿法两种制备高铁酸钾的方法。
(1)干法制备高铁酸钾时,先制备得到 ,反应为:
,反应为: ,该反应的氧化产物是
,该反应的氧化产物是___________ ;每生成 转移电子数目为
转移电子数目为___________ 。
(2)湿法制备高铁酸钾( )的反应体系中有六种数粒:
)的反应体系中有六种数粒: 、
、 、
、 、
、 、
、 、
、 写出并配平湿法制高铁酸钾的离子反应方程式并用单线桥表示出电子转移的方向和数目:
写出并配平湿法制高铁酸钾的离子反应方程式并用单线桥表示出电子转移的方向和数目:___________ 。
(3)低温下,在高铁酸钠溶液中加入KOH至饱和也可制得高铁酸钾( )固体,请解释其原因
)固体,请解释其原因___________ 。
(4)高铁酸钾能用于处理饮用水的原因?___________ 、___________ 。
Ⅱ.对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(5)含氰废水中的 有剧毒。在微生物的作用下,
有剧毒。在微生物的作用下, 能被氧气氧化成
能被氧气氧化成 同时生成
同时生成 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(6)试分析 反应中,被
反应中,被 氧化的P的物质的量为
氧化的P的物质的量为___________ 。
I.高铁酸钾(
 )是一种新型绿色消毒剂,具有强氧化性,常用于处理饮用水。工业上有干法与湿法两种制备高铁酸钾的方法。
)是一种新型绿色消毒剂,具有强氧化性,常用于处理饮用水。工业上有干法与湿法两种制备高铁酸钾的方法。(1)干法制备高铁酸钾时,先制备得到
 ,反应为:
,反应为: ,该反应的氧化产物是
,该反应的氧化产物是 转移电子数目为
转移电子数目为(2)湿法制备高铁酸钾(
 )的反应体系中有六种数粒:
)的反应体系中有六种数粒: 、
、 、
、 、
、 、
、 、
、 写出并配平湿法制高铁酸钾的离子反应方程式并用单线桥表示出电子转移的方向和数目:
写出并配平湿法制高铁酸钾的离子反应方程式并用单线桥表示出电子转移的方向和数目:(3)低温下,在高铁酸钠溶液中加入KOH至饱和也可制得高铁酸钾(
 )固体,请解释其原因
)固体,请解释其原因(4)高铁酸钾能用于处理饮用水的原因?
Ⅱ.对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(5)含氰废水中的
 有剧毒。在微生物的作用下,
有剧毒。在微生物的作用下, 能被氧气氧化成
能被氧气氧化成 同时生成
同时生成 ,该反应的离子方程式为
,该反应的离子方程式为(6)试分析
 反应中,被
反应中,被 氧化的P的物质的量为
氧化的P的物质的量为
您最近一年使用:0次
解题方法
3 . T、X、Y、Z、W五种短周期元素在周期表中的位置关系如图所示。
已知Z元素原子的最外层电子数是电子层数的2倍。
(1) 和
和 元素形成的常见化合物的化学式
元素形成的常见化合物的化学式___________
(2)元素T在元素周期表中的位置是___________
(3)X的简单氢化物的电子式为___________
(4)某同学为了比较碳元素和硅元素非金属性的强弱,用如图所示装置进行实验:

①M为___________ (填化学式),
②Na2SiO3溶液中发生反应的离子方程式___________ 。
(5) 的最高价氧化物对应水化物的浓溶液不稳定,受热可分解,分解产物中有2种气体单质,
的最高价氧化物对应水化物的浓溶液不稳定,受热可分解,分解产物中有2种气体单质,
其中一种是黄绿色,且当有28mol电子转移时,共产生2mol黄绿色气体,则该反应的化学方程式为___________ 。
| T | X | Y | |
| Z | W |
(1)
 和
和 元素形成的常见化合物的化学式
元素形成的常见化合物的化学式(2)元素T在元素周期表中的位置是
(3)X的简单氢化物的电子式为
(4)某同学为了比较碳元素和硅元素非金属性的强弱,用如图所示装置进行实验:

①M为
②Na2SiO3溶液中发生反应的离子方程式
(5)
 的最高价氧化物对应水化物的浓溶液不稳定,受热可分解,分解产物中有2种气体单质,
的最高价氧化物对应水化物的浓溶液不稳定,受热可分解,分解产物中有2种气体单质,其中一种是黄绿色,且当有28mol电子转移时,共产生2mol黄绿色气体,则该反应的化学方程式为
您最近一年使用:0次
4 . 将18g由A1、Fe、Cu组成的合金投入到足量的NaOH溶液中,充分反应后产生的3.36L气体(标准状况下)。另取等质量的合金溶于过量的稀硝酸中,向反应后的溶液中加入过量的NaOH溶液,得到沉淀的质量为25.5g。若HNO3的还原产物只有NO,则合金与稀硝酸反应生成的NO在标准状况下的体积为
| A.2.24L | B.3.36L | C.4.48L | D.6.72L |
您最近一年使用:0次
5 . 已知水煤气反应: ,
, 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 ,
, 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是| A.所得混合气体产物的平均摩尔质量为15g |
B.若反应得到2g  ,则生成的CO体积为22.4L ,则生成的CO体积为22.4L |
C.每消耗18g  ,反应转移电子数为 ,反应转移电子数为 |
D.当断裂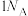 极性共价键时反应生成 极性共价键时反应生成 |
您最近一年使用:0次
2024-04-01更新
|
220次组卷
|
2卷引用:2024届四川省雅安市、遂宁市、眉山市高三第二次诊断性考试理科综合试题-高中化学
名校
6 .  为阿伏加德罗常数,下列说法正确的是
为阿伏加德罗常数,下列说法正确的是
 为阿伏加德罗常数,下列说法正确的是
为阿伏加德罗常数,下列说法正确的是A.标准状况下,22.4L己烷中含有碳碳单键数目大于 |
B.60g二氧化硅晶体中含有Si-O键数为 |
C.将2.3gNa与氧气完全反应,反应中转移的电子数介于 到 到 之间 之间 |
D.2mL0.5mol/L硅酸钠溶液中滴入盐酸制硅酸胶体,所得胶粒数目为 |
您最近一年使用:0次
解题方法
7 .  是光电转化材料。利用钛铁矿(主要成分为
是光电转化材料。利用钛铁矿(主要成分为 ,还含有少量
,还含有少量 等杂质)来制备
等杂质)来制备 ,并回收铁制备难溶于水的黄钾铁矾
,并回收铁制备难溶于水的黄钾铁矾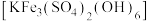 ,制备流程如图,回答下列问题:
,制备流程如图,回答下列问题:
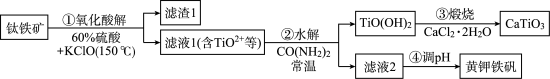
部分原料价格表:
(1) 中Ti的化合价为
中Ti的化合价为_______ 。
(2)步骤①滤渣1的主要成分是_______ ,若氧化酸解的氧化剂用 替代
替代 ,则理论上氧化剂与还原剂物质的量之比为
,则理论上氧化剂与还原剂物质的量之比为_______ ,相同条件下,用 做氧化剂时,其酸解效率较
做氧化剂时,其酸解效率较 低,原因可能是
低,原因可能是_______ 。
(3)已知 在水中能部分水解并有
在水中能部分水解并有 生成,则相关离子方程式为
生成,则相关离子方程式为_______ ;常温下,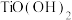
 为
为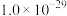 ,滤液1中
,滤液1中 浓度为
浓度为 ,步骤②中要使
,步骤②中要使 水解的转化率达99%,加
水解的转化率达99%,加 时忽略溶液体积变化,则此时溶液的pH应为
时忽略溶液体积变化,则此时溶液的pH应为_______ 。
(4)步骤③反应的化学方程式为_______ ,若在实验室煅烧,用到的实验仪器除了玻璃棒、酒精灯、三脚架及泥三角外,还需要_______ 。
(5)结合信息分析,步骤④调pH最适宜的试剂是_______。
 是光电转化材料。利用钛铁矿(主要成分为
是光电转化材料。利用钛铁矿(主要成分为 ,还含有少量
,还含有少量 等杂质)来制备
等杂质)来制备 ,并回收铁制备难溶于水的黄钾铁矾
,并回收铁制备难溶于水的黄钾铁矾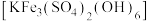 ,制备流程如图,回答下列问题:
,制备流程如图,回答下列问题:
部分原料价格表:
| 物质 | 纯碱(99% ) ) | 氢氧化钾(90% ) ) | 碳酸钾(99% ) ) | 液氨(99.9%) |
| 价格(元/吨) | 1800 | 4000 | 4500 | 25000 |
 中Ti的化合价为
中Ti的化合价为(2)步骤①滤渣1的主要成分是
 替代
替代 ,则理论上氧化剂与还原剂物质的量之比为
,则理论上氧化剂与还原剂物质的量之比为 做氧化剂时,其酸解效率较
做氧化剂时,其酸解效率较 低,原因可能是
低,原因可能是(3)已知
 在水中能部分水解并有
在水中能部分水解并有 生成,则相关离子方程式为
生成,则相关离子方程式为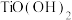
 为
为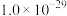 ,滤液1中
,滤液1中 浓度为
浓度为 ,步骤②中要使
,步骤②中要使 水解的转化率达99%,加
水解的转化率达99%,加 时忽略溶液体积变化,则此时溶液的pH应为
时忽略溶液体积变化,则此时溶液的pH应为(4)步骤③反应的化学方程式为
(5)结合信息分析,步骤④调pH最适宜的试剂是_______。
A. | B. | C. | D. |
您最近一年使用:0次
2024-03-28更新
|
111次组卷
|
3卷引用:2024届四川省雅安市高三上学期第一次诊断性考试理综试题
8 . 已知离子反应: (已配平),下列说法错误的是
(已配平),下列说法错误的是
A. 是 是 | B. 是还原产物 是还原产物 |
C.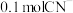 反应,转移的电子数目为 反应,转移的电子数目为 | D.该反应中 体现氧化性 体现氧化性 |
您最近一年使用:0次
9 . “碳中和”已作为一种新型环保形式,CH4和CO2的催化重整可以缓解一部分环保压力。反应为CH4+CO2 2CO+2H2,下列说法错误的是
2CO+2H2,下列说法错误的是
 2CO+2H2,下列说法错误的是
2CO+2H2,下列说法错误的是| A.生成2molH2时,转移6NA电子 | B.CH4的摩尔质量为16g |
| C.CH4既是氧化剂,又是还原剂 | D.该反应既可以缓解温室效应,又能提供燃料 |
您最近一年使用:0次
10 .  在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与
在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与 反应,其化学方程式是
反应,其化学方程式是 。已知:稀
。已知:稀 溶液几乎无色。
溶液几乎无色。
(1)X的化学式是___________ 。
(2)用双线桥法标出,上述反应中电子转移的方向和数目___________ 。
(3)上述反应中的还原剂为___________ (填化学式),被还原的元素是___________ (填元素符号)。
(4)向酸性 溶液中滴入过量双氧水,观察到的现象是
溶液中滴入过量双氧水,观察到的现象是___________ ,反应后溶液的pH___________ (填“增大”“减小”或“不变”)。
(5)0.2mol 参加上述反应,转移电子
参加上述反应,转移电子___________ mol。
 在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与
在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与 反应,其化学方程式是
反应,其化学方程式是 。已知:稀
。已知:稀 溶液几乎无色。
溶液几乎无色。(1)X的化学式是
(2)用双线桥法标出,上述反应中电子转移的方向和数目
(3)上述反应中的还原剂为
(4)向酸性
 溶液中滴入过量双氧水,观察到的现象是
溶液中滴入过量双氧水,观察到的现象是(5)0.2mol
 参加上述反应,转移电子
参加上述反应,转移电子
您最近一年使用:0次



