名校
1 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.1 mol·L-1 Na2SO4溶液中含钠离子的数目为2NA |
| B.标准状况下,22.4 L盐酸中含有NA个HCl分子 |
| C.1 mol Na被完全氧化生成Na2O2,失去2NA个电子 |
| D.常温常压下,8 g O2含有4NA个电子 |
您最近一年使用:0次
解题方法
2 . 根据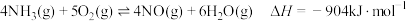 ,下列说法
,下列说法不正确 的是
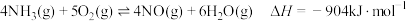 ,下列说法
,下列说法A.反应的 |
B.有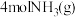 和 和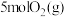 在反应器中充分反应,能放出 在反应器中充分反应,能放出 热量 热量 |
C.断裂1mol 键的同时,断裂 键的同时,断裂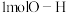 键,说明该反应达到平衡状态 键,说明该反应达到平衡状态 |
D.每消耗 转移电子的数目约为 转移电子的数目约为 |
您最近一年使用:0次
名校
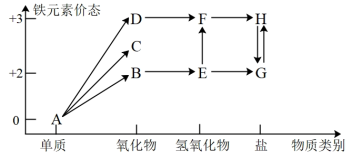
3 . 铁是人类较早使用的金属之一,下图为铁元素的价类二维图,其中的箭头表示部分物质间的转化关系。运用铁及其化合物的知识,回答下列问题。_______ ;E→F反应的化学方程式是_______ ,该反应过程的现象为_______ 。
(2)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,高铁酸钾作为自来水处理剂的优点_______ ;湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O,写出并配平该法制备高铁酸钾的离子反应方程式
、Cl-、H2O,写出并配平该法制备高铁酸钾的离子反应方程式_______ 。
(3)将FeCl3饱和溶液滴入沸水中,继续煮沸至液体呈_______ ,制得分散系为_______ ,它与FeCl3溶液、Fe(OH)3浊液的本质区别是_______ 。
(4)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路请写出FeCl3溶液与铜反应的离子方程式:_______ 。
(5)城市饮用水处理新技术用NaClO2、高铁酸钠代替Cl2,如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么NaClO2、Na2FeO4、Cl2的消毒效率由大到小的顺序是_______ 。
(2)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,高铁酸钾作为自来水处理剂的优点
 、Cl-、H2O,写出并配平该法制备高铁酸钾的离子反应方程式
、Cl-、H2O,写出并配平该法制备高铁酸钾的离子反应方程式(3)将FeCl3饱和溶液滴入沸水中,继续煮沸至液体呈
(4)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路请写出FeCl3溶液与铜反应的离子方程式:
(5)城市饮用水处理新技术用NaClO2、高铁酸钠代替Cl2,如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么NaClO2、Na2FeO4、Cl2的消毒效率由大到小的顺序是
您最近一年使用:0次
名校
解题方法
4 . 在500mL硫酸铁、硫酸铜的混合液中,金属阳离子的浓度均为 ,现加入amol铁粉,充分振荡反应后,下列说法不正确的是
,现加入amol铁粉,充分振荡反应后,下列说法不正确的是
 ,现加入amol铁粉,充分振荡反应后,下列说法不正确的是
,现加入amol铁粉,充分振荡反应后,下列说法不正确的是A.当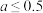 时,发生的反应为 时,发生的反应为 |
B.当 时,发生的反应为 时,发生的反应为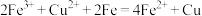 |
C.当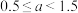 时,溶液中 时,溶液中 、 、 、 、 的物质的量之比为(1.5-a):(1+a):5 的物质的量之比为(1.5-a):(1+a):5 |
| D.当加入a为2.0时,此时反应中电子转移数目等于3NA |
您最近一年使用:0次
5 . 丙烯腈(C3H3N)是制备腈纶的单体。一种制备丙烯腈反应的热化学方程式为C3H6(g)+NH3(g)+ O2(g)=C3H3N(g)+3H2O(g)
O2(g)=C3H3N(g)+3H2O(g)  H<0,下列说法正确的是
H<0,下列说法正确的是
 O2(g)=C3H3N(g)+3H2O(g)
O2(g)=C3H3N(g)+3H2O(g)  H<0,下列说法正确的是
H<0,下列说法正确的是| A.该反应只有在低温下才能自发进行 |
B.该反应的平衡常数K= |
| C.该反应每消耗1molC3H6,转移电子的物质的量为6mol |
| D.其他条件相同,减压和升温均有利于提高丙烯腊的平衡产率 |
您最近一年使用:0次
名校
6 . 氧化还原反应在日常生活中有着广泛的应用,下列有关化学用语和相关说法均正确的是
选项 | 化学反应方程式 | 相关说法 |
A |
|  是氧化产物, 是氧化产物, 既是氧化剂又是还原剂 既是氧化剂又是还原剂 |
B |
| 均为单质被还原的置换反应 |
C |
| 每生成1mol |
D |
| 氧化性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 如图是乙烯催化氧化的过程(部分配平相关离子未画出),下列描述错误的是
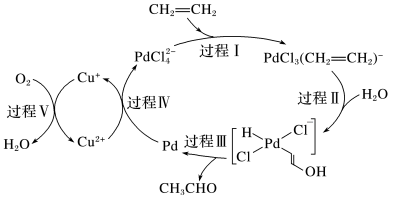
| A.“过程Ⅰ”中涉及到非极性键的断裂 |
B.反应过程中部分碳原子杂化类型由 |
C. 分子中 分子中 键与 键与 键数目之比为6:1 键数目之比为6:1 |
| D.“过程V”中消耗的氧化剂与还原剂物质的量之比为1:4 |
您最近一年使用:0次
解题方法
8 . 已知30mL浓度为0.5 的Na2SO3溶液恰好与50mL浓度为0.1
的Na2SO3溶液恰好与50mL浓度为0.1 的KRO4溶液完全反应转化为
的KRO4溶液完全反应转化为 ,则R元素在产物中的化合价是
,则R元素在产物中的化合价是
 的Na2SO3溶液恰好与50mL浓度为0.1
的Na2SO3溶液恰好与50mL浓度为0.1 的KRO4溶液完全反应转化为
的KRO4溶液完全反应转化为 ,则R元素在产物中的化合价是
,则R元素在产物中的化合价是| A.-1 | B.0 | C.+1 | D.+2 |
您最近一年使用:0次
解题方法
9 . 对于反应:2Na2O2+2CO2=2Na2CO3+O2↑,下列说法正确的是
| A.Na2O2是氧化剂,CO2是还原剂 |
| B.该反应中电子转移的数目为4e- |
| C.Na2O2既是氧化剂,又是还原剂 |
| D.每有44gCO2与足量Na2O2反应,则固体增重56g |
您最近一年使用:0次
解题方法
10 . 在反应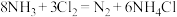 中,氧化剂和还原剂的物质的量之比为
中,氧化剂和还原剂的物质的量之比为
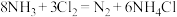 中,氧化剂和还原剂的物质的量之比为
中,氧化剂和还原剂的物质的量之比为A.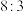 | B. | C.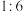 | D. |
您最近一年使用:0次


 ,
,
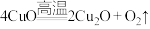
 个电子
个电子