名校
解题方法
1 . 铁是一种重要的金属材料,它的单质及化合物在生产生活中应用广泛。
(1)某补铁口服液中含有 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加___________ ,若变为红色,则说明其已变质。
(2)工业盐的主要成分是 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力。以上事实说明
结合的能力。以上事实说明 具有
具有___________ 。下列不能实现 转化为
转化为 的物质是
的物质是___________ (填字母)。
A. B.
B. C.
C. D.
D.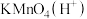
(3) 常用作杀菌消毒剂,生产
常用作杀菌消毒剂,生产 的反应原理是:
的反应原理是: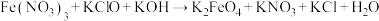 (未配平),则该反应中氧化剂与还原剂的物质的量之比为
(未配平),则该反应中氧化剂与还原剂的物质的量之比为___________ 。
(4)从制造印刷电路板的废液中回收铜,并重新获得 溶液的工艺流程如下,某工程师为了从使用过的腐蚀废液中回收铜,并重新获得
溶液的工艺流程如下,某工程师为了从使用过的腐蚀废液中回收铜,并重新获得 溶液,准备采用下列步骤:
溶液,准备采用下列步骤:
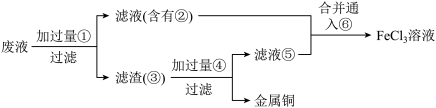
请写出上述流程中加入物质④的化学式:___________ 。请写出通入⑥反应的离子方程式___________ 。
(5)实验室由 固体配制
固体配制 溶液。
溶液。
①如下图所示的仪器中配制溶液不需使用的是___________ (填字母),还缺少的玻璃仪器是___________ (填写仪器名称)。
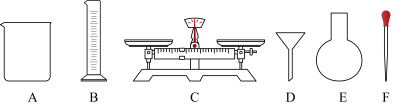
②若实验遇下列情况,导致所配溶液的物质的量浓度偏低的是___________ (填字母)。
A.定容时仰视刻度线 B. 固体失去部分结晶水
固体失去部分结晶水
C.移液前,容量瓶内有蒸馏水 D.未冷却至室温就转移定容
(1)某补铁口服液中含有
 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加(2)工业盐的主要成分是
 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力。以上事实说明
结合的能力。以上事实说明 具有
具有 转化为
转化为 的物质是
的物质是A.
 B.
B. C.
C. D.
D.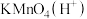
(3)
 常用作杀菌消毒剂,生产
常用作杀菌消毒剂,生产 的反应原理是:
的反应原理是: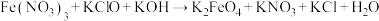 (未配平),则该反应中氧化剂与还原剂的物质的量之比为
(未配平),则该反应中氧化剂与还原剂的物质的量之比为(4)从制造印刷电路板的废液中回收铜,并重新获得
 溶液的工艺流程如下,某工程师为了从使用过的腐蚀废液中回收铜,并重新获得
溶液的工艺流程如下,某工程师为了从使用过的腐蚀废液中回收铜,并重新获得 溶液,准备采用下列步骤:
溶液,准备采用下列步骤:
请写出上述流程中加入物质④的化学式:
(5)实验室由
 固体配制
固体配制 溶液。
溶液。①如下图所示的仪器中配制溶液不需使用的是

②若实验遇下列情况,导致所配溶液的物质的量浓度偏低的是
A.定容时仰视刻度线 B.
 固体失去部分结晶水
固体失去部分结晶水C.移液前,容量瓶内有蒸馏水 D.未冷却至室温就转移定容
您最近一年使用:0次
名校
2 . 下列鉴别或检验方法能达到实验目的的是
A.用 溶液鉴别 溶液鉴别 与 与 | B.用焰色试验鉴别KCl和KOH |
C.用NaOH溶液鉴别碘水和 溶液 溶液 | D.用稀盐酸和澄清石灰水证明溶液中含有 |
您最近一年使用:0次
名校
解题方法
3 . 用 溶液刻蚀铜电路板,对刻蚀后的液体(含
溶液刻蚀铜电路板,对刻蚀后的液体(含 、
、 和
和 )进行处理以提取
)进行处理以提取 和
和 ,流程如图所示:
,流程如图所示:
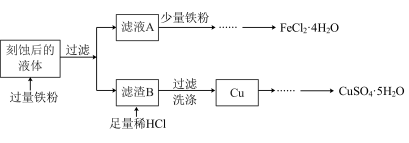
回答下列问题:
(1)氯化铁溶液刻蚀铜电路板的离子方程式为_______ ,过氧化氢和盐酸的混合溶液也可以刻蚀铜电路板,反应的化学方程式为_______ 。
(2)取少量滤液 ,滴入
,滴入 溶液,其现象:生成的白色絮状沉淀迅速变成灰绿色,最终生成
溶液,其现象:生成的白色絮状沉淀迅速变成灰绿色,最终生成_______ 沉淀。白色沉淀转化过程对应的化学方程式为_______ 。
(3)检验刻蚀后液体中 通常选用的试剂为
通常选用的试剂为_______ ,滤渣 的主要成分为
的主要成分为_______ 。
(4)检验滤渣 中提取出的
中提取出的 已经洗净的操作为
已经洗净的操作为_______ 。
 溶液刻蚀铜电路板,对刻蚀后的液体(含
溶液刻蚀铜电路板,对刻蚀后的液体(含 、
、 和
和 )进行处理以提取
)进行处理以提取 和
和 ,流程如图所示:
,流程如图所示:
回答下列问题:
(1)氯化铁溶液刻蚀铜电路板的离子方程式为
(2)取少量滤液
 ,滴入
,滴入 溶液,其现象:生成的白色絮状沉淀迅速变成灰绿色,最终生成
溶液,其现象:生成的白色絮状沉淀迅速变成灰绿色,最终生成(3)检验刻蚀后液体中
 通常选用的试剂为
通常选用的试剂为 的主要成分为
的主要成分为(4)检验滤渣
 中提取出的
中提取出的 已经洗净的操作为
已经洗净的操作为
您最近一年使用:0次
23-24高三下·湖南·阶段练习
名校
4 . 由硫铁矿烧渣(主要成分为 、
、 、
、 和
和 )得到绿矾
)得到绿矾 ,然后制取透明氧化铁颜料的流程如下:
,然后制取透明氧化铁颜料的流程如下: ),难溶于水;②“还原”时,
),难溶于水;②“还原”时, 能将
能将 中的硫元素氧化为+6价。
中的硫元素氧化为+6价。
回答下列问题:
(1)“滤渣”中的主要成分有过量的 和
和___________ (填化学式)。
(2)“还原”过程中涉及的离子方程式为___________ 。
(3)流程中“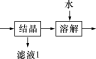 ”环节的目的是
”环节的目的是___________ 。
(4)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到色泽纯正的氢氧化铁,而且还可以___________ 。
(5)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁1.2红的含量。已知 的吸光度
的吸光度 (对特定波长光的吸收程度)与
(对特定波长光的吸收程度)与 标准溶液浓度的关系如图所示:
标准溶液浓度的关系如图所示: 的质量分数为
的质量分数为___________ %(保留小数点后一位)。
(6)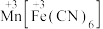 可用作钾离子电池的正极材料,其晶胞结构如下图所示:
可用作钾离子电池的正极材料,其晶胞结构如下图所示: 最近的
最近的 有
有___________ %个。
②第三电离能 ,结合原子结构解释原因:
,结合原子结构解释原因:___________ %。
③ 放电后转化为
放电后转化为 ,充电时物质的变化如下:
,充电时物质的变化如下:
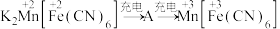
写出充电时生成A的电极反应式:___________ (请标注A中Fe和Mn的化合价)。
 、
、 、
、 和
和 )得到绿矾
)得到绿矾 ,然后制取透明氧化铁颜料的流程如下:
,然后制取透明氧化铁颜料的流程如下: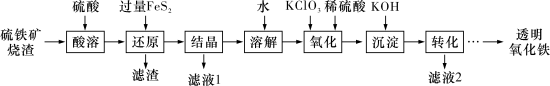
 ),难溶于水;②“还原”时,
),难溶于水;②“还原”时, 能将
能将 中的硫元素氧化为+6价。
中的硫元素氧化为+6价。回答下列问题:
(1)“滤渣”中的主要成分有过量的
 和
和(2)“还原”过程中涉及的离子方程式为
(3)流程中“
 ”环节的目的是
”环节的目的是(4)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到色泽纯正的氢氧化铁,而且还可以
(5)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁1.2红的含量。已知
 的吸光度
的吸光度 (对特定波长光的吸收程度)与
(对特定波长光的吸收程度)与 标准溶液浓度的关系如图所示:
标准溶液浓度的关系如图所示: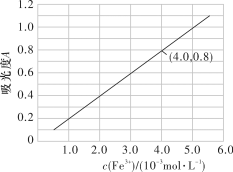
 的质量分数为
的质量分数为(6)
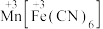 可用作钾离子电池的正极材料,其晶胞结构如下图所示:
可用作钾离子电池的正极材料,其晶胞结构如下图所示: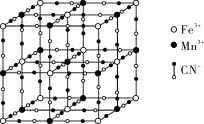
 最近的
最近的 有
有②第三电离能
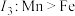 ,结合原子结构解释原因:
,结合原子结构解释原因:③
 放电后转化为
放电后转化为 ,充电时物质的变化如下:
,充电时物质的变化如下: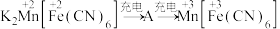
写出充电时生成A的电极反应式:
您最近一年使用:0次
5 . 化学实验源于生活。下列实验方案设计、现象与结论均正确的是
| 选项 | 目的 | 方案设计 | 现象结论 |
| A | 检验鸡皮中是否含有脂肪 | 取一小块鸡皮于表面皿上,将几滴浓硝酸滴到鸡皮上 | 一段时间后鸡皮变黄,说明鸡皮中含有脂肪 |
| B | 检验火柴头中是否含有氯元素 | 将几根未燃过的火柴头浸入水中,稍后取少量溶液于试管中,加入稀 、 、 溶液 溶液 | 若有白色沉淀产生,说明火柴头中含有氯元素 |
| C | 检验海带中的碘元素 | 向海带灰的浸取液中通入适量氯气,再加入 萃取 萃取 | 若下层出现紫红色,则海带中含有碘元素 |
| D | 检验黑木耳中的铁元素 | 取少量黑木耳剪碎研磨后加水搅拌,取上层清液于试管中,加入稀硫酸后再加入KSCN溶液 | 若溶液未变红,说明黑木耳中不含三价铁元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 下列离子方程式书写正确的是
A.钠与水反应: |
B.氯气与水反应: |
C.盐酸中滴入少量碳酸钠溶液: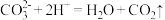 |
D.氯化铁溶液中加入铁粉: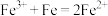 |
您最近一年使用:0次
2024-02-12更新
|
82次组卷
|
3卷引用:江西省宜春市宜丰中学2023-2024学年高一上学期1月月考化学试题
解题方法
7 . 下列各组离子在指定溶液中一定能大量共存的是
A.  溶液中: 溶液中: 、 、 、 、 、 、 |
B.含有 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C.与铝反应放出氢气的溶液中: 、 、 、 、 、 、 |
D.滴加 溶液显红色的溶液中: 溶液显红色的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
解题方法
8 . 下列实验事实与对应的结论正确的是
| 选项 | 实验事实 | 结论 |
| A | 蓝色石蕊试纸上滴加新制氯水先变红后褪色 | 新制氯水无酸性,只有漂白性 |
| B | 一定量Fe粉与水蒸气反应后的混合物溶于稀硫酸,在此溶液中滴加KSCN后无明显变化 | 生成的 可能与多余的Fe粉反应,全部变成了 可能与多余的Fe粉反应,全部变成了 |
| C | 金属钠在空气中燃烧后生成淡黄色固体 | 钠在空气中长久放置生成 |
| D | 配制一定物质的量浓度的溶液时,定容时液面超过刻度线 | 需趁下层溶质尚未扩散之际,快速用胶头滴管吸出上层溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-27更新
|
62次组卷
|
2卷引用:江西省丰城市第九中学2023-2024学年高一下学期开学考试化学试题
名校
解题方法
9 . 下列各组离子在指定溶液中一定能大量共存的是
A.澄清透明溶液中: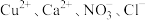 |
B.滴加石蕊试液显红色的溶液中: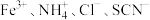 |
C.与Al反应产生H2的溶液中: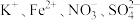 |
D.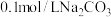 溶液中: 溶液中: |
您最近一年使用:0次
2024-01-22更新
|
111次组卷
|
3卷引用:江西省宜春市丰城中学东校区(九中)2023-2024学年高二下学期开学考试化学试卷
23-24高三上·宁夏银川·阶段练习
名校
解题方法
10 . 为达到相应目的,下列方案设计、现象与结论均正确的是
| 选项 | 目的 | 方案设计 | 现象与结论 |
| A | 检验食盐中是否含有碘元素 | 向某品牌的食盐水溶液中滴加淀粉溶液 | 溶液颜色不变,说明该食盐为无碘盐 |
| B | 检验葡萄酒中是否含有SO2 | 向葡萄酒中滴加几滴酸性高锰酸钾溶液 | 酸性高锰酸钾溶液紫色褪去,证明葡萄酒中含 SO2 |
| C | SO2缓慢通入滴有酚酞的NaOH 溶液中 | 溶液红色褪去 | SO2具有漂白性 |
| D | 检验菠菜中的铁元素 | 取少量菠菜叶,剪碎研磨后加水搅拌,取上层清液于试管中,加入新制氯水后再滴入 KSCN 溶液 | 若溶液变红,说明菠菜中含有铁元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



