11-12高二上·福建福州·阶段练习
名校
解题方法
1 . 肼(N2H4)是火箭发动机的燃料,它与N2O4反应生成氮气和水蒸气。已知:
①N2(g)+2O2(g)=N2O4(g) △H=+8.7 kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g) △H= - 534.0 kJ/mol
下列表示肼跟N2O4反应的热化学方程式正确的是
①N2(g)+2O2(g)=N2O4(g) △H=+8.7 kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g) △H= - 534.0 kJ/mol
下列表示肼跟N2O4反应的热化学方程式正确的是
| A.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) △H=-542.7 kJ/mol |
| B.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) △H=-1076.7 kJ/mol |
| C.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) △H=-2153.4 kJ/mol |
| D.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) △H=-1059.3 kJ/mol |
您最近一年使用:0次
2020-12-01更新
|
195次组卷
|
19卷引用:2013-2014学年江苏省常州市某重点中学高二上学期期中考试化学试卷
(已下线)2013-2014学年江苏省常州市某重点中学高二上学期期中考试化学试卷(已下线)2011-2012年福建省福州市罗源一中高二上学期第一次月考化学试卷(已下线)2012-2013学年江苏省宿迁青华中学高二下学期期中考化学普通班试卷(已下线)2012-2013学年河北省存瑞中学高一下学期第三次月考化学试卷2014-2015浙江省台州书生中学高二上学期第三次月考化学试卷2015-2016学年福建省福州八中高二上学期期末化学试卷2015-2016学年河北省邢台一中高一下第一次月考化学试卷2016-2017学年河南省郸城中学高二上第一次考试化学卷2016-2017学年山东省济南市长清一中高二上第一次质检化学卷内蒙古杭锦后旗奋斗中学2018届高三上学期第三次月考化学试题湖北省仙桃市汉江高级中学2016-2017学年高一下学期期末考试化学试题【全国校级联考】山西省汾阳市第二高级中学、文水县第二高级中学2016-2017学年高二上学期第一次联考化学试题甘肃省岷县二中2018-2019学年高二上学期第一次月考化学试题【全国百强校】黑龙江省哈尔滨市第六中学2019届高三上学期10月月考化学试题(已下线)2018年12月21日 《每日一题》人教选修4-盖斯定律(已下线)2019年12月18日 《每日一题》化学人教版(选修4)——盖斯定律黑龙江省安达市第七中学2019-2020学年高二3月月考化学试题广东实验中学附属天河学校2020--2021学年高二上学期期中考试化学试题海南省北京师范大学万宁附中2020-2021学年高一下学期期中考试化学试题
名校
解题方法
2 . TiO2和 TiCl4均为重要的工业原料。已知:
Ⅰ.TiCl4(g)+O2(g) TiO2(s)+2Cl2(g) ΔH1=-175.4 kJ•mol-1
TiO2(s)+2Cl2(g) ΔH1=-175.4 kJ•mol-1
Ⅱ.2C(s)+O2(g) 2CO(g) ΔH2=-220.9 kJ•mol -1
2CO(g) ΔH2=-220.9 kJ•mol -1
请回答下列问题:
(1) TiCl4(g)与CO(g)反应生成 TiO2(s)、C(s)和氯气的热化学方程式为____________________________________________________________________ 。
(2)若反应Ⅱ的逆反应活化能表示为E kJ•mol -1,则E__________ 220.9(填“>”“<”或“=”)。
(3) t ℃时,向 10 L 恒容密闭容器中充入 1 mol TiCl4和 2 mol O2,发生反应Ⅰ。5 min 达到平衡时测得 TiO2的物质的量为 0.2 mol。
①0~5 min 内,用 Cl2表示的反应速率 v(Cl2)=_____________ 。
②TiCl4的平衡转化率α=_________________ 。
③下列措施,既能加快逆反应速率又能增大 TiCl4的平衡转化率的是______________ (填选项字母)。
A.缩小容器容积 B.加入催化剂
C.分离出部分 TiO2 D.增大 O2浓度
④t ℃时,向10L恒容密闭容器中充入 3 mol TiCl4和一定量 O2的混合气体,发生反应
Ⅰ,两种气体的平衡转化率(α)与起始的物质的量之比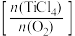 的关系如图所示:
的关系如图所示:
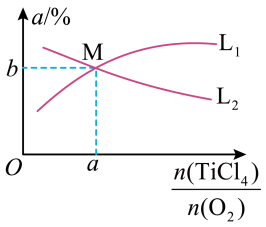
能表示 TiCl4平衡转化率的曲线为_________________ (填“L1”或“L2”);M 点的坐标为 ________________________ 。
Ⅰ.TiCl4(g)+O2(g)
 TiO2(s)+2Cl2(g) ΔH1=-175.4 kJ•mol-1
TiO2(s)+2Cl2(g) ΔH1=-175.4 kJ•mol-1Ⅱ.2C(s)+O2(g)
 2CO(g) ΔH2=-220.9 kJ•mol -1
2CO(g) ΔH2=-220.9 kJ•mol -1请回答下列问题:
(1) TiCl4(g)与CO(g)反应生成 TiO2(s)、C(s)和氯气的热化学方程式为
(2)若反应Ⅱ的逆反应活化能表示为E kJ•mol -1,则E
(3) t ℃时,向 10 L 恒容密闭容器中充入 1 mol TiCl4和 2 mol O2,发生反应Ⅰ。5 min 达到平衡时测得 TiO2的物质的量为 0.2 mol。
①0~5 min 内,用 Cl2表示的反应速率 v(Cl2)=
②TiCl4的平衡转化率α=
③下列措施,既能加快逆反应速率又能增大 TiCl4的平衡转化率的是
A.缩小容器容积 B.加入催化剂
C.分离出部分 TiO2 D.增大 O2浓度
④t ℃时,向10L恒容密闭容器中充入 3 mol TiCl4和一定量 O2的混合气体,发生反应
Ⅰ,两种气体的平衡转化率(α)与起始的物质的量之比
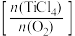 的关系如图所示:
的关系如图所示:
能表示 TiCl4平衡转化率的曲线为
您最近一年使用:0次
2020-09-10更新
|
204次组卷
|
4卷引用:江苏省常州市第一中学2023-2024学年高二上学期10月月考化学试题
3 . 氮和氮的化合物在工农业生产、国防和生活中都有极其广泛的用途。请回答下列与氮元素有关的问题:
(1)亚硝酸氯(结构式为Cl-N=O)是有机合成中的重要试剂,可由Cl2和NO在一定条件下通过以下反应制得:2NO+Cl2=2ClNO,已知几种化学键的键能数据如下表所示:
请根据表中数据计算:2NO(g)+Cl2(g)=2ClNO(g)△H=___ kJ•mol-1。
(2)温度一定时,在一个体积为1L的密闭容器中通入2molNO和1molCl2,10min时ClNO体积占气体总体积40%(气体的“体积分数”即“物质的量分数”),则反应开始到10min内NO的平均反应速率:v(NO)=___ mol·L-1·min-1
(3)以NH3为还原剂在脱硝装置中消除烟气中的氮氧化物,
主反应为4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) △H1
副反应:4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H2=-1267.1kJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H3=-907.3kJ/mol
①△H1=___ 。
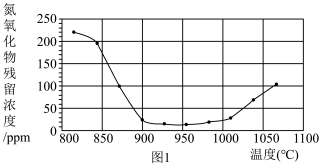
②将烟气按一定的流速通过脱硝装置,测得出口NO的浓度与温度的关系如图1,试分析脱硝的适宜温度是___ (填序号)
a.<850℃ b.900~1000℃ c.>1050 ℃
(4)以连二亚硫酸盐(S2O42-)为还原剂脱除烟气中的NO,并通过电解再生,装置如图2。阴极的电极反应式为___ 。
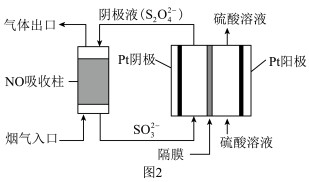
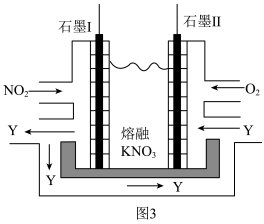
(5)利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,装置如图3所示,电池工作时,NO2转变成绿色硝化剂Y(N2O5),可循环使用,则石墨Ⅰ附近发生的电极反应式为:___ 。
(1)亚硝酸氯(结构式为Cl-N=O)是有机合成中的重要试剂,可由Cl2和NO在一定条件下通过以下反应制得:2NO+Cl2=2ClNO,已知几种化学键的键能数据如下表所示:
| 化学键 | Cl-Cl | Cl-N | N=O | N=O(NO) |
| 键能(kJ·mol-1) | 243 | a | 607 | 630 |
(2)温度一定时,在一个体积为1L的密闭容器中通入2molNO和1molCl2,10min时ClNO体积占气体总体积40%(气体的“体积分数”即“物质的量分数”),则反应开始到10min内NO的平均反应速率:v(NO)=
(3)以NH3为还原剂在脱硝装置中消除烟气中的氮氧化物,
主反应为4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) △H1
副反应:4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H2=-1267.1kJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H3=-907.3kJ/mol
①△H1=
②将烟气按一定的流速通过脱硝装置,测得出口NO的浓度与温度的关系如图1,试分析脱硝的适宜温度是
a.<850℃ b.900~1000℃ c.>1050 ℃

(4)以连二亚硫酸盐(S2O42-)为还原剂脱除烟气中的NO,并通过电解再生,装置如图2。阴极的电极反应式为

(5)利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,装置如图3所示,电池工作时,NO2转变成绿色硝化剂Y(N2O5),可循环使用,则石墨Ⅰ附近发生的电极反应式为:

您最近一年使用:0次
4 . 科学家认为,氢气是21世纪一种高效而无污染的理想能源。
(1)为了有效发展氢能源,首先必须制得廉价的氢气,下列可供开发较经济且资源可持续利用的制氢气的方法是___ 。
A.电解水 B.锌和稀硫酸反应 C.催化光解海水 D.分解天然气
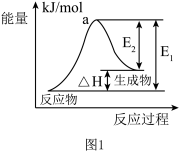
(2)用水分解获得氢气的能量变化如图1所示,则此反应的焓变△H=___ kJ/mol。(请用关于E1,E2的代数式表示)。
(3)以甲烷为原料制取氢气是工业上常用的制氢方法。已知:
CH4(g)+H2O(g)═CO(g)+3H2(g) △H=+206.2kJ•mol﹣1
CH4(g)+CO2(g)═2CO(g)+2H2(g) △H=+247.4kJ•mol﹣1
则CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=___ kJ•mol﹣1
(4)某固体酸膜氢氧燃料电池以Ca(HSO4)2固体为电解质传递H+,其基本结构如图2所示,请按要求回答下列问题:
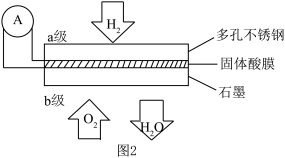
①b极上的电极反应式为___ 。
②此电池工作时每消耗4.48L(标准状况下)H2,转移电子___ mol。
③若将这些电子用于铅蓄电池(两极板上分别覆盖有Pb、PbO2,电解质溶液是H2SO4溶液)充电,铅蓄电池中产生H2SO4的物质的量为___ mol,铅蓄电池阳极发生的反应为___ 。
(1)为了有效发展氢能源,首先必须制得廉价的氢气,下列可供开发较经济且资源可持续利用的制氢气的方法是
A.电解水 B.锌和稀硫酸反应 C.催化光解海水 D.分解天然气
(2)用水分解获得氢气的能量变化如图1所示,则此反应的焓变△H=

(3)以甲烷为原料制取氢气是工业上常用的制氢方法。已知:
CH4(g)+H2O(g)═CO(g)+3H2(g) △H=+206.2kJ•mol﹣1
CH4(g)+CO2(g)═2CO(g)+2H2(g) △H=+247.4kJ•mol﹣1
则CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=
(4)某固体酸膜氢氧燃料电池以Ca(HSO4)2固体为电解质传递H+,其基本结构如图2所示,请按要求回答下列问题:

①b极上的电极反应式为
②此电池工作时每消耗4.48L(标准状况下)H2,转移电子
③若将这些电子用于铅蓄电池(两极板上分别覆盖有Pb、PbO2,电解质溶液是H2SO4溶液)充电,铅蓄电池中产生H2SO4的物质的量为
您最近一年使用:0次
5 . 天然气既是高效洁净的能源,又是重要的化工原料,在生产、生活中用途广泛。
(1)已知25℃、101kPa时,1g甲烷不完全燃烧生成CO和液态水时放出37.96kJ热量,则该条件下反应2CH4(g)+3O2(g)=2CO(g)+4H2O(l)的ΔH=___ kJ·mol-1。
(2)甲烷可以消除氮氧化物污染。如:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g)。下列措施能够使该反应速率加快的是
N2(g)+CO2(g)+2H2O(g)。下列措施能够使该反应速率加快的是___ 。
a.使用催化剂 b.降低温度 c.及时分离水
(3)甲烷可直接应用于燃料电池,该电池采用可传导O2-的固体氧化物为电解质,其工作原理如图所示:
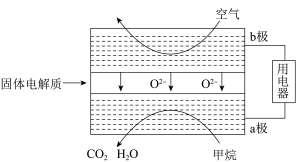
①外电路电子移动方向:___ 。(填“a极到b极”或“b极到a极”)。
②a极电极反应式为___ 。
③若燃料电池消耗的空气在标准状况下的体积是22.4L(假设空气中O2体积分数为20%),则理论上消耗甲烷___ mol。
(1)已知25℃、101kPa时,1g甲烷不完全燃烧生成CO和液态水时放出37.96kJ热量,则该条件下反应2CH4(g)+3O2(g)=2CO(g)+4H2O(l)的ΔH=
(2)甲烷可以消除氮氧化物污染。如:CH4(g)+2NO2(g)
 N2(g)+CO2(g)+2H2O(g)。下列措施能够使该反应速率加快的是
N2(g)+CO2(g)+2H2O(g)。下列措施能够使该反应速率加快的是a.使用催化剂 b.降低温度 c.及时分离水
(3)甲烷可直接应用于燃料电池,该电池采用可传导O2-的固体氧化物为电解质,其工作原理如图所示:

①外电路电子移动方向:
②a极电极反应式为
③若燃料电池消耗的空气在标准状况下的体积是22.4L(假设空气中O2体积分数为20%),则理论上消耗甲烷
您最近一年使用:0次
解题方法
6 . 已知:①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1;
②C(s)+O2(g)=CO2(g) ΔH2;
③2H2(g)+O2(g)=2H2O(l) ΔH3;
④2CO2(g)+4H2(g)=CH3COOH(l)+2H2O(l) ΔH4;
⑤2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH5。
下列关于上述反应焓变的判断正确的是( )
②C(s)+O2(g)=CO2(g) ΔH2;
③2H2(g)+O2(g)=2H2O(l) ΔH3;
④2CO2(g)+4H2(g)=CH3COOH(l)+2H2O(l) ΔH4;
⑤2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH5。
下列关于上述反应焓变的判断正确的是( )
| A.ΔH1>0,ΔH2<0 | B.ΔH5=2ΔH2+ΔH3-ΔH1 |
| C.ΔH1<0,ΔH3<0 | D.ΔH4=ΔH1-2ΔH3 |
您最近一年使用:0次
名校
解题方法
7 . 用H2O2和H2SO4的混合溶液可腐蚀印刷电路板上的铜,其热化学方程式为Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l) ΔH
已知①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH1=64kJ·mol-1
②2H2O2(l)=2H2O(l)+O2(g) ΔH2=-196kJ·mol-1
③H2(g)+ O2(g)=H2O(l) ΔH3=-286kJ·mol-1
O2(g)=H2O(l) ΔH3=-286kJ·mol-1
下列说法不正确的是( )
已知①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH1=64kJ·mol-1
②2H2O2(l)=2H2O(l)+O2(g) ΔH2=-196kJ·mol-1
③H2(g)+
 O2(g)=H2O(l) ΔH3=-286kJ·mol-1
O2(g)=H2O(l) ΔH3=-286kJ·mol-1下列说法不正确的是( )
| A.反应①可通过铜作电极电解稀的H2SO4方法实现 |
| B.反应②在任何条件下都能自发进行 |
C.若H2(g)+ O2(g)=H2O(g) ΔH4,则ΔH4<ΔH3 O2(g)=H2O(g) ΔH4,则ΔH4<ΔH3 |
| D.ΔH=-320kJ·mol-1 |
您最近一年使用:0次
2020-03-03更新
|
281次组卷
|
6卷引用:江苏省常州市第一中学2019届高三上学期10月月考化学试题
解题方法
8 . 通过多种方法对废水废气脱硝,可以减轻含氮物质对环境的污染。
(1)在缺氧条件下,由于兼性脱氮菌的作用,将NO2-和NO还原成N2实现脱硝的过程,称为反硝化。污水处理厂以甲醇作碳源实现硝酸盐的反硝化过程分两步进行:
3NO3-(aq)+CH3OH(l)=3NO2-(aq)+CO2(g)+2H2O(l);ΔH=-398.9 kJ·mol-1
2NO2-(aq)+CH3OH(l)=N2(g)+CO2(g)+H2O(l)+2OH-(aq);ΔH=-91.5 kJ·mol-1
反应6NO3-(aq)+5CH3OH(l)=3N2(g)+5CO2(g)+7H2O(l)+6OH-(aq)的ΔH=______ kJ·mol-1。
(2)在船舶废气的脱硝工艺中,采用无隔膜电解法对海水进行电解,再用循环喷淋模式对船舶废气进行脱硝。
①使用惰性电极对海水电解。由于采用无隔膜电解槽,阳极产物大部分是ClO-,同时会有少量Cl2、ClO3-生成,则电解生成ClO3-的电极反应式为________ 。
②一段时间后,随电解海水中ClO-含量的不断增加,经循环喷淋系统吸收的废气中NO脱除率不断增加,而NO2的脱除率却有所下降,这是由于NO被氧化为NO2,该反应的离子方程式为_________________________ 。
③电解海水溶液的pH对氮氧化物的去除率会产生一定影响,见下图。当电解液pH从5.5下降至4.5过程中,NO和NOx的脱除率快速上升的原因是________________ 。综合考虑脱硝效率、后期处理、设备使用等因素,选择电解海水溶液的最佳pH为________ 。
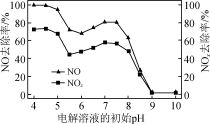
(3)锅炉的烟气脱硝处理常采用以氨为还原剂进行催化还原,主要反应如下:
4NH3+4NO+O2=4N2+6H2O①
4NH3+6NO=5N2+6H2O②
当反应温度过高时,NH3会发生以下反应:
4NH3+3O2=2N2+6H2O③
4NH3+5O2=4NO+6H2O④
在反应②中当生成1 mol N2时,转移的电子数为________ mol。随着反应温度升高,脱硝效率降低的原因可能是________ 。
(1)在缺氧条件下,由于兼性脱氮菌的作用,将NO2-和NO还原成N2实现脱硝的过程,称为反硝化。污水处理厂以甲醇作碳源实现硝酸盐的反硝化过程分两步进行:
3NO3-(aq)+CH3OH(l)=3NO2-(aq)+CO2(g)+2H2O(l);ΔH=-398.9 kJ·mol-1
2NO2-(aq)+CH3OH(l)=N2(g)+CO2(g)+H2O(l)+2OH-(aq);ΔH=-91.5 kJ·mol-1
反应6NO3-(aq)+5CH3OH(l)=3N2(g)+5CO2(g)+7H2O(l)+6OH-(aq)的ΔH=
(2)在船舶废气的脱硝工艺中,采用无隔膜电解法对海水进行电解,再用循环喷淋模式对船舶废气进行脱硝。
①使用惰性电极对海水电解。由于采用无隔膜电解槽,阳极产物大部分是ClO-,同时会有少量Cl2、ClO3-生成,则电解生成ClO3-的电极反应式为
②一段时间后,随电解海水中ClO-含量的不断增加,经循环喷淋系统吸收的废气中NO脱除率不断增加,而NO2的脱除率却有所下降,这是由于NO被氧化为NO2,该反应的离子方程式为
③电解海水溶液的pH对氮氧化物的去除率会产生一定影响,见下图。当电解液pH从5.5下降至4.5过程中,NO和NOx的脱除率快速上升的原因是

(3)锅炉的烟气脱硝处理常采用以氨为还原剂进行催化还原,主要反应如下:
4NH3+4NO+O2=4N2+6H2O①
4NH3+6NO=5N2+6H2O②
当反应温度过高时,NH3会发生以下反应:
4NH3+3O2=2N2+6H2O③
4NH3+5O2=4NO+6H2O④
在反应②中当生成1 mol N2时,转移的电子数为
您最近一年使用:0次
10-11高三上·吉林·阶段练习
名校
9 . 根据下列热化学方程式:
①C(s)+O2=CO2(g) ΔH1=-393.5 kJ·mol-1
②H2(g)+1/2O2(g)=H2O(l) ΔH2=-285.8 kJ·mol-1
③CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH3=-870.3kJ·mol-1
可计算出2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热
①C(s)+O2=CO2(g) ΔH1=-393.5 kJ·mol-1
②H2(g)+1/2O2(g)=H2O(l) ΔH2=-285.8 kJ·mol-1
③CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH3=-870.3kJ·mol-1
可计算出2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热
| A.ΔH=244.1 kJ·mol-1 | B.ΔH=-488.3 kJ·mol-1 |
| C.ΔH=-996.6 kJ·mol-1 | D.ΔH=996.6 kJ·mol-1 |
您最近一年使用:0次
2019-10-13更新
|
422次组卷
|
24卷引用:2013-2014学年江苏常州市某重点高中高二上学期第四次月考化学试卷
(已下线)2013-2014学年江苏常州市某重点高中高二上学期第四次月考化学试卷(已下线)2011届吉林省第一中学高三上学期第二次教学质量检测化学卷(已下线)2011届黑龙江省哈尔滨六中高三上学期期末考试化学试卷(已下线)2010—2011学年广东省广州六中高二上学期期末考试化学试卷卷(已下线)2013届山东省济宁市鱼台一中高三上学期期中考试化学试卷(已下线)2012-2013学年甘肃省武威第五中学高二11月月考化学试卷(已下线)2012-2013学年黑龙江省集贤县第一中学高二上学期期末考试化学试卷(已下线)2013-2014学年天津市南开区高二上学期期末考试化学试卷(已下线)2014~2015学年江西四校9月联考高二化学试卷2016届山东省枣庄市滕州十一中高三上学期期末模拟化学试卷(已下线)同步君 人教版 选修4 第1章 第3节 反应热的计算2016-2017学年河北省景县中学高二上学期摸底化学试卷广东省阳东广雅学校2017-2018学年高二9月月考化学试题高中化学人教版 选修四 第一章 化学反应与能量 第三节 化学反应热的计算 化学反应热的计算第二课时(反应热的计算)河北省承德市第二中学2017-2018学年高二上学期第一次月考化学试题广西宾阳县宾阳中学2019-2020学年高二9月月考化学试题山东省济南外国语学校三箭分校2019-2020学年高二上学期期中考试化学试题吉林省公主岭市范家屯镇第一中学2020届高三上学期第二次月考化学试题吉林省长春市第二十九中学2019-2020学年高一下学期线上检测化学试题福建省永安市第三中学2020-2021学年高二10月月考化学(学考班)试题湖南省湘潭电机子弟中学2019-2020学年高二下学期期中考试化学(理)试题广东省梅州市大埔县虎山中学2021-2022学年高二上学期第一次段考(10月)化学试题广东省惠州市博罗县博罗中学2023-2024学年高二上学期高二10月月考化学试题青海省西宁市海湖中学2023-2024学年高二下学期开学考试化学试卷
10 . 1mol气态钠离子和1mol气态氯离子结合生成1mol 氯化钠晶体所释放出的热能为氯化钠晶体的晶格能。
(1)下列热化学方程式中,能直接表示出氯化钠晶体晶格能的是________
A.Na+(g) + Cl-(g) = NaCl(s) ΔH B.Na(s) +1/2Cl2(g)=NaCl(s) ΔH1
C.Na(s)= Na(g) ΔH2 D.Na(g) —e-= Na+(g) ΔH3
E.1/2Cl2(g) =Cl(g) ΔH4 F.Cl(g)+ e-= Cl-(g) ΔH5
(2)写出ΔH1与ΔH、ΔH2、ΔH3、ΔH4、ΔH5之间的关系式________
(1)下列热化学方程式中,能直接表示出氯化钠晶体晶格能的是
A.Na+(g) + Cl-(g) = NaCl(s) ΔH B.Na(s) +1/2Cl2(g)=NaCl(s) ΔH1
C.Na(s)= Na(g) ΔH2 D.Na(g) —e-= Na+(g) ΔH3
E.1/2Cl2(g) =Cl(g) ΔH4 F.Cl(g)+ e-= Cl-(g) ΔH5
(2)写出ΔH1与ΔH、ΔH2、ΔH3、ΔH4、ΔH5之间的关系式
您最近一年使用:0次
2019-04-29更新
|
75次组卷
|
2卷引用:【校级联考】江苏省常州“教学研究合作联盟”2018-2019学年高二下学期期中考试化学试题



