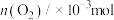1 . 一定温度下,在2.0L密闭容器中加入纳米级 并通入
并通入 ,发生反应:
,发生反应: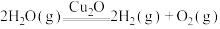
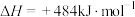 ,不同时间产生
,不同时间产生 的物质的量见下表,下列说法错误的是
的物质的量见下表,下列说法错误的是
 并通入
并通入 ,发生反应:
,发生反应: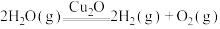
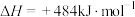 ,不同时间产生
,不同时间产生 的物质的量见下表,下列说法错误的是
的物质的量见下表,下列说法错误的是时间 | 20 | 40 | 60 | 80 |
| 1.0 | 1.6 | 2.0 | 2.0 |
A.使用纳米级 ,可以增大平衡时氧气的体积分数 ,可以增大平衡时氧气的体积分数 |
B.达到平衡时,至少需要从外界吸收能量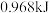 |
C.增大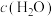 ,可以改变反应的限度 ,可以改变反应的限度 |
D.前20min的平均反应速率 |
您最近一年使用:0次
2 . 氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。
(1)已知:2C(s)+O2(g)⇌2CO(g)
C(s)+O2(g)⇌CO2(g)
N2(g)+O2(g)⇌2NO(g)
①则反应2CO(g)+2NO(g)⇌N2(g)+2CO2(g)的
___________ ;(用 、
、 、
、 表示)
表示)
②在一个恒温恒容的密闭容器中发生反应2CO(g)+2NO(g)⇌N2(g)+2CO2(g),能表明已达到平衡状态的标志有___________ 。
A.混合气体的压强保持不变
B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变
D.气体的总质量
E.
F. 内生成
内生成 同时消耗
同时消耗
(2)向容积为 的密闭容器中加入活性炭(足量)和
的密闭容器中加入活性炭(足量)和 ,发生反应C(s)+2NO(g)⇌N2(g)+CO2(g),
,发生反应C(s)+2NO(g)⇌N2(g)+CO2(g), 和
和 的物质的量变化如下表所示。
的物质的量变化如下表所示。
①0~5min内,以 表示的该反应速率
表示的该反应速率
___________ ,最终达平衡时 的转化率
的转化率
___________ ,该温度T℃下的平衡常数
___________ 。
②若该反应ΔH>0,要提高工业上NO的转化率可采取的措施有___________ (至少写一种)。
(3)CO2和H2在一定条件下可制取甲醇,反应如下:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),向容积相同的恒容密闭容器中分别充入等量的CO2和H2,在不同催化剂(M型、N型)条件下反应相同时间,CO2转化率随反应温度变化如图。
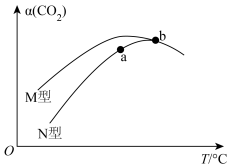
①使用___________ (选填M、N)型催化剂反应的活化能更高。
②b点不同催化剂作用下,CO2的转化率相同且均有下降趋势的原因是___________ 。
(1)已知:2C(s)+O2(g)⇌2CO(g)

C(s)+O2(g)⇌CO2(g)

N2(g)+O2(g)⇌2NO(g)

①则反应2CO(g)+2NO(g)⇌N2(g)+2CO2(g)的

 、
、 、
、 表示)
表示)②在一个恒温恒容的密闭容器中发生反应2CO(g)+2NO(g)⇌N2(g)+2CO2(g),能表明已达到平衡状态的标志有
A.混合气体的压强保持不变
B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变
D.气体的总质量
E.

F.
 内生成
内生成 同时消耗
同时消耗
(2)向容积为
 的密闭容器中加入活性炭(足量)和
的密闭容器中加入活性炭(足量)和 ,发生反应C(s)+2NO(g)⇌N2(g)+CO2(g),
,发生反应C(s)+2NO(g)⇌N2(g)+CO2(g), 和
和 的物质的量变化如下表所示。
的物质的量变化如下表所示。| 条件 | 保持温度为 /℃ /℃ | ||||||
| 时间 | 0 | 5min | 10min | 15min | 20min | 25min | 30min |
 物质的量 物质的量 | 2.0 | 1.4 | 1.0 | 0.70 | 0.50 | 0.40 | 0.40 |
| N2物质的量/mol | 0 | 0.3 | 0.50 | 0.65 | 0.75 | 0.80 | 0.80 |
 表示的该反应速率
表示的该反应速率
 的转化率
的转化率

②若该反应ΔH>0,要提高工业上NO的转化率可采取的措施有
(3)CO2和H2在一定条件下可制取甲醇,反应如下:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),向容积相同的恒容密闭容器中分别充入等量的CO2和H2,在不同催化剂(M型、N型)条件下反应相同时间,CO2转化率随反应温度变化如图。

①使用
②b点不同催化剂作用下,CO2的转化率相同且均有下降趋势的原因是
您最近一年使用:0次
2024-02-02更新
|
112次组卷
|
2卷引用:四川省广安市华蓥中学2023-2024学年高二上学期11月月考化学试题
名校
解题方法
3 . 环戊二烯( )是一种重要的有机化工原料。
)是一种重要的有机化工原料。
Ⅰ.环戊二烯容易反应生成双环戊二烯(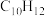 ):
):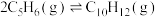 ,不同温度下,溶液中环戊二烯(
,不同温度下,溶液中环戊二烯( )浓度(初始浓度为
)浓度(初始浓度为 )与反应时间的关系如图所示:
)与反应时间的关系如图所示:
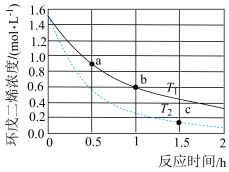
(1)反应开始至b点时,用双环戊二烯(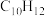 )表示的平均速率为
)表示的平均速率为______ 。
(2)
______  ,b点的逆反应速率
,b点的逆反应速率______ a点的正反应速率(两空均选填“>”、“<”或“=”)。
(3)一定量的环戊二烯气体在恒温恒压的密闭容器中发生上述反应,可说明一定达化学平衡状态的是______ 。
a.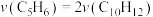
b.容器内气体压强不再变化
c.容器内混合气体的密度不再变化
d.容器内混合气体的平均相对分子质量不再变化
Ⅱ.可用伓戊烯(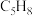 )制备环戊二烯(
)制备环戊二烯( ),有如下反应:
),有如下反应:
反应i: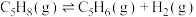

反应ii:
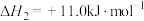
反应iii: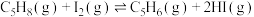
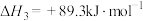
(4)反应i的焓变
______ ,反应iii的平衡常数 为
为______ (用 、
、 表示)。
表示)。
(5)某温度时在恒容密闭容器中充入等物质的量的碘和环戊烯发生反应iii,起始总压为 ,平衡时总压为
,平衡时总压为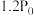 。
。
①平衡时HI的体积分数为______ %。
②用平衡分压代替平衡浓度计算压强平衡常数
______ (要求用最简整数比,含 的代数式表示)。
的代数式表示)。
③达到平衡后,既增加环戊烯(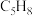 )的平衡转化率同时加快反应速率的措施有
)的平衡转化率同时加快反应速率的措施有______ (仅写一条)
 )是一种重要的有机化工原料。
)是一种重要的有机化工原料。Ⅰ.环戊二烯容易反应生成双环戊二烯(
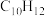 ):
):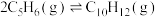 ,不同温度下,溶液中环戊二烯(
,不同温度下,溶液中环戊二烯( )浓度(初始浓度为
)浓度(初始浓度为 )与反应时间的关系如图所示:
)与反应时间的关系如图所示:
(1)反应开始至b点时,用双环戊二烯(
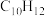 )表示的平均速率为
)表示的平均速率为(2)

 ,b点的逆反应速率
,b点的逆反应速率(3)一定量的环戊二烯气体在恒温恒压的密闭容器中发生上述反应,可说明一定达化学平衡状态的是
a.
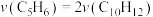
b.容器内气体压强不再变化
c.容器内混合气体的密度不再变化
d.容器内混合气体的平均相对分子质量不再变化
Ⅱ.可用伓戊烯(
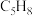 )制备环戊二烯(
)制备环戊二烯( ),有如下反应:
),有如下反应:反应i:
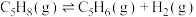

反应ii:

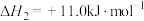
反应iii:
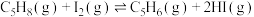
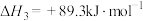
(4)反应i的焓变

 为
为 、
、 表示)。
表示)。(5)某温度时在恒容密闭容器中充入等物质的量的碘和环戊烯发生反应iii,起始总压为
 ,平衡时总压为
,平衡时总压为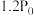 。
。①平衡时HI的体积分数为
②用平衡分压代替平衡浓度计算压强平衡常数

 的代数式表示)。
的代数式表示)。③达到平衡后,既增加环戊烯(
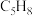 )的平衡转化率同时加快反应速率的措施有
)的平衡转化率同时加快反应速率的措施有
您最近一年使用:0次
名校
4 . 在一定温度下,将 和
和 放入容积为
放入容积为 的刚性密闭容器中发生反应:
的刚性密闭容器中发生反应: 。
。 后达到平衡,测得容器内
后达到平衡,测得容器内 的浓度减少了
的浓度减少了 ,则下列叙述正确的是
,则下列叙述正确的是
 和
和 放入容积为
放入容积为 的刚性密闭容器中发生反应:
的刚性密闭容器中发生反应: 。
。 后达到平衡,测得容器内
后达到平衡,测得容器内 的浓度减少了
的浓度减少了 ,则下列叙述正确的是
,则下列叙述正确的是A.在 内该反应用 内该反应用 的浓度变化表示的反应速率为 的浓度变化表示的反应速率为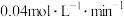 |
| B.当体系中气体的密度不变时,反应达到平衡 |
C.初始时的压强与平衡时的压强比为 |
D.平衡时 的体积分数为 的体积分数为 |
您最近一年使用:0次
名校
解题方法
5 . 在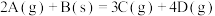 反应中,表示反应速率最快的是
反应中,表示反应速率最快的是
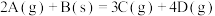 反应中,表示反应速率最快的是
反应中,表示反应速率最快的是A. | B. |
C. | D.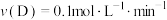 |
您最近一年使用:0次
2024-01-22更新
|
209次组卷
|
2卷引用:四川省达州外国语学校2023-2024学年高二上学期12月月考化学试题
名校
6 . 向两个锥形瓶中各加入0.048g镁条,塞紧橡胶塞,然后用注射器分别注入2 mL 2 mol⋅L 盐酸、2 mL 2 mol⋅L
盐酸、2 mL 2 mol⋅L 醋酸,测得锥形瓶内气体的压强随时间的变化如图所示,下列说法错误的是
醋酸,测得锥形瓶内气体的压强随时间的变化如图所示,下列说法错误的是
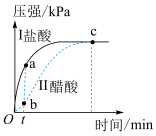
已知: 。
。
 盐酸、2 mL 2 mol⋅L
盐酸、2 mL 2 mol⋅L 醋酸,测得锥形瓶内气体的压强随时间的变化如图所示,下列说法错误的是
醋酸,测得锥形瓶内气体的压强随时间的变化如图所示,下列说法错误的是
已知:
 。
。A.0~t min内,反应速率 mol⋅L mol⋅L ⋅min ⋅min |
| B.溶液的pH:c>b |
C.反应结束后,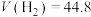 mL(标准状况下) mL(标准状况下) |
D.对于曲线Ⅱ,c点溶液中一定含有 、 、 、 、 和 和 |
您最近一年使用:0次
2024-01-19更新
|
52次组卷
|
2卷引用:四川省自贡市第一中学校2023-2024学年高二上学期期中考试化学试卷
名校
7 . 已知 ,一定温度时,在
,一定温度时,在 恒容密闭容器中,加入一定量
恒容密闭容器中,加入一定量 和
和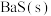 ,发生上述反应,各组分的物质的量随时间变化如图所示,下列说法正确的是
,发生上述反应,各组分的物质的量随时间变化如图所示,下列说法正确的是
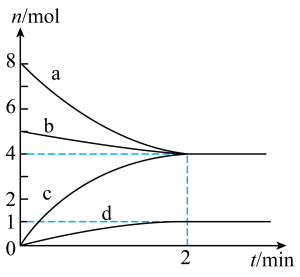
 ,一定温度时,在
,一定温度时,在 恒容密闭容器中,加入一定量
恒容密闭容器中,加入一定量 和
和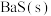 ,发生上述反应,各组分的物质的量随时间变化如图所示,下列说法正确的是
,发生上述反应,各组分的物质的量随时间变化如图所示,下列说法正确的是
A. 内反应速率 内反应速率 |
B.曲线 代表的物质为 代表的物质为 |
C.向平衡体系中加入 ,平衡逆向移动 ,平衡逆向移动 |
| D.该温度下反应的平衡常数为1 |
您最近一年使用:0次
名校
8 . 二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚,三步反应如下:
①2H2(g) + CO(g)⇌CH3OH(g) ΔH =-90.8kJ·mol-1
② CO(g) + H2O(g)⇌CO2(g) + H2(g) ΔH =-41.3kJ·mol-1
③2CH3OH(g)⇌CH3OCH3(g) + H2O(g) ΔH =-23.5kJ·mol-1
回答下列问题:
(1)一定条件下的密闭容器中,②反应达到平衡后,要提高CO的转化率,可以采取的措施是(填字母代号)_______ 。
a.高温高压 b.加入催化剂 c.增加H2O的浓度 d.分离出CO2
(2)写出由 H2(g)和CO(g)生成 CH3OCH3(g)和CO2(g)的热化学反应方程式_______ 。
(3)已知反应③在某温度下的平衡常数为400。此温度下,在恒容密闭容器中加入一定量的 CH3OH(g),反应T时刻测得各组分的浓度如下:
①比较T时刻正、逆反应速率的大小关系:v(正)_______ v(逆)(填“>”“<”或“=”)。
②若加入 CH3OH(g)后,经10min 反应达到平衡,此时c(CH3OH) =_______ ;0~10min内反应速率v(CH3OH)= _______ 。
③若反应达平衡后,温度不变,从体系中移走部分CH3OCH3,重新达到平衡后,CH3OH(g)的转化率_______ (填“增大”“减小”或“不变”)。若要使该反应平衡常数增大可采取的措施是_______ 。
①2H2(g) + CO(g)⇌CH3OH(g) ΔH =-90.8kJ·mol-1
② CO(g) + H2O(g)⇌CO2(g) + H2(g) ΔH =-41.3kJ·mol-1
③2CH3OH(g)⇌CH3OCH3(g) + H2O(g) ΔH =-23.5kJ·mol-1
回答下列问题:
(1)一定条件下的密闭容器中,②反应达到平衡后,要提高CO的转化率,可以采取的措施是(填字母代号)
a.高温高压 b.加入催化剂 c.增加H2O的浓度 d.分离出CO2
(2)写出由 H2(g)和CO(g)生成 CH3OCH3(g)和CO2(g)的热化学反应方程式
(3)已知反应③在某温度下的平衡常数为400。此温度下,在恒容密闭容器中加入一定量的 CH3OH(g),反应T时刻测得各组分的浓度如下:
| 物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
| 浓度(mol/L) | 0.44 | 0.6 | 0.6 |
②若加入 CH3OH(g)后,经10min 反应达到平衡,此时c(CH3OH) =
③若反应达平衡后,温度不变,从体系中移走部分CH3OCH3,重新达到平衡后,CH3OH(g)的转化率
您最近一年使用:0次
名校
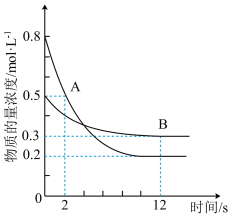
9 . 某温度下,在容积为2 L的密闭容器中投入一定量的A、B发生反应3A(g)+bB(g) cC(g) ΔH=-Q kJ·mol-1(Q>0),12 s时反应达到平衡,生成C的物质的量为0.8 mol,反应过程中A、B的物质的量浓度随时间的变化关系如图所示。下列说法正确的是
cC(g) ΔH=-Q kJ·mol-1(Q>0),12 s时反应达到平衡,生成C的物质的量为0.8 mol,反应过程中A、B的物质的量浓度随时间的变化关系如图所示。下列说法正确的是
 cC(g) ΔH=-Q kJ·mol-1(Q>0),12 s时反应达到平衡,生成C的物质的量为0.8 mol,反应过程中A、B的物质的量浓度随时间的变化关系如图所示。下列说法正确的是
cC(g) ΔH=-Q kJ·mol-1(Q>0),12 s时反应达到平衡,生成C的物质的量为0.8 mol,反应过程中A、B的物质的量浓度随时间的变化关系如图所示。下列说法正确的是
| A.前12 s内,A的平均反应速率为0.025 mol·L-1·s-1 |
| B.12 s后,A的消耗速率等于B的生成速率 |
| C.化学计量数之比b:c=1:4 |
| D.12 s内,A和B反应放出的热量为0.4Q kJ |
您最近一年使用:0次
2024-01-08更新
|
173次组卷
|
3卷引用:四川省成都石室中学2023-2024学年高二上学期期中考试化学试卷
名校
解题方法
10 . 天然气的主要成分为CH4,还含有C2H6等烃类,是重要的燃料和化工原料。
(1)乙烷在一定条件可发生如下反应:C2H6(g) C2H4(g)+H2(g)ΔH,相关物质的燃烧热数据如下表所示:
C2H4(g)+H2(g)ΔH,相关物质的燃烧热数据如下表所示:
①ΔH=___________ kJ•mol-1。
②提高该反应平衡转化率的方法有___________ 、___________ 。
(2)密闭容器中通入等物质的量的乙烷和氢气,在等温等压下(p)发生上述反应C2H6(g) C2H4(g)+H2(g)。
C2H4(g)+H2(g)。
①可判断该反应达平衡的标志为___________ (填选项字母)。
A.容器内混合气体的密度恒定
B.容器内混合气体的压强恒定
C.容器内乙烷和氢气的物质的量之比恒定
D.生成乙烯的速率和乙烷消耗的速率相等
②如果乙烷的平衡转化率为α,反应的平衡常数Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)高温下,甲烷生成乙烷的反应如下:2CH4 C2H6+H2,反应在初期阶段的速率方程为:r=kc(CH4),其中k为反应速率常数,设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=
C2H6+H2,反应在初期阶段的速率方程为:r=kc(CH4),其中k为反应速率常数,设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=___________ r1。
(4)CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:___________ 。
②若生成的乙烯和乙烷的体积比为2∶1,则消耗的CH4和CO2体积比为___________ 。
(1)乙烷在一定条件可发生如下反应:C2H6(g)
 C2H4(g)+H2(g)ΔH,相关物质的燃烧热数据如下表所示:
C2H4(g)+H2(g)ΔH,相关物质的燃烧热数据如下表所示:| 物质 | C2H6(g) | C2H4(g) | H2(g) |
| 燃烧热ΔH/(kJ•mol-1) | —1560 | —1411 | —286 |
②提高该反应平衡转化率的方法有
(2)密闭容器中通入等物质的量的乙烷和氢气,在等温等压下(p)发生上述反应C2H6(g)
 C2H4(g)+H2(g)。
C2H4(g)+H2(g)。①可判断该反应达平衡的标志为
A.容器内混合气体的密度恒定
B.容器内混合气体的压强恒定
C.容器内乙烷和氢气的物质的量之比恒定
D.生成乙烯的速率和乙烷消耗的速率相等
②如果乙烷的平衡转化率为α,反应的平衡常数Kp=
(3)高温下,甲烷生成乙烷的反应如下:2CH4
 C2H6+H2,反应在初期阶段的速率方程为:r=kc(CH4),其中k为反应速率常数,设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=
C2H6+H2,反应在初期阶段的速率方程为:r=kc(CH4),其中k为反应速率常数,设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=(4)CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:
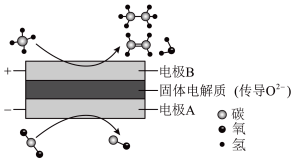
②若生成的乙烯和乙烷的体积比为2∶1,则消耗的CH4和CO2体积比为
您最近一年使用:0次