1 . 化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①哪一时间段反应速率最大___________ min(填“0~1”“1~2”“2~3”“3~4”或“4~5”),原因是___________ 。
②求2~3min时间段以盐酸的浓度变化来表示的该反应速率___________ (设溶液体积不变)。
(2)另一学生为了提高氢气的化学反应速率,他事先在盐酸中加入等体积的下列溶液以加快反应速率,你认为可行的是___________(填字母)。
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图所示:

①达到平衡状态时Z的浓度为___________ mol/L,该反应的化学方程式是___________ 。
②该反应达到平衡状态的标志是___________ (填字母)。
A.Y的体积分数在混合气体中保持不变 B.X、Y的反应速率比为3:1
C.容器内气体压强保持不变 D.容器内气体的平均相对分子质量保持不变
E.消耗1molY的同时消耗3molX
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL(标准状况) | 109 | 220 | 332 | 412 | 480 |
②求2~3min时间段以盐酸的浓度变化来表示的该反应速率
(2)另一学生为了提高氢气的化学反应速率,他事先在盐酸中加入等体积的下列溶液以加快反应速率,你认为可行的是___________(填字母)。
| A.蒸馏水 | B.KCl溶液 | C. 溶液 溶液 | D. 溶液 溶液 |

①达到平衡状态时Z的浓度为
②该反应达到平衡状态的标志是
A.Y的体积分数在混合气体中保持不变 B.X、Y的反应速率比为3:1
C.容器内气体压强保持不变 D.容器内气体的平均相对分子质量保持不变
E.消耗1molY的同时消耗3molX
您最近一年使用:0次
2022-06-08更新
|
204次组卷
|
3卷引用:山西省大同市灵丘一中、广灵一中2020-2021学年高一下学期期中联考化学试题
名校
2 . 2021年国务院政府工作报告明确提出要制定2030年前碳排放达峰行动方案。如何实现碳的氧化物的资源化利用解决温室效应问题是当前科学家亟待解决的问题。请回答下列问题:
(1)一定温度下,测得CO(g)、H2(g)和CH3OH(g)的燃烧热 分别为
分别为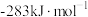 、
、 和
和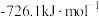 ,由
,由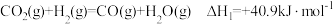 ,可知
,可知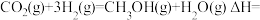
___________  。
。
(2)在恒温恒容条件下,下列不能说明反应 达到平衡状态的是
达到平衡状态的是
___________ (填序号)。
a.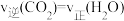 b.混合气体的密度不变
b.混合气体的密度不变
c.混合气体的平均摩尔质量不变 d.化学平衡常数不变
e.混合气体的压强不变
(3)在2L恒容密闭容器中分别加入2molCO2和6molH2,测得反应容器中CO2平衡转化率、CH3OH选择性、CO选择性随温度的变化关系如图所示[已知:CH3OH选择性=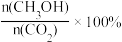 ]
]
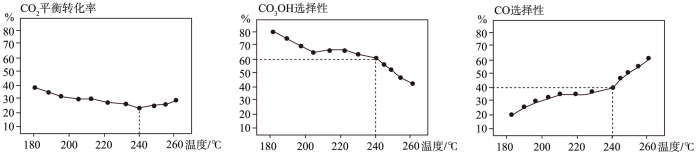
240℃时,10min后上述反应达到平衡,测得CO2平衡转化率为25%,CH3OH选择性为60%,则用CH3OH表示的化学反应速率为___________  ,反应
,反应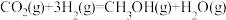 的平衡常数为
的平衡常数为___________ (用浓度列出表达式)。
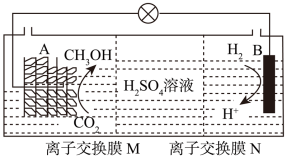
(4)利用电化学转化法,如图所示,在微生物的作用下,二氧化碳可自发地转化为甲醇,则电极A的名称为___________ 。
(1)一定温度下,测得CO(g)、H2(g)和CH3OH(g)的燃烧热
 分别为
分别为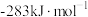 、
、 和
和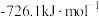 ,由
,由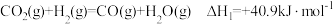 ,可知
,可知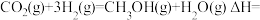
 。
。(2)在恒温恒容条件下,下列不能说明反应
 达到平衡状态的是
达到平衡状态的是a.
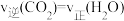 b.混合气体的密度不变
b.混合气体的密度不变c.混合气体的平均摩尔质量不变 d.化学平衡常数不变
e.混合气体的压强不变
(3)在2L恒容密闭容器中分别加入2molCO2和6molH2,测得反应容器中CO2平衡转化率、CH3OH选择性、CO选择性随温度的变化关系如图所示[已知:CH3OH选择性=
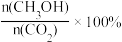 ]
]
240℃时,10min后上述反应达到平衡,测得CO2平衡转化率为25%,CH3OH选择性为60%,则用CH3OH表示的化学反应速率为
 ,反应
,反应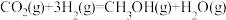 的平衡常数为
的平衡常数为(4)利用电化学转化法,如图所示,在微生物的作用下,二氧化碳可自发地转化为甲醇,则电极A的名称为

您最近一年使用:0次
解题方法
3 . 一定温度下,可逆反应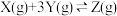 达到化学平衡状态的标志是
达到化学平衡状态的标志是
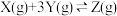 达到化学平衡状态的标志是
达到化学平衡状态的标志是A.X的生成速率是Z的分解速率 | B.单位时间消耗a mol X,同时消耗3a mol Y |
| C.X、Y、Z的浓度不再发生变化 | D.X、Y、Z的分子数比为1∶3∶2 |
您最近一年使用:0次
2022-01-06更新
|
163次组卷
|
5卷引用:山西省晋中市平遥县第二中学2021-2022学年高二上学期12月考试化学试题
名校
4 . 下列说法正确的是
| A.H2(g)+I2(g)⇌2HI(g),其他条件不变,缩小反应容器体积,正、逆反应速率不变,平衡不发生移动 |
| B.1molN2和3molH2反应达到平衡时H2转化率为10%,放出热量Q1;在相同温度和压强下,2molNH3分解为N2和H2的转化率为10%时,吸收热量Q2,Q2不等于Q1 |
| C.C(s)+H2O(g)⇌H2(g)+CO(g),碳的质量不再改变说明反应已达平衡 |
| D.若压强不再随时间变化能说明反应2A(?)+B(g)⇌2C(?)已达平衡,则A、C不能同时是气体 |
您最近一年使用:0次
名校
5 . 将装有 气体的圆底烧瓶(封口)置于冰水浴中,圆底烧瓶中气体颜色变浅。下列说法错误的是
气体的圆底烧瓶(封口)置于冰水浴中,圆底烧瓶中气体颜色变浅。下列说法错误的是
 气体的圆底烧瓶(封口)置于冰水浴中,圆底烧瓶中气体颜色变浅。下列说法错误的是
气体的圆底烧瓶(封口)置于冰水浴中,圆底烧瓶中气体颜色变浅。下列说法错误的是A.反应  |
| B.烧瓶内压强不再变化时,反应达到新的平衡 |
| C.气体颜色不再变化时,反应达到新的平衡 |
| D.混合气体的密度不再变化时,反应达到新的平衡 |
您最近一年使用:0次
2021-11-22更新
|
145次组卷
|
3卷引用:山西省运城市康杰中学2021-2022学年高二上学期期中化学试题
名校
解题方法
6 . 一定条件下,CH4与CO2反应可制备CH3COOH,反应的热化学方程式为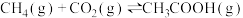 ,
,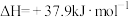 。回答下列问题:
。回答下列问题:
(1)若上述反应在恒容密闭容器中进行,则下列情况能说明反应已经达到平衡状态的是___________(填字母,下同)。
(2)下列措施既能提高CH4的平衡转化率又能加快反应速率的是___________。
(3)T1℃时催化剂作用下,将体积比为1:1的CH4与CO2混合气体充入恒容密闭容器中反应生成CH3COOH(g),每隔一定时间测得容器内气体压强如表所示:
①已知: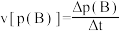 。反应开始10 min内,用CH4的压强变化表示该反应的平均反应速率为
。反应开始10 min内,用CH4的压强变化表示该反应的平均反应速率为___________  。
。
② ℃时,反应的平衡常数Kp=
℃时,反应的平衡常数Kp=___________  (Kp为用各气体分压表示的平衡常数,分压
(Kp为用各气体分压表示的平衡常数,分压 总压
总压 物质的量分数)。
物质的量分数)。
(4)用Co作催化剂,可使反应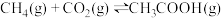 在较温和条件下进行,反应历程如图:
在较温和条件下进行,反应历程如图:
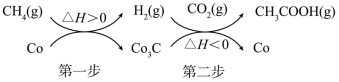
①第二步反应的化学方程式为___________ 。
②为增大CH3COOH的平衡产率:从温度角度考虑,第一步反应在高温下进行,第二步反应在___________ 进行;从H2浓度的角度考虑,第二步应采取的措施是___________ 。
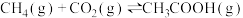 ,
,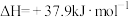 。回答下列问题:
。回答下列问题:(1)若上述反应在恒容密闭容器中进行,则下列情况能说明反应已经达到平衡状态的是___________(填字母,下同)。
| A.容器内气体密度保持不变 | B.CO2的体积分数保持不变 |
| C.该反应的平衡常数保持不变 | D.混合气体的平均相对分子质量不变 |
| A.升高温度 | B.使用高效催化剂 |
| C.加入CH4 | D.扩大容器体积 |
| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
| 压强/kPa | 2 | 1.5 | 1.3 | 1.2 | 1.2 | 1.2 |
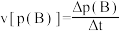 。反应开始10 min内,用CH4的压强变化表示该反应的平均反应速率为
。反应开始10 min内,用CH4的压强变化表示该反应的平均反应速率为 。
。②
 ℃时,反应的平衡常数Kp=
℃时,反应的平衡常数Kp= (Kp为用各气体分压表示的平衡常数,分压
(Kp为用各气体分压表示的平衡常数,分压 总压
总压 物质的量分数)。
物质的量分数)。(4)用Co作催化剂,可使反应
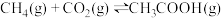 在较温和条件下进行,反应历程如图:
在较温和条件下进行,反应历程如图:
①第二步反应的化学方程式为
②为增大CH3COOH的平衡产率:从温度角度考虑,第一步反应在高温下进行,第二步反应在
您最近一年使用:0次
2021-11-11更新
|
179次组卷
|
2卷引用:山西省运城市康杰中学2021-2022学年高二上学期期中化学试题
解题方法
7 . 下列方法中可以证明2HI(气) H2(气)+I2(气)已达平衡状态的是
H2(气)+I2(气)已达平衡状态的是
①单位时间内生成nmolH2的同时生成nmolHI
②一个H-H键断裂的同时有两个H-I键断裂
③温度和压强一定时混合气体密度不再变化
④反应速率v(H2)=v(I2)=0.5v(HI)时
⑤c(HI):c(H2):c(I2)=2:1:1
⑥温度和体积一定时,某一生成物浓度不再变化
⑦温度和体积一定时,容器内压强不再变化
⑧条件一定,混合气体的平均相对分子质量不再变化
⑨温度和体积一定时混合气体的颜色不再变化
 H2(气)+I2(气)已达平衡状态的是
H2(气)+I2(气)已达平衡状态的是①单位时间内生成nmolH2的同时生成nmolHI
②一个H-H键断裂的同时有两个H-I键断裂
③温度和压强一定时混合气体密度不再变化
④反应速率v(H2)=v(I2)=0.5v(HI)时
⑤c(HI):c(H2):c(I2)=2:1:1
⑥温度和体积一定时,某一生成物浓度不再变化
⑦温度和体积一定时,容器内压强不再变化
⑧条件一定,混合气体的平均相对分子质量不再变化
⑨温度和体积一定时混合气体的颜色不再变化
| A.②③④⑤⑥ | B.②⑥⑦⑧⑨ | C.①②⑥⑧ | D.②⑥⑨ |
您最近一年使用:0次
2021-11-06更新
|
161次组卷
|
2卷引用:山西省太原市第五十六中学2021-2022学年高二上学期10月月考化学试题
解题方法
8 . 对于反应 ,判断下列说法正确的是
,判断下列说法正确的是
①单位时间内生成 ,同时生成
,同时生成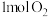 ,则处于化学平衡状态
,则处于化学平衡状态
② 的生成速率等于
的生成速率等于 的消耗速率,则处于化学平衡状态
的消耗速率,则处于化学平衡状态
③ 、
、 、
、 的体积分数不再发生变化,则处于化学平衡状态
的体积分数不再发生变化,则处于化学平衡状态
④气体的密度不变
⑤气体的压强不变
⑥气体的平均相对分子质量不变则处于化学平衡状态
 ,判断下列说法正确的是
,判断下列说法正确的是①单位时间内生成
 ,同时生成
,同时生成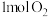 ,则处于化学平衡状态
,则处于化学平衡状态②
 的生成速率等于
的生成速率等于 的消耗速率,则处于化学平衡状态
的消耗速率,则处于化学平衡状态③
 、
、 、
、 的体积分数不再发生变化,则处于化学平衡状态
的体积分数不再发生变化,则处于化学平衡状态④气体的密度不变
⑤气体的压强不变
⑥气体的平均相对分子质量不变则处于化学平衡状态
| A.①③④⑥ | B.①②④⑤ | C.②③⑤⑥ | D.②③④⑥ |
您最近一年使用:0次
名校
解题方法
9 . 一定温度下的恒容密闭容器中,下列哪些物理量不再发生变化时,表明反应A(g)+2B(g)⇌C(g)+D(g)已达到化学平衡状态
①混合气体的压强②混合气体的密度③B的物质的量浓度④混合气体的总物质的量⑤混合气体的平均相对分子质量⑥混合气体的总质量
①混合气体的压强②混合气体的密度③B的物质的量浓度④混合气体的总物质的量⑤混合气体的平均相对分子质量⑥混合气体的总质量
| A.①②③④⑤⑥ | B.①③④⑤ | C.①②③④⑤ | D.②⑥ |
您最近一年使用:0次
2021-10-04更新
|
714次组卷
|
6卷引用:山西省怀仁市第一中学2021-2022学年高二上学期第二次月考理科综合化学试题
山西省怀仁市第一中学2021-2022学年高二上学期第二次月考理科综合化学试题(已下线)必考点03 化学平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)宁夏银川一中2021-2022学年高二上学期期中考试化学试题天津市实验中学滨海学校黄南民族班2021-2022学年高二上学期期中质量监测化学试题河南省温县第一高级中学2021-2022学年高二下学期开学考试化学试题(已下线)第13讲 第二章《化学反应速率与化学平衡》单元测试(基础巩固)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
2021高三·全国·专题练习
名校
10 . T℃,向体积为VL的密闭容器中充入NO,容器内各组分的物质的量随时间变化曲线如图所示。下列说法不正确的是
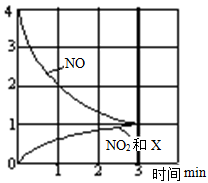

| A.X是N2O |
| B.1 min~3 min时,v(NO2)=1/6Vmol·(L·min)-1 |
| C.T℃时该反应的平衡常数为1 |
| D.NO2和X的浓度相等不可以作为判断反应到达平衡的标志 |
您最近一年使用:0次
2021-09-05更新
|
201次组卷
|
3卷引用:山西省运城市康杰中学2021-2022学年高二上学期期中化学试题
山西省运城市康杰中学2021-2022学年高二上学期期中化学试题(已下线)模块九 化学反应速率与化学平衡(模块检测)-2022年高考化学一轮复习小题多维练(全国通用)河南省范县第一中学2021-2022学年高二上学期第二次月考检测化学试题



