1 . 在容积为2.0 L的密闭容器中,通入一定量的N2O4,发生反应:N2O4 (g) 2NO2(g)。100℃时,各物质浓度随时间变化如下图所示。
2NO2(g)。100℃时,各物质浓度随时间变化如下图所示。
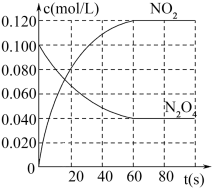
(1)60 s内,v(N2O4)=___________ 。
(2)下列叙述中,能说明该反应达到化学平衡状态的是___________(填字母序号)。
(3)降低温度,混合气体的颜色变浅,正反应是___________ 反应(填“放热”或“吸热”)。
(4)欲提高N2O4的平衡转化率,理论上可以采取的措施为___________ 。
A.增大压强 B.升高温度 C.加入催化剂
(5)100℃时,该反应的化学平衡常数的表达式为___________ ,数值为___________ ,请写出计算该平衡常数的三段式。
(6)平衡时,N2O4的转化率是___________ 。
(7)100℃时,在容器中按初始浓度c(N2O4)=0.10 mol/L、c(NO2)=0.10 mol/L投料,反应___________ 进行(填“正向”或“逆向”)。
 2NO2(g)。100℃时,各物质浓度随时间变化如下图所示。
2NO2(g)。100℃时,各物质浓度随时间变化如下图所示。
(1)60 s内,v(N2O4)=
(2)下列叙述中,能说明该反应达到化学平衡状态的是___________(填字母序号)。
| A.NO2的生成速率是N2O4的生成速率的2倍 |
| B.单位时间内消耗a mol N2O4,同时生成2a mol NO2 |
| C.容器内的压强不再变化 |
| D.容器内混合气体的密度不再变化 |
(3)降低温度,混合气体的颜色变浅,正反应是
(4)欲提高N2O4的平衡转化率,理论上可以采取的措施为
A.增大压强 B.升高温度 C.加入催化剂
(5)100℃时,该反应的化学平衡常数的表达式为
(6)平衡时,N2O4的转化率是
(7)100℃时,在容器中按初始浓度c(N2O4)=0.10 mol/L、c(NO2)=0.10 mol/L投料,反应
您最近一年使用:0次
2022-09-27更新
|
363次组卷
|
4卷引用:北京市中国农业大学附属中学2021-2022学年高二上学期期中学业水平调研化学试题
2 . 高炉炼铁是冶炼铁的主要方法,发生的主要反应为:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ΔH=akJ·mol-1。
2Fe(s)+3CO2(g) ΔH=akJ·mol-1。
(1)已知:
①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH1=+489.0kJ·mol-1
②C(石墨)+CO2(g)=2CO(g) ΔH2=+172.5kJ·mol-1
则a=_______ kJmol-1。
(2)冶炼铁反应的平衡常数表达式K=_______ ,温度升高后,K值_______ (填“增大”、“不变”或“减小”)。
(3)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
①甲容器中CO的平衡转化率为_______ 。
②下列说法正确的是_______ (填字母)。
a.若容器内气体密度恒定时,标志反应达到平衡状态
b.甲容器中CO的平衡转化率大于乙的
c.甲、乙容器中,CO的平衡浓度之比为2∶3
d.增加Fe2O3可以提高CO的转化率
 2Fe(s)+3CO2(g) ΔH=akJ·mol-1。
2Fe(s)+3CO2(g) ΔH=akJ·mol-1。(1)已知:
①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH1=+489.0kJ·mol-1
②C(石墨)+CO2(g)=2CO(g) ΔH2=+172.5kJ·mol-1
则a=
(2)冶炼铁反应的平衡常数表达式K=
(3)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
①甲容器中CO的平衡转化率为
②下列说法正确的是
a.若容器内气体密度恒定时,标志反应达到平衡状态
b.甲容器中CO的平衡转化率大于乙的
c.甲、乙容器中,CO的平衡浓度之比为2∶3
d.增加Fe2O3可以提高CO的转化率
您最近一年使用:0次
解题方法
3 . 工业上利用CO2和H2反应生成甲醇,也是减少CO2的一种方法。在容积为1L的恒温恒容密闭容器中充入1molCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(1)达到平衡的时刻是_______ min(填“3”或“10”)。在前10min内,用CO2浓度的变化表示的反应速率v(CO2)=_______ mol/(L·min)。
(2)能判断该反应达到化学平衡状态的依据是_______ 。
a.容器内压强不变 b.混合气体中c(CO2)不变
c.v(CH3OH)=v(H2O) d.混合气体的密度不变
(3)该反应的平衡常数表达式为_______ 。达平衡后,H2的转化率是_______ 。为了提高H2的转化率,可采取的措施有_______ (写出一种措施即可)。
(4)工业上也可用CO和H2合成甲醇
已知:①CO(g)+ O2(g)=CO2(g) △H1=-283.0kJ/mol
O2(g)=CO2(g) △H1=-283.0kJ/mol
②H2(g)+ O2(g)=H2O(g) △H2=-241.8kJ/mol
O2(g)=H2O(g) △H2=-241.8kJ/mol
③CH3OH(g)+ O2(g)=CO2(g)+2H2O(g) △H3=-192.2kJ/mol
O2(g)=CO2(g)+2H2O(g) △H3=-192.2kJ/mol
则反应CO(g)+2H2(g)=CH3OH(g) △H=_______ kJ/mol

(1)达到平衡的时刻是
(2)能判断该反应达到化学平衡状态的依据是
a.容器内压强不变 b.混合气体中c(CO2)不变
c.v(CH3OH)=v(H2O) d.混合气体的密度不变
(3)该反应的平衡常数表达式为
(4)工业上也可用CO和H2合成甲醇
已知:①CO(g)+
 O2(g)=CO2(g) △H1=-283.0kJ/mol
O2(g)=CO2(g) △H1=-283.0kJ/mol②H2(g)+
 O2(g)=H2O(g) △H2=-241.8kJ/mol
O2(g)=H2O(g) △H2=-241.8kJ/mol③CH3OH(g)+
 O2(g)=CO2(g)+2H2O(g) △H3=-192.2kJ/mol
O2(g)=CO2(g)+2H2O(g) △H3=-192.2kJ/mol则反应CO(g)+2H2(g)=CH3OH(g) △H=
您最近一年使用:0次
解题方法
4 . 对一定温度下的容积固定的密闭容器中,可逆反应:H2(g)+I2(g) 2HI(g),达到平衡的标志是
2HI(g),达到平衡的标志是
 2HI(g),达到平衡的标志是
2HI(g),达到平衡的标志是| A.压强不随时间的变化而变化 | B.混合气的平均相对分子质量一定 |
| C.生成n mol H2,同时生成2n mol HI | D.v(H2)=v(I2) |
您最近一年使用:0次
2022-09-15更新
|
251次组卷
|
3卷引用:北京市第四十四中学2021-2022学年高二上学期期中考试化学试题
北京市第四十四中学2021-2022学年高二上学期期中考试化学试题(已下线)专题04 可逆反应、化学平衡状态、化学平衡常数【考题猜想】(5大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)天津市第八中学2022-2023学年高二上学期期中检测化学试题
5 . 合成氨对人类的生存和发展有着重要意义,1909年哈伯在实验室中首次利用氮气与氢气反应合成氨,实现了人工固氮。
(1)反应N2(g)+3H2(g)⇌2NH3(g)的化学平衡常数表达式为_______ 。
(2)对于反应N2(g)+3H2(g)⇌2NH3(g),在一定条件下氨的平衡含量如下表。
①该反应为_______ (填“吸热”或“放热”)反应。
②其他条件不变时,温度升高氨的平衡含量减小的原因是_______ (填字母序号)。
a.温度升高,正反应速率减小,逆反应速率增大,平衡逆向移动
b.温度升高,浓度商(Q)变大,Q>K,平衡逆向移动
c.温度升高,活化分子数增多,反应速率加快
d.温度升高,K变小,平衡逆向移动
(3)一定温度下,在容积恒定的密闭容器中充入1 mol 氮气和3 mol氢气,一段时间后达化学平衡状态。若保持其他条件不变,向上述平衡体系中再充入1 mol氮气和3 mol 氢气,氮气的平衡转化率_______ (填“变大”“变小”或“不变”)。
(4)原料气H2可通过反应 CH4(g)+H2O(g)⇌CO(g) + 3H2(g)获取,已知该反应中当初始混合气中的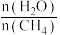 恒定时,温度、压强对平衡混合气CH4含量的影响如下图:
恒定时,温度、压强对平衡混合气CH4含量的影响如下图:
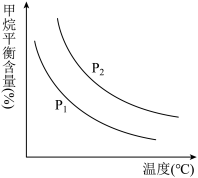
①图中,两条曲线表示压强的关系是:P1_______ P2(填“>”、“=”或“<”)。
②该反应为_______ 反应(填“吸热”或“放热”)。
(5)原料气H2还可通过反应CO(g)+H2O(g)⇌CO2(g)+H2(g)获取。
①T℃时,向容积固定为5 L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO的浓度为0.08 mol·L-1,则平衡时CO的转化率为_______ ,该温度下反应的平衡常数K值为_______ 。
②保持温度仍为T℃,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是_______ (填序号)。
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6
(1)反应N2(g)+3H2(g)⇌2NH3(g)的化学平衡常数表达式为
(2)对于反应N2(g)+3H2(g)⇌2NH3(g),在一定条件下氨的平衡含量如下表。
| 温度/℃ | 压强/MPa | 氨的平衡含量 |
| 200 | 10 | 81.5% |
| 550 | 10 | 8.25% |
②其他条件不变时,温度升高氨的平衡含量减小的原因是
a.温度升高,正反应速率减小,逆反应速率增大,平衡逆向移动
b.温度升高,浓度商(Q)变大,Q>K,平衡逆向移动
c.温度升高,活化分子数增多,反应速率加快
d.温度升高,K变小,平衡逆向移动
(3)一定温度下,在容积恒定的密闭容器中充入1 mol 氮气和3 mol氢气,一段时间后达化学平衡状态。若保持其他条件不变,向上述平衡体系中再充入1 mol氮气和3 mol 氢气,氮气的平衡转化率
(4)原料气H2可通过反应 CH4(g)+H2O(g)⇌CO(g) + 3H2(g)获取,已知该反应中当初始混合气中的
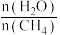 恒定时,温度、压强对平衡混合气CH4含量的影响如下图:
恒定时,温度、压强对平衡混合气CH4含量的影响如下图:
①图中,两条曲线表示压强的关系是:P1
②该反应为
(5)原料气H2还可通过反应CO(g)+H2O(g)⇌CO2(g)+H2(g)获取。
①T℃时,向容积固定为5 L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO的浓度为0.08 mol·L-1,则平衡时CO的转化率为
②保持温度仍为T℃,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6
您最近一年使用:0次
名校
6 . 将5mL0.1mol•L-1 KI溶液与1mL0.1mol•L-1 FeCl3溶液混合,发生反应a,一段时间后溶液颜色不再改变。将所得溶液分成两份,一份加淀粉,溶液变蓝;一份加KSCN,溶液变红。下列说法不正确的是
| A.加淀粉溶液变蓝,表明Fe3+与I-反应生成I2 |
| B.加KSCN溶液变红,表明反应a存在限度 |
| C.溶液的颜色不再变化,表明反应a达到平衡状态 |
| D.溶液的颜色不再变化,表明Fe2+、Fe3+、I2、I-的物质的量浓度均相等 |
您最近一年使用:0次
2022-07-07更新
|
345次组卷
|
3卷引用:北京市朝阳区2020-2021学年高一下学期期末化学试题
9-10高二下·浙江杭州·期中
名校
解题方法
7 . 在一定条件下,容器内某一反应中参加反应的气体M和气体N的物质的量随反应时间变化的曲线如图所示,下列表述中正确的是
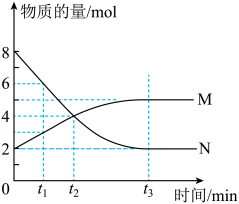

A.反应的化学方程式为2M N N |
| B.t2时,正、逆反应速率相等,达到平衡 |
| C.t3时,正反应速率大于逆反应速率 |
| D.t1时,N的浓度是M的浓度的2倍 |
您最近一年使用:0次
2022-07-06更新
|
1333次组卷
|
98卷引用:北京市第六十六中学2020-2021学年高一下学期期中考试化学试题
北京市第六十六中学2020-2021学年高一下学期期中考试化学试题北京市第一五六中学2021-2022学年高二上学期期中考试化学试题(已下线)专题06 化学反应速率和化学平衡——备战2021年高考化学纠错笔记北京东城区2019-2020学年高二下学期期中考试化学试题河南省信阳市浉河区新时代学校2020-2021学年高一下学期期中教学质量检化学试题广东省汕头市东方中学2020-2021学年高一下学期期中考试化学试题河南省周口市中英文学校2020-2021学年高一下学期期中考试化学试题(已下线)期末检测卷1 -2020-2021学年高一化学必修2章末集训必刷卷(人教版)云南省玉溪市江川区第二中学2020-2021学年高一下学期竞赛化学试题甘肃省永昌县第一高级中学2020-2021学年高一下学期期末考试化学试题河北省石家庄市第一中学2021-2022学年高二上学期开学考试化学试题广西桂林市第十八中学2021-2022学年高二上学期期中考试化学(理科)试题(已下线)2.2.2 化学平衡状态(1)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)广西贵港市江南中学2021-2022学年高二上学期12月月考化学(理科)试题北京市第四十三中学2021-2022学年高一下学期期中考试化学试题宁夏吴忠市吴忠中学2021-2022学年高二上学期月考化学试题甘肃省民勤县第四中学2021-2022学年高二上学期期中考试化学试题(已下线)2010年浙江省杭州地区七校联考高二第二学期期中化学试卷(已下线)2010年新疆农七师高级中学高一第二学期第二阶段考试化学试题(已下线)2009一2010年度吉林一中下学期高一期中考试化学卷(已下线)2010年河北省唐山一中高二上学期期中考试化学卷(已下线)2010—2011学年安徽省亳州市高二上学期期末考试化学试卷(已下线)2010—2011学年安徽省师大附中高二下学期期中考查化学试卷(已下线)2010—2011学年海南省洋浦中学高二上学期期末考试化学试卷(已下线)2010-2011学年湖北省襄阳四校高一下学期期中考试化学试卷(已下线)2010-2011学年江苏省盐城市伍佑中学高一下学期期中考试化学试卷(已下线)2010-2011学年广东省揭阳一中高一下学期期中考试化学试题(已下线)2010-2011学年浙江省宁波市高一下学期期末化学试卷(已下线)2011-2012学年河北省涿州二中高二上学期期中考试化学试卷(已下线)2012届福建省四地六校高三第三次月考化学试卷(已下线)2011-2012学年河南省焦作市修武一中分校高二上学期期中考试化学试卷(已下线)2011-2012年浙江永嘉县普高联合体高一下学期期中联考化学试卷(已下线)2011-2012年浙江温州龙湾中学高一期中考试理科化学试卷(已下线)2011-2012学年浙江省嘉兴八校高一下学期期中联考化学试卷(已下线)2011-2012学年浙江东阳中学、兰溪一中高一下学期期中考试化学卷 (已下线)2011-2012学年辽宁省沈阳二中高一下学期期中考试化学试卷(已下线)2011-2012学年河南省信阳高中高一下学期期中考试化学试卷(已下线)2011-2012学年福建省南安一中高一下学期期末考试化学试卷(已下线)2011-2012学年浙江省余姚中学高一下学期期中考试理科化学试卷(已下线)2011-2012年湖北宜昌金东方学校高二上学期期末考试化学试卷(已下线)2011-2012学年海南省洋浦中学高二下学期期末考试化学试卷(已下线)2012-2013学年陕西省长安一中高一下学期期中考试化学试卷(已下线)2012-2013学年宁夏育才中学高一下学期期中考试化学试卷2014-2015福建省泉州一中高三上学期期末考化学试卷2015-2016学年河南省漯河高中高一下期末化学试卷湖南省岳阳县第一中学2016-2017学年高一下学期期末考试化学试题江西省宜春市奉新县第一中学2016-2017学年高一下学期期末考试化学试题广西南宁市第二中学2016-2017学年高一下学期期末考试(理)化学试题甘肃省兰州新舟中学2017-2018学年高二上学期第二次月考化学试题安徽省滁州市民办高中2017-2018学年高一下学期第二次月考化学试题【全国百强校】贵州省思南中学2017-2018学年高一下学期期中考试化学试题【全国市级联考】广东省潮州市2017-2018学年高一下学期期末考试化学试题【全国百强校】甘肃省兰州第一中学2017-2018学年高一下学期期末考试化学试题河南省林州一中分校(林虑中学)2018-2019学年高二上学期8月调研考试化学试题云南省玉溪市新平县第一中学2018-2019学年高二入学分班考试化学试题2017-2018学年鲁科版选修4 第二单元第四节 化学反应条件的优化-工业合成氨练习题西藏自治区日喀则市南木林高级中学2018-2019学年高二上学期期中考试化学试题浙江省宁波市咸祥中学2018-2019学年高二上学期期中考试化学试题高二人教版选修4 第二章 第三节 化学平衡【全国百强校】内蒙古北方重工业集团有限公司第三中学2018-2019学年高一下学期期中考试化学试题重庆市四区2018-2019学年高一下学期高中联合调研评估测试(期末)化学试题重庆市大足区2018-2019学年高一下学期期末考试化学试题云南省楚雄市楚雄实验中学2018—2019学年高二上学期9月月考化学试题云南省普洱市普洱第二中学2019—2020学年高二上学期期末考试化学试题河北省邯郸市第一中学2019—2020学年高一4月月考化学试题山西省太原市第二十一中学2019-2020高一下学期期中考试化学试题陕西省渭南市三贤中学2020年高一下学期期中考试化学试题山东省临沂市2019-2020学年高一下学期月考化学试题山东济南市历城第二中学2019-2020学年高一下学期开学考试化学试题广西百色市2019-2020学年高二上学期期末考试化学试题吉林省长春外国语学校2019-2020学年高一下学期期末考试化学(理)试题黑龙江省肇州县第二中学2019-2020学年高一下学期6月月考化学试题北京师范大学珠海分校附属外国语学校2019-2020学年高一下学期期中考试化学试题高一必修第二册(人教2019版)第六章 第二节 化学反应的速率与限度 课时2 化学反应的限度(已下线)2.3.1+化学平衡状态-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)安徽省舒城中学2020-2021学年高二上学期第二次月考化学试题(已下线)2.3.1化学平衡状态(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)甘肃省庆阳市宁县第二中学2020-2021学年高二上学期第一次月考化学试题四川省自贡市富顺一中2020—2021学年度高二上学期期中考试化学试题黑龙江省伊春市伊美区第二中学2018-2019学年高二上学期阶段考试(12月)化学试题云南省大理州祥云县2019-2020学年高二下学期期末统测化学试题陕西省宝鸡市渭滨中学2021-2022学年高一下学期第一次月考化学试题河南省开封市五县部分学校2021-2022学年高一下学期期中考试化学试题广西三新教学质量测评2021-2022学年高一4月段考化学试题黑龙江省齐齐哈尔市恒昌中学校2021-2022学年高一下学期期中考试化学试题上海市同济大学第一附属中学2021-2022学年高一下学期等级阶段性测试2化学试题辽宁省营口市第二高级中学2021-2022学年高一6月月考化学试题云南省石屏县第一中学2021-2022学年高一下学期3月份考试化学试题云南省玉龙县第一中学2021-2022学年高二下学期3月份考试化学试题陕西省安康市汉滨区江北高级中学2020-2021学年高一下学期第二次月考化学试题安徽省滁州市定远县民族中学2021-2022学年高一下学期期中考试化学试题(已下线)2.2.3 化学反应速率和化学平衡图像——同步学习必备知识河南省驻马店市2022-2023学年高一下学期4月期中考试化学试题福建省厦门第一中学2022-2023学年高一下学期期中考试化学试题(已下线)第04讲 化学平衡状态 化学平衡常数-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)(已下线)第05练 化学反应的速率与限度-2023年【暑假分层作业】高一化学(人教版2019必修第二册)广东省汕头市澄海汇璟中学2021-2022学年高一下学期阶段素质监测化学试题云南省保山市腾冲市第八中学2022-2023学年高一下学期期中考试化学试卷
名校
解题方法
8 . 利用反应CO(g)+H2O(g) H2(g)+CO2(g)可得到清洁能源H2。
H2(g)+CO2(g)可得到清洁能源H2。
(1)该反应化学平衡常数表达式K=____ 。
(2)该反应的平衡常数随温度的变化如表:
从上表可以推断:此反应是____ (填“吸热”或“放热”)反应。
(3)830℃时,向容积为2L的密闭容器中充入1molCO与1molH2O,2min时CO为0.6mol。2min内v(CO2)=____ ,此时反应进行的方向是___ ,依据是____ ,可以判断该反应达到平衡的标志是____ (填字母)。
a.体系的压强不再发生变化 b.混合气体的密度不变
c.CO的消耗速率与CO2的消耗速率相等 d.各组分的物质的量浓度不再改变
 H2(g)+CO2(g)可得到清洁能源H2。
H2(g)+CO2(g)可得到清洁能源H2。(1)该反应化学平衡常数表达式K=
(2)该反应的平衡常数随温度的变化如表:
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
(3)830℃时,向容积为2L的密闭容器中充入1molCO与1molH2O,2min时CO为0.6mol。2min内v(CO2)=
a.体系的压强不再发生变化 b.混合气体的密度不变
c.CO的消耗速率与CO2的消耗速率相等 d.各组分的物质的量浓度不再改变
您最近一年使用:0次
2022-03-14更新
|
584次组卷
|
3卷引用:北京市日坛中学2021-2022学年高二上学期期中考试化学试题
北京市日坛中学2021-2022学年高二上学期期中考试化学试题(已下线)2.2.2 影响化学平衡的因素 -2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)吉林省普通高中友好学校联合体2023-2024学年高二上学期期中联考化学试题
9-10高二下·浙江宁波·期中
名校
解题方法
9 . 恒温条件下,可逆反应: 在体积固定的密闭容器中进行,达到平衡状态的标志是
在体积固定的密闭容器中进行,达到平衡状态的标志是
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
 在体积固定的密闭容器中进行,达到平衡状态的标志是
在体积固定的密闭容器中进行,达到平衡状态的标志是①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
| A.①④⑥⑦ | B.②⑤⑥⑦ | C.①③④⑤ | D.全部 |
您最近一年使用:0次
2022-01-22更新
|
2508次组卷
|
146卷引用:北京市第一五六中学2021-2022学年高二上学期期中考试化学试题
北京市第一五六中学2021-2022学年高二上学期期中考试化学试题甘肃省兰州市第四片区2020-2021学年高二上学期期末考试化学试题(人教版2019)必修第二册 第六章 化学反应与能量 第二节 化学反应的速率与限度人教版2019必修第二册 六章 第二节 第2课时 化学反应的限度黑龙江省龙东南六校2020-2021学年高二上学期期末联考化学试题黑龙江省鸡东二中2020-2021学年高二上学期期末考试化学试题西藏昌都市第三中学2020-2021学年高二上学期期末考试化学试题江苏省扬州中学2020-2021学年高一下学期期中考试化学试题江西省赣州市南康区第三中学2020-2021学年高一下学期期中考试化学试题河南省周口市中英文学校2020-2021学年高一下学期期中考试化学试题青海省西宁市海湖中学2021-2022学年高二上学期开学考试化学试题(已下线)第19讲 化学平衡 (练) — 2022年高考化学一轮复习讲练测(新教材新高考)甘肃省张掖二中 2020-2021学年高一下学期6月月考化学试题(已下线)选择性必修1 期中检测(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)河南省辉县市一中2020-2021学年高一下学期第一次阶段性考试化学试题湖南省长沙市长郡中学2021-2022学年高二上学期第一次月考化学试题福建省三明第一中学2021-2022学年高二上学期第一次月考化学试题四川省华蓥中学2020-2021学年高一下学期5月月考化学考试题福建省莆田市擢英中学2021-2022学年高二上学期第一次月考化学试卷重庆市朝阳中学2021-2022学年高二上学期期中考试化学试题浙江省温州市平阳县万全综合高级中学2021-2022学年高二上学期期中考试化学试题云南省楚雄天人中学2021-2022学年高二上学期12月月考化学试题(B卷)(已下线)2010年浙江省慈溪中学高二第二学期期中考试(普通班)化学试题(已下线)09-10年邯郸市高一下学期期末质量检测化学卷(已下线)2010年宁夏青铜峡市高级中学高一下学期期末考试化学试题(已下线)2010年山东省聊城四中高一第二学期期末考试化学试题(已下线)2010年福建省福州八中高二第二学期期末考试化学试题(已下线)2010年黑龙江省双鸭山一中高三上学期期中考试(化学)(已下线)2010年湖北省襄樊市四校联考-高二上学期期中考试化学卷(已下线)2010—2011学年安徽蚌埠二中第二学期高一期中考试化学试卷(已下线)2010—2011学年江西省白鹭洲中学高一下学期期中考试化学试卷(已下线)2010-2011学年陕西省勉县一中高一下学期期中考试化学试卷(已下线)2012届福建省龙岩一中高三第一学段考试化学试卷(已下线)2012届山东省淄博市第一中学高三上学期期中模块考试化学试卷(已下线)2011-2012学年安徽省濉溪县临涣中学高二上学期期中联考化学试卷(已下线)2011-2012学年河北省涿州二中高二上学期期中考试化学试卷(已下线)2011-2012学年云南省玉溪一中高二上学期期末考试化学试卷(已下线)2011-2012年浙江温州龙湾中学高一期中考试理科化学试卷(已下线)2011-2012学年江西省横峰中学高一下学期期中考试化学试卷(已下线)2011-2012学年湖北省襄阳市四校联考高一下学期期中考试化学试卷(已下线)2011-2012学年重庆市杨家坪中学高一下学期期中考试化学试卷(已下线)2011-2012学年浙江临海市白云高级中学高二下学期期中考试化学卷(已下线)2012年人教版高中化学必修二第二章 化学反应与能量练习卷(已下线)2013-2014学年江苏省常州市四校高二期中考试化学试卷(已下线)2013-2014浙江省温州中学高一下学期期中化学试卷(已下线)2013届江西省高安中学高一下学期期中考试试题化学试卷(已下线)2013-2014黑龙江省哈尔滨三中高一下学期期末考试化学试卷(已下线)2013-2014江西省上高二中高一下学期期末考试化学试卷(已下线)2014~2015学年江西四校9月联考高二化学试卷(已下线)2014秋安徽省淮北师范大学附属实验中学高二上学期期中化学试卷(已下线)2014-2015学年江西省景德镇市高二上学期期中化学(理)试卷(已下线)2015届浙江省桐乡一中等四校高三上学期期中联考化学试卷2014-2015学年广东省东莞市三校高二上学期期中联考化学试卷2015届河北省衡水冀州中学高三12月月考化学试卷2014-2015学年河南省扶沟县高级中学高一5月月考化学试卷2014-2015学年云南省玉溪市第一中学高一下期末化学试卷2015-2016学年河北省望都中学高二上学期第二次月考化学试卷2015-2016学年西藏日喀则高级中学高二上期末化学试卷2015-2016学年福建师大附中高一下期中化学试卷2015-2016学年广西河池高中高一下第二次月考化学试卷2015-2016学年辽宁省大连市二十中高一下期末化学试卷2017届山东省滕州市第二中学高三上学期10月月考化学试卷2016-2017学年天津市静海一中高二上9月调研化学试卷2016-2017学年河南省新乡市延津县中学高二上第一次月考化学卷2016-2017学年新疆生产建设兵团二中高二上期中化学卷新疆生产建设兵团第二中学2016-2017学年高一下学期第二次月考化学试题吉林省汪清县第六中学2016-2017学年高一下学期第二次月考化学试题云南省大理州南涧彝族自治县民族中学2016-2017学年高一下学期6月月考化学试题陕西省宝鸡中学2016-2017学年高一下学期期末考试化学试题河南省林州市第一中学分校(林虑中学)2017-2018学年高二上学期开学检测化学试题吉林省乾安县第七中学2017-2018学年高二上学期月考化学试题黑龙江省饶河县高级中学2017-2018学年高二上学期第一次月考化学试题云南省玉溪市民族中学2017-2018学年高二上学期期中考试化学试卷河南省豫北重点中学2017-2018学年高二12月联考化学试题湖南省临武一中、嘉禾一中2017-2018学年高二12月联考化学试题湖南省师范大学附属中学2017-2018学年高二上学期期末考试化学(理)试题河南省固始县2017-2018学年上期期末高中二年级期末化学试题河南省安阳市林虑中学2017-2018学年高二下学期开学考试化学试题【全国百强校】内蒙古集宁一中(东校区)2017-2018学年高一下学期期末考试化学试题吉林省榆树一中2017-2018学年高一下学期期末考试化学试题【全国百强校】内蒙古集宁一中(西校区)2017-2018学年高一下学期期末考试化学试题【全国百强校】安徽省安庆一中2017-2018学年高一下学期期末考试化学试题陕西省城固县第一中学2018-2019学年高二上学期开学考试化学试题【全国百强校】辽宁省实验中学2016-2017学年高一下学期期中考试化学试题【全国百强校】安徽省合肥市一六八中学2018-2019学年高二开学考试化学试题【全国百强校】黑龙江省鹤岗市第一中学2018-2019学年高二上学期第一次月考(10月)化学试题黑龙江省绥滨县第一中学2018-2019学年高二(理)上学期期中考试化学试题甘肃省岷县一中2018-2019学年高二上学期期中考试化学试题【全国百强校】山西省平遥中学2018-2019学年高二上学期期中考试化学试题湖北省利川市第五中学2018-2019学年高二上学期期中模拟考试化学试题新疆维吾尔自治区石河子二中2018-2019学年高二上学期第二次月考化学试题(已下线)2019年3月31日 《每日一题》 必修2 每周一测步步为赢 高一化学暑假作业:作业九 化学反应的限度新疆奎屯市第一高级中学2018-2019学年高一下学期第二次月考化学试题黑龙江省齐齐哈尔市第八中学2018-2019学年高一下学期期中考试化学试题安徽省黄山市屯溪第一中学2019-2020学年高二上学期入学摸底考试化学试题(已下线)2019年9月23日 《每日一题》2020年高考一轮复习-化学平衡状态的判断黑龙江省哈尔滨市第六中学2019-2020学年高二10月月考化学试题福建省漳州市长泰县第一中学2019-2020学年高二10月月考化学试题山西省应县第一中学校2019-2020学年高二上学期期中考试化学试题福建省泉州市永春华侨中学2019-2020学年高二上学期期中考试化学试题(已下线)专题7.2 化学平衡状态 化学平衡移动(练)-《2020年高考一轮复习讲练测》河北省宣化市第一中学2019-2020学年高一11月月考化学试题陕西省渭南韩城市2019-2020学年高二上学期期中考试化学试题新疆乌鲁木齐市第四中学2019-2020学年高二上学期期末考试化学试题吉林省四平市双辽市第二中学2019-2020学年高二上学期期末考试化学试题河北省邯郸市第一中学2019—2020学年高一4月月考化学试题山东省济宁市汶上圣泽中学2019-2020学年高一下学期第二次月考化学试题宁夏育才中学2019-2020学年高一下学期5月教学质量检测化学试题江苏省震泽中学2019-2020学年高一下学期期中考试(非杨班)化学试题江苏省泰州中学2019-2020学年高一下学期期中考试化学试题(已下线)【南昌新东方】2019-2020 南大附中 高一下 第三次月考宁夏回族自治区石嘴山市第三中学2019-2020学年高一下学期6月月考化学试题山东济南市历城第二中学2019-2020学年高一下学期开学考试化学试题(已下线)第06练化学反应的速率与限度-2020年【衔接教材·暑假作业】新高二化学(人教版)河北省衡水市桃城区第十四中学2019-2020学年高一下学期第五次综合测试化学试题(已下线)第02章 化学反应速率与化学平衡(A卷基础强化篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)黑龙江省实验中学2020-2021学年高二上学期期中考试化学试题(已下线)第23讲 化学平衡状态 化学平衡的移动(精练)-2021年高考化学一轮复习讲练测湖北省利川市第五中学2020-2021学年高二上学期期中考试化学试题吉林省长春市农安县2020-2021学年高二上学期期中考试化学试题贵州省毕节市七星关区毕节市实验高级中学2020-2021学年高二上学期期中考试化学试题湖北省黄冈麻城市第二中学2020-2021学年高二10月月考化学试题高中化学苏教2019版必修第二册-专题6 本专题复习提升云南省丽江市2019-2020学年高一下学期期末教学质量监测化学试题江西省新余市2021-2022学年高二上学期期末检测化学试题宁夏青铜峡市高级中学2021-2022学年高二下学期开学考试化学试题课后-6.2.2 化学反应的限度、化学反应条件的控制-人教2019必修第二册湖南省长沙市第一中学2021-2022学年高一下学期期中考试化学试题江苏省前黄高级中学2021-2022学年高一下学期4月调研考试化学试题江苏省海州高级中学2021-2022学年高一下学期期中考试化学试题黑龙江省齐齐哈尔市恒昌中学校2021-2022学年高一下学期期中考试化学试题新疆乌鲁木齐市第七十中学2021-2022学年高一下学期期中考试化学(理)试题河南省三门峡市第一高级中学2021-2022学年高一下学期5月月考化学试题河北省石家庄市新乐市第一中学2021-2022学年高一下学期第三次月考化学试题吉林省吉化第一高级中学校2021-2022学年高一下学期复课检测化学试题新疆乌鲁木齐市第四中学2021-2022学年高一下学期期末考试化学试题新疆乌鲁木齐市第七十中学2021-2022学年高一下学期期末考试化学试题黑龙江省双鸭山市集贤县一中、四中等2021-2022学年高一下学期期末考试化学试题广东省江门市新会陈经纶中学2021-2022学年高一下学期期中考试化学(选择考)试题吉林省白城市通榆县毓才高级中学2022-2023学年高二上学期第一次月考化学试题黑龙江省佳木斯市汤原县高级中学2021-2022学年高二上学期期末考试化学试题福建省安溪一中、养正中学、惠安一中、泉州实验中学2022-2023学年高二上学期期中考联考化学试题广西钦州市第四中学2023-2024学年高一下学期3月份考试化学试卷6.2.2 化学反应的限度 课堂例题河北省唐山市开滦第二中学2023-2024学年高一下学期4月月考化学试题
名校
解题方法
10 . 可逆反应2HI(g)  H2(g)+I2(g)在体积固定的密闭容器中,下列说法
H2(g)+I2(g)在体积固定的密闭容器中,下列说法不能 说明反应达到化学平衡状态的是
 H2(g)+I2(g)在体积固定的密闭容器中,下列说法
H2(g)+I2(g)在体积固定的密闭容器中,下列说法| A.混合气体的压强不再改变 |
| B.混合气体的颜色不再改变 |
| C.H2的体积分数不再变化 |
| D.HI的转化率不再改变 |
您最近一年使用:0次
2022-01-02更新
|
417次组卷
|
5卷引用:北京一零一中学2021-2022学年高二上学期期中考试化学试题



