1 . 下列操作或事实不能 用勒夏特列原理解释的是
A. ,把充有 ,把充有 的球浸泡在冰水中,气体颜色变浅 的球浸泡在冰水中,气体颜色变浅 |
| B.打开碳酸饮料瓶盖时,会有气泡冒出 |
| C.合成氨工业中,采用高温有利于提高生产效率 |
D.向含有 的红色溶液中加入铁粉,振荡,溶液颜色变浅或褪去 的红色溶液中加入铁粉,振荡,溶液颜色变浅或褪去 |
您最近半年使用:0次
2 . 一定条件下,1-苯基丙炔(Ph-C≡C-CH3)可与HCl发生催化加成,反应如下:

反应过程中该炔烃及反应产物的占比随时间变化如图(已知:反应Ⅰ、Ⅱ为放热反应,下列说法不正确的是

反应过程中该炔烃及反应产物的占比随时间变化如图(已知:反应Ⅰ、Ⅱ为放热反应,下列说法不正确的是
| A.反应焓变:反应Ⅰ>反应Ⅱ |
| B.反应活化能:反应Ⅰ<反应Ⅱ |
| C.增加HCl浓度可增加平衡时产物Ⅱ和产物Ⅰ的比例 |
| D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ |
您最近半年使用:0次
3 . 下列过程或现象不能用勒夏特列原理解释的是
| A.酸溶液遇紫色石蕊试剂变红 |
| B.可用浓氨水和氢氧化钠固体快速制取氨气 |
| C.CO2在水中的溶解度大于在NaHCO3溶液中的溶解度 |
| D.工业合成氨,反应条件选择500℃高温 |
您最近半年使用:0次
名校
4 . 下列事实不能用勒夏特列原理解释的是
| A.25℃时,纯水pH=7;100℃时,纯水的pH<7 |
B.实验室用过氧化氢制取氧气时,常常加入 固体 固体 |
| C.实验室常用排饱和食盐水的方法收集氯气 |
| D.新制的氯水在光照条件下颜色变浅 |
您最近半年使用:0次
解题方法
5 . 将二氧化碳转化为高附加值化学品是目前研究的热点之一,甲醇是重要的化工原料和优良的替代燃料,因此加氢制甲醇被广泛关注。在催化剂作用下主要发生以下反应。
Ⅰ.

Ⅱ.
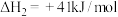
Ⅲ.

(1)反应Ⅲ自发进行的条件是______ 。
(2)恒温恒容条件下,原料气 、
、 以物质的量浓度1:3投料时,控制合适条件(不考虑反应Ⅲ),甲醇的选择性为
以物质的量浓度1:3投料时,控制合适条件(不考虑反应Ⅲ),甲醇的选择性为 。已知初始压强为
。已知初始压强为 ,
, ,
, 平衡转化率为
平衡转化率为 ,则该条件下反应Ⅱ
,则该条件下反应Ⅱ
______ 。(对于气相反应,用组分B的平衡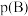 代替
代替 ,记作
,记作 。
。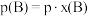 ,p为平衡压强,
,p为平衡压强,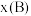 为平衡系统中
为平衡系统中 的物质的量分数。)
的物质的量分数。)
在 ,
, ,
, 、
、 以物质的量浓度1:3投料,以一定流速通过不同
以物质的量浓度1:3投料,以一定流速通过不同 与
与 催化剂,图a和b为催化反应
催化剂,图a和b为催化反应 转化率、甲醇选择性、甲醇收率随温度的变化,反应的产物只有甲醇、
转化率、甲醇选择性、甲醇收率随温度的变化,反应的产物只有甲醇、 和
和 。
。
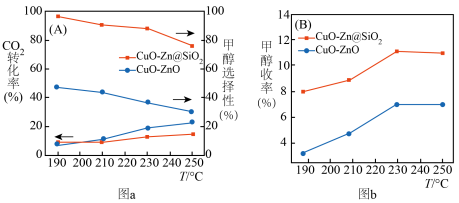
(3)分析在该压强下的最适合反应条件为______ 。
(4)推测在一定温度范围内,随着反应温度的升高, 转化率增大,但甲醇选择性降低的原因是
转化率增大,但甲醇选择性降低的原因是______ 。
(5)催化加氢的反应机理如下图所示。

下列说法正确的是_______
(6)在 催化剂条件下,保持流速与反应物投料比不变,增加反应物用量,请在图b上画出甲醇收率随温度变化曲线
催化剂条件下,保持流速与反应物投料比不变,增加反应物用量,请在图b上画出甲醇收率随温度变化曲线__________ 。
Ⅰ.


Ⅱ.

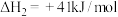
Ⅲ.


(1)反应Ⅲ自发进行的条件是
(2)恒温恒容条件下,原料气
 、
、 以物质的量浓度1:3投料时,控制合适条件(不考虑反应Ⅲ),甲醇的选择性为
以物质的量浓度1:3投料时,控制合适条件(不考虑反应Ⅲ),甲醇的选择性为 。已知初始压强为
。已知初始压强为 ,
, ,
, 平衡转化率为
平衡转化率为 ,则该条件下反应Ⅱ
,则该条件下反应Ⅱ
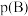 代替
代替 ,记作
,记作 。
。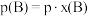 ,p为平衡压强,
,p为平衡压强,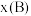 为平衡系统中
为平衡系统中 的物质的量分数。)
的物质的量分数。) 在
 ,
, ,
, 、
、 以物质的量浓度1:3投料,以一定流速通过不同
以物质的量浓度1:3投料,以一定流速通过不同 与
与 催化剂,图a和b为催化反应
催化剂,图a和b为催化反应 转化率、甲醇选择性、甲醇收率随温度的变化,反应的产物只有甲醇、
转化率、甲醇选择性、甲醇收率随温度的变化,反应的产物只有甲醇、 和
和 。
。
(3)分析在该压强下的最适合反应条件为
(4)推测在一定温度范围内,随着反应温度的升高,
 转化率增大,但甲醇选择性降低的原因是
转化率增大,但甲醇选择性降低的原因是(5)催化加氢的反应机理如下图所示。

下列说法正确的是_______
A. 催化剂中 催化剂中 抑制了 抑制了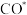 的解吸附,从而抑制 的解吸附,从而抑制 的生成。 的生成。 |
B. 催化剂上主要通过甲酸盐路径加氢生成甲醇。 催化剂上主要通过甲酸盐路径加氢生成甲醇。 |
| C.增大流速,原料气与催化剂碰撞机会多,甲醇产率一定增加。 |
D.随着温度升高,有利于 在催化剂表面反应,平衡转化率增大。 在催化剂表面反应,平衡转化率增大。 |
(6)在
 催化剂条件下,保持流速与反应物投料比不变,增加反应物用量,请在图b上画出甲醇收率随温度变化曲线
催化剂条件下,保持流速与反应物投料比不变,增加反应物用量,请在图b上画出甲醇收率随温度变化曲线
您最近半年使用:0次
6 . 氯化钠应用广泛,下列说法正确的是
A.侯氏制碱法是将足量 通入氨化的氯化钠饱和溶液中,析出 通入氨化的氯化钠饱和溶液中,析出 晶体 晶体 |
| B.氯碱工业采用阴离子交换膜电解槽电解饱和食盐水获得氯气和氢氧化钠 |
| C.用洗净的铂丝蘸取某样品在酒精灯上灼烧,火焰呈黄色,该样品一定是钠盐 |
| D.向饱和氯化钠溶液中滴加浓盐酸能观察到固体析出 |
您最近半年使用:0次
7 . 下列不能用勒夏特列原理解释的是
| A.打开汽水瓶时,有气泡冒出 |
B.可逆反应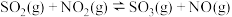 平衡后,缩小体积颜色加深 平衡后,缩小体积颜色加深 |
| C.氯水宜在避光、低温条件下保存 |
| D.用饱和食盐水除去氯气中的氯化氢杂质 |
您最近半年使用:0次
解题方法
8 . 下列说法正确的是
A.恒温恒容下,NH2COONH4(s)  2NH3(g)+CO2(g),当气体的平均相对分子质量不变时,可以判断该反应已经达到平衡 2NH3(g)+CO2(g),当气体的平均相对分子质量不变时,可以判断该反应已经达到平衡 |
B.恒温恒容下,X(g)+Y(g)  2Z(g)+N(s),当混合气体的密度不再发生变化时,能表明该反应达到平衡状态 2Z(g)+N(s),当混合气体的密度不再发生变化时,能表明该反应达到平衡状态 |
C.恒温恒容下,X(g)+Y(g)  2Z(g)+N(s)达到平衡,移走部分N,平衡向正反应方向移动 2Z(g)+N(s)达到平衡,移走部分N,平衡向正反应方向移动 |
D.N2(g)+3H2(g)  2NH3(g) ΔH<0,反应达到平衡后升温,则H2反应速率和平衡转化率均增大 2NH3(g) ΔH<0,反应达到平衡后升温,则H2反应速率和平衡转化率均增大 |
您最近半年使用:0次
9 . 对于反应:A(g)+B(g) 2C(g)+ D(s) △H<0,下列措施会使该反应的平衡正向移动的是
2C(g)+ D(s) △H<0,下列措施会使该反应的平衡正向移动的是
 2C(g)+ D(s) △H<0,下列措施会使该反应的平衡正向移动的是
2C(g)+ D(s) △H<0,下列措施会使该反应的平衡正向移动的是| A.升高温度 | B.分离出C |
| C.加入合适的催化剂 | D.恒压充入不参与反应的稀有气体 |
您最近半年使用:0次
10 . 下列实验方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 方案设计 | 现象和结论 |
| A | 探究反应物浓度对化学反应速率的影响 | 分别取 溶液和 溶液和 溶液、5mL蒸馏水于两支试管中,然后同时加入 溶液、5mL蒸馏水于两支试管中,然后同时加入 溶液 溶液 | 前者出现浑浊的时间更短,说明增大 浓度,可以加快反应速率影响 浓度,可以加快反应速率影响 |
| B | 探究反应物浓度对化学平衡的影响 | 取一支试管,加入 溶液,再向试管中滴加5~10滴 溶液,再向试管中滴加5~10滴 溶液。已知: 溶液。已知: | 溶液由黄色变为橙色,说明增大氢离子浓度,平衡向生成 的方向移动 的方向移动 |
| C | 探究生成物浓度对化学平衡的影响 | 向 溶液加入1滴KSCN溶液,再加入少量KCl溶液 溶液加入1滴KSCN溶液,再加入少量KCl溶液 | 若溶液先变血红色,加入KCl溶液后血红色变浅,说明增大生成物浓度,平衡逆向移动 |
| D | 探究催化剂对化学反应速率的影响 | 向两支盛有少量 溶液的试管中分别加入5滴 溶液的试管中分别加入5滴 溶液和5滴 溶液和5滴 溶液 溶液 | 加入 溶液的试管生成气体的速率比加入 溶液的试管生成气体的速率比加入 溶液的快,说明 溶液的快,说明 对 对 分解的催化效果强 分解的催化效果强 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-12-13更新
|
174次组卷
|
2卷引用:浙江省浙东北联盟(ZDB)2023-2024学年高二上学期期中考试化学试题



