12-13高二上·北京·期中
1 . 在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个恒压的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应C(g) A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡,下列说法中正确的是
A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡,下列说法中正确的是
 A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡,下列说法中正确的是
A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡,下列说法中正确的是| A.平均反应速度:乙>甲 | B.平衡时C的物质的量甲>乙 |
| C.平衡时C的转化率:乙<甲 | D.平衡时A的物质的量甲>乙 |
您最近一年使用:0次
2016-11-17更新
|
134次组卷
|
5卷引用:新疆维吾尔自治区巴州二中2021届高三第六次月考化学试题
新疆维吾尔自治区巴州二中2021届高三第六次月考化学试题(已下线)2011-2012学年北京市四中高二上学期期中测试化学试卷2015-2016学年甘肃兰州一中高二上期中测试理科化学试卷2016-2017学年贵州省思南中学高二上半期考试化学卷辽宁省本溪市第一中学2017-2018学年高二上学期第一次月考化学试题
名校
2 . 在特制的密闭真空容器中加入一定量纯净的氨基甲酸铵固体(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g) ΔH>0。下列说法中正确的是
2NH3(g)+CO2(g) ΔH>0。下列说法中正确的是
 2NH3(g)+CO2(g) ΔH>0。下列说法中正确的是
2NH3(g)+CO2(g) ΔH>0。下列说法中正确的是| A.密闭容器中气体的平均相对分子质量不变则该反应达到平衡状态 |
| B.该反应在任何条件下都能自发进行 |
| C.再加入一定量氨基甲酸铵,可加快反应速率 |
| D.保持温度不变,压缩体积,达到新的平衡时,NH3的浓度不变 |
您最近一年使用:0次
2017-08-30更新
|
1109次组卷
|
12卷引用:课时36 化学平衡及平衡移动-2022年高考化学一轮复习小题多维练(全国通用)
(已下线)课时36 化学平衡及平衡移动-2022年高考化学一轮复习小题多维练(全国通用)陕西省西安市雁塔区第二中学2021-2022学年高二上学期第一次月考化学试题辽宁省六校协作体2018届高三期初联考化学试题山东省济宁市邹城市兖矿第一中学2018-2019学年高二上学期期中模拟考化学试题鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 高考挑战区 过模拟山东师范大学附属中学2022-2023学年高二上学期第一次月考化学试题河北省石家庄新乐市第一中学2022-2023学年高二上学期第一次月考化学试题山东省2022-2023学年高二上学期学业水平测试化学试题(已下线)江苏省南京市盐城市2023届高三3月第二次模拟考试化学试题变式题(选择题6-10)福建省泉州市永春第一中学2022-2023学年高二下学期6月期末考试化学试题河南省南阳市第一中学校2023-2024学年高二上学期第一次月考化学试题山东省东明县第一中学2023-2024学年高二上学期10月月考化学试题
3 . 在容积一定的密闭器中发生可逆反应:A(g)+2B(g)  2C(g)
2C(g)  H=+Q(Q>0),条件变化时,影响平衡移动的关系如图所示。下列说法不正确的是
H=+Q(Q>0),条件变化时,影响平衡移动的关系如图所示。下列说法不正确的是

 2C(g)
2C(g)  H=+Q(Q>0),条件变化时,影响平衡移动的关系如图所示。下列说法不正确的是
H=+Q(Q>0),条件变化时,影响平衡移动的关系如图所示。下列说法不正确的是
A.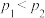 ,纵坐标指A的质量分数 ,纵坐标指A的质量分数 |
B. ,纵坐标指C的质量分数 ,纵坐标指C的质量分数 |
C. ,纵坐标指混合气体的平均摩尔质量 ,纵坐标指混合气体的平均摩尔质量 |
D. ,纵坐标指A的转化率 ,纵坐标指A的转化率 |
您最近一年使用:0次
2017-06-29更新
|
387次组卷
|
5卷引用:专题讲座(七) 常考速率、平衡图像题解题策略(精讲)-2022年一轮复习讲练测
(已下线)专题讲座(七) 常考速率、平衡图像题解题策略(精讲)-2022年一轮复习讲练测江西省玉山县第一中学2016-2017学年高一(19-31班)下学期期中考试化学试题北京市第161中学2017-2018学年高二上学期期中适应性训练化学试题鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第2节 化学反应的限度课时3 化学平衡图象新疆昌吉州教育共同体2020-2021学年高二上学期期中考试化学试题
13-14高二·全国·单元测试
名校
4 . 合成氨反应的正反应是气体体积减小的放热反应。合成氨工业的生产流程如下:
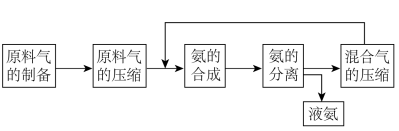
关于合成氨工业的说法中不正确的是( )

关于合成氨工业的说法中不正确的是( )
| A.混合气进行循环利用遵循绿色化学思想 |
| B.合成氨反应须在低温下进行 |
| C.对原料气进行压缩是为了增大原料气的转化率 |
| D.使用催化剂可以提高反应的速率,但是不能使平衡向正反应方向移动 |
您最近一年使用:0次
2016-12-09更新
|
1466次组卷
|
13卷引用:2.4 化学反应的调控-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)
(已下线)2.4 化学反应的调控-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)重庆市第七中学校2021-2022学年高二上学期第一次月考化学试题山东省济宁曲阜市第一中学2021-2022学年高二10月月考化学试题重庆市石柱中学校2021-2022学年高二上学期第一次月考化学试题(已下线)2014年高中化学鲁科版选修四第2章 反应的方向限度与速率练习卷2015-2016学年山东省武城县第二中学高二上学期第一次月考化学试卷云南省砚山县第二中学2019-2020学年高二上学期期末考试化学试题鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第4节 化学反应条件的优化—工业合成氨(已下线)第06练 化学反应的调控-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)(已下线)第29练 化学反应的调控-2023年高考化学一轮复习小题多维练(全国通用)辽宁省本溪市高级中学2024届高三适应性测试(一)化学试题(已下线)第5讲 化学反应的调控浙江省杭州第十一中学2023-2024学年高二上学期期末考试化学试题
5 . 在体积为V L的密闭容器中存在化学平衡:2NO2(g)⇌ N2O4(g)△H<0。现保持温度不变,将容器体积缩小一半后,下列说法不正确的是
| A.容器内气体颜色变深 |
| B.容器内NO2分子数减少 |
| C.混合气体的平均相对分子质量增大 |
| D.NO2的物质的量分数增大 |
您最近一年使用:0次
2017-01-06更新
|
396次组卷
|
4卷引用:福建省莆田第七中学2020-2021学年高二上学期期末考试化学试题
13-14高二下·江苏盐城·期中
名校
6 . 在25 ℃时,密闭容器中X、Y、Z三种气体的浓度变化情况如图,下列说法错误的是
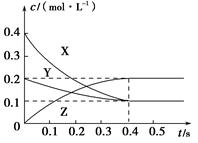

A.反应可表示为3X+Y 2Z 2Z |
| B.从反应开始到0.4 s时,以Y表示的化学反应速率为0.25 mol·L-1·s-1 |
| C.增大压强使平衡向生成Z的方向移动,正逆反应速率均增大 |
| D.升高温度,平衡常数一定增大 |
您最近一年使用:0次
2016-12-09更新
|
919次组卷
|
6卷引用:2021年河北省高考化学试卷变式题10-18题
2021年河北省高考化学试卷变式题10-18题(已下线)2013-2014江苏省盐城中学第二学期期中考试高二化学试卷(已下线)2014届江苏省盐城中学第二学期期中考试高二化学试卷江西省南昌市进贤县第一中学2019-2020学年高二上学期期中考试化学试题(已下线)【南昌新东方】2019 进贤一中 高二上 期中江西省宜春市第九中学2020-2021学年高二上学期期中考试化学试题
名校
7 . 请回答下列问题
(1)已知:25℃时,0.1 mol·L-1的HA溶液中c(H+)/c(OH-)=1010。
①HA是________ (填“强电解质”或“弱电解质”);
②在加水稀释HA溶液的过程中,随着水量的增加而减小的是________ (填字母)。
A.c(H+)/c(HA) B.c(HA)/ c (A-)
C.c(H+)与c(OH-)的乘积 D.c(OH-)
③若M溶液是由上述HA溶液V1 mL与pH = 12的NaOH溶液V2 mL混合充分反应而得,则下列说法中正确的是_______ (填字母)。
A.若溶液M呈中性,则溶液M中c(H+) + c(OH-) = 2.0×10-7 mol·L-1
B.若V1 =V2 ,则溶液M的pH一定等于7
C.若溶液M呈酸性,V1一定大于V2
D.若溶液M呈碱性,V1一定小于V2
(2)若已知在25℃,AgCl的Ksp = 1.8×10-10,现将足量AgCl分别放入:①100 mL 蒸馏水中;②100 mL 0.2mol·L-1 AgNO3溶液中;③100 mL 0.1mol·L-1 AlCl3溶液中;④100 mL 0.1mol·L-1盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是__________ (用序号连接)
(3)对于2NO2(g) N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是
N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是____ 。

①A、C两点的反应速率:A>C
②A、C两点气体的颜色:A深、C浅
③B、C两点的气体的平均分子质量:B<C
④由状态B到状态A,可以用加热方法
(1)已知:25℃时,0.1 mol·L-1的HA溶液中c(H+)/c(OH-)=1010。
①HA是
②在加水稀释HA溶液的过程中,随着水量的增加而减小的是
A.c(H+)/c(HA) B.c(HA)/ c (A-)
C.c(H+)与c(OH-)的乘积 D.c(OH-)
③若M溶液是由上述HA溶液V1 mL与pH = 12的NaOH溶液V2 mL混合充分反应而得,则下列说法中正确的是
A.若溶液M呈中性,则溶液M中c(H+) + c(OH-) = 2.0×10-7 mol·L-1
B.若V1 =V2 ,则溶液M的pH一定等于7
C.若溶液M呈酸性,V1一定大于V2
D.若溶液M呈碱性,V1一定小于V2
(2)若已知在25℃,AgCl的Ksp = 1.8×10-10,现将足量AgCl分别放入:①100 mL 蒸馏水中;②100 mL 0.2mol·L-1 AgNO3溶液中;③100 mL 0.1mol·L-1 AlCl3溶液中;④100 mL 0.1mol·L-1盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是
(3)对于2NO2(g)
 N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是
N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是
①A、C两点的反应速率:A>C
②A、C两点气体的颜色:A深、C浅
③B、C两点的气体的平均分子质量:B<C
④由状态B到状态A,可以用加热方法
您最近一年使用:0次
2016-12-09更新
|
248次组卷
|
3卷引用:江西省吉安市永新中学2021-2022学年高二上学期期中考试化学(理科)试题
13-14高二上·山东临沂·阶段练习
名校
8 . 在密闭容器中发生如下反应:xA(g)+yB(g)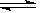 zC(g),达到平衡后测得A的浓度为0.20mol/L。在恒温下增大压强使容器容积缩小为原来的一半,再次达到平衡时,测得A的浓度为0.35mol/L。下列说法不正确的是
zC(g),达到平衡后测得A的浓度为0.20mol/L。在恒温下增大压强使容器容积缩小为原来的一半,再次达到平衡时,测得A的浓度为0.35mol/L。下列说法不正确的是
 zC(g),达到平衡后测得A的浓度为0.20mol/L。在恒温下增大压强使容器容积缩小为原来的一半,再次达到平衡时,测得A的浓度为0.35mol/L。下列说法不正确的是
zC(g),达到平衡后测得A的浓度为0.20mol/L。在恒温下增大压强使容器容积缩小为原来的一半,再次达到平衡时,测得A的浓度为0.35mol/L。下列说法不正确的是| A.x+y﹥z | B.平衡向右移动 | C.B的转化率提高 | D.C的体积分数降低 |
您最近一年使用:0次
2016-12-09更新
|
802次组卷
|
7卷引用:江苏省沭阳县修远中学2020-2021学年高二下学期第一次联考化学试题
11-12高三上·辽宁·期中
名校
9 . 在一定温度下的密闭容器中,加入1 mol CO和1 mol H2O发生反应:CO(g)+H2O(g) CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的
CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的
 CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的
CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的| A.在该温度下平衡常数K=1 | B.平衡常数与反应温度无关 |
| C.CO的转化率为50% | D.其他条件不变,改变压强平衡不移动 |
您最近一年使用:0次
2016-11-14更新
|
195次组卷
|
9卷引用:陕西省咸阳市泾干中学2021-2022学年高二上学期第二次月考化学试题
陕西省咸阳市泾干中学2021-2022学年高二上学期第二次月考化学试题(已下线)2012届辽宁省辽南协作体高三上学期期中考试化学试卷(已下线)2011-2012学年陕西省师大附中高一下学期期末考试化学试卷(已下线)2013-2014河南师大附中第一学期期中考试高二化学试卷2016-2017学年河南省师大附中高二上期中化学试卷浙江省诸暨市牌头中学2017-2018学年高一下学期期中考试(A)化学试题湖南省娄底市第四中学2018-2019学年高二上学期10月月考化学试题北京市延庆区2019-2020学年高二下学期期末考试化学试题江苏省徐州市睢宁县第一中学2021-2022学年高二下学期第一次月考化学试题
13-14高三上·北京朝阳·期中
名校
10 . N2O5是一种新型硝化剂,在一定温度下可发生以下反应:
2N2O5(g)⇌4NO2(g)+ O2(g) ΔH>0
T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:
下列说法中不正确的是
2N2O5(g)⇌4NO2(g)+ O2(g) ΔH>0
T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:
| 时间/s | 0 | 500 | 100 0 | 150 0 |
| c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
| A.500 s内N2O5分解速率为2.96×10-3mol·L-1·s-1 |
| B.T1温度下的平衡常数为K1=125,平衡时N2O5的转化率为50% |
| C.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2 |
D.达平衡后其他条件不变,将容器的体积压缩到原来的 ,则再次平衡时c(N2O5)> 5.00 mol·L-1 ,则再次平衡时c(N2O5)> 5.00 mol·L-1 |
您最近一年使用:0次
2014-07-16更新
|
194次组卷
|
14卷引用:黑龙江省龙东南六校2020-2021学年高二上学期期末联考化学试题
黑龙江省龙东南六校2020-2021学年高二上学期期末联考化学试题云南省富宁县一中2020-2021学年高二下学期第一次月考化学试题陕西省西安市雁塔区第二中学2021-2022学年高二上学期第一次月考化学试题(已下线)2014届学年北京市朝阳区高三上学期期中考试化学试卷(已下线)2014届江西省新余市高三上学期期末质量检测化学试卷(已下线)2014湖南长沙市长郡中学高三上学期第四次月考化学试卷2014-2015吉林省延边二中高二12月阶段考试化学试卷2015届河北省冀州中学高三上学期第四次月考化学试卷2015届北京市大兴区高三上学期期末考试化学试卷2014-2015福建省福州市第八中学高二下学期期中化学试卷2016届山东省枣庄三中高三上学期12月质检化学试卷福建省莆田第一中学2017-2018学年高二下学期期初考试化学试题福建省莆田九中2019-2020学年高二上学期期中考试化学试题浙江省北斗联盟2020-2021学年高二上学期期中联考化学试题



