名校
1 . 已知2A(g)  3B(s)+C(g) ΔH<0, 假设ΔH和ΔS不随温度而改变,下列说法中正确的是
3B(s)+C(g) ΔH<0, 假设ΔH和ΔS不随温度而改变,下列说法中正确的是
 3B(s)+C(g) ΔH<0, 假设ΔH和ΔS不随温度而改变,下列说法中正确的是
3B(s)+C(g) ΔH<0, 假设ΔH和ΔS不随温度而改变,下列说法中正确的是| A.低温下能自发进行 |
| B.高温下能自发进行 |
| C.任何温度下都能自发进行 |
| D.任何温度下都不能自发进行 |
您最近一年使用:0次
2022-01-18更新
|
260次组卷
|
2卷引用:安徽省宿州市十三所重点中学2021-2022学年高二上学期期末质量检测(理科人教版)化学试题
名校
2 . 在2 L密闭容器中充入气体A和B,发生反应A(g)+B(g)  C(g)+2D(g) ΔH,所得实验数据如下表。下列说法不正确的是
C(g)+2D(g) ΔH,所得实验数据如下表。下列说法不正确的是
 C(g)+2D(g) ΔH,所得实验数据如下表。下列说法不正确的是
C(g)+2D(g) ΔH,所得实验数据如下表。下列说法不正确的是| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(A) | n(B) | n(C) | ||
| ① | 300 | 0.40 | 0.10 | 0.09 |
| ② | 500 | 0.40 | 0.10 | 0.08 |
| ③ | 500 | 0.20 | 0.05 | a |
| A.ΔH<0 |
| B.500 ℃该反应的平衡常数K=0.16 |
| C.③中达到平衡时,A的转化率大于20% |
| D.5 min末测得①中n(C)=0.05 mol,则0到5 min内v(D)=0.005mol·L-1·min-1 |
您最近一年使用:0次
名校
3 . 下列说法正确的是
| A.CaCO3(s)=CaO(s)+CO2(g) △H=+178.5kJ·mol-1,该反应低温才能自发 |
| B.需要加热才能发生的反应一定是吸热反应 |
| C.在任何条件下,化学反应的焓变都等于化学反应的反应热 |
| D.常温下,反应A(s)+B(g)=2X(g)不能自发进行,则该反应的ΔH>0 |
您最近一年使用:0次
解题方法
4 . 下列说法错误的是
| A.1 mol H2O在不同状态时的熵值:S[H2O(s)]<S[H2O(g)] |
| B.合成氨反应,加入合适的催化剂能降低反应的活化能,从而改变反应的焓变 |
C.CaCO3(s)  CaO(s)+CO2(g) ΔH>0 能否自发进行与温度有关 CaO(s)+CO2(g) ΔH>0 能否自发进行与温度有关 |
| D.常温下,反应C(s) +CO2(g) =2CO(g)不能自发进行,则该反应的ΔH>0 |
您最近一年使用:0次
2021-12-21更新
|
151次组卷
|
2卷引用:安徽省滁州九校2021-2022学年高二上学期第四次调研考试化学试题
名校
5 . 在25℃, 条件下,下列熵值的大小比较正确的是
条件下,下列熵值的大小比较正确的是
 条件下,下列熵值的大小比较正确的是
条件下,下列熵值的大小比较正确的是A. | B.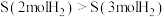 |
C.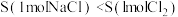 | D. |
您最近一年使用:0次
名校
解题方法
6 . 氢气在社会发展中有着重要的作用,如新能源的开发,氢能源的储存一直是科学界在研究的方向
Ⅰ.利用氨热分解法制氢气是可行方法之一
一定条件下,利用催化剂将氨气分解为氮气和氢气。相关化学键的键能数据:
(1)已知该反应的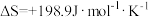 ,在下列哪个温度下反应能自发进行?___________(填标号)(已知:
,在下列哪个温度下反应能自发进行?___________(填标号)(已知: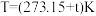 )
)
(2)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将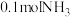 通入3L的密闭容器中进行反应(此时容器内总压为200kPa),部分物质的分压随时间的变化曲线如图所示。
通入3L的密闭容器中进行反应(此时容器内总压为200kPa),部分物质的分压随时间的变化曲线如图所示。
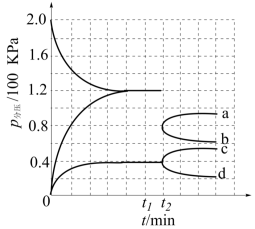
①若保持容器体积不变,t1时反应达到平衡,用H2的分压变化表示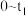 时间内的反应速率是
时间内的反应速率是___________ 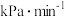
②t2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 分压变化趋势的曲线是
分压变化趋势的曲线是___________ (用图中a、b、c、d表示),理由是___________
③该温度下,反应标准平衡常数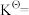
___________ 。(已知:分压=总压×该组分物质的量分数,对于反应 ,其中
,其中 ,
,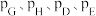 为各组分的平衡分压)。
为各组分的平衡分压)。
Ⅱ.下列是大规模制取H2的方法之一: 在一定体积的密闭容器中,其化学平衡常数K和温度T的关系如下表:
在一定体积的密闭容器中,其化学平衡常数K和温度T的关系如下表:
请回答下列问题:
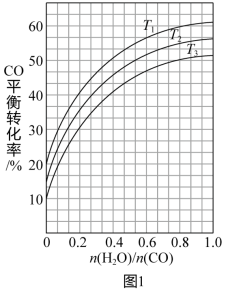
(3)图1表示不同温度条件下,CO平衡转化率随着 的变化趋势。判断T1、T2和T3的大小关系并说明理由:
的变化趋势。判断T1、T2和T3的大小关系并说明理由:___________
(4)实验发现,其它条件不变,在相同时间内,向反应体系中投入一定量的CaO可以增大H2的体积分数,理由是:___________ ,实验结果如图2所示。(已知:1微米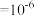 米,1纳米
米,1纳米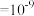 米)。投入纳米CaO比微米CaO,H2的体积分数更高的原因是
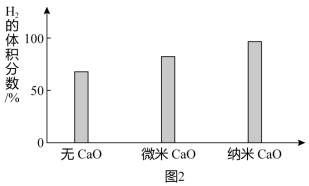
米)。投入纳米CaO比微米CaO,H2的体积分数更高的原因是___________
Ⅰ.利用氨热分解法制氢气是可行方法之一
一定条件下,利用催化剂将氨气分解为氮气和氢气。相关化学键的键能数据:
| 化学键 |  | H-H | N-H |
| 键能kJ/mol | 946 | 436.0 | 390.08 |
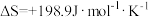 ,在下列哪个温度下反应能自发进行?___________(填标号)(已知:
,在下列哪个温度下反应能自发进行?___________(填标号)(已知: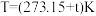 )
)| A.50℃ | B.100℃ | C.150℃ | D.200℃ |
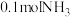 通入3L的密闭容器中进行反应(此时容器内总压为200kPa),部分物质的分压随时间的变化曲线如图所示。
通入3L的密闭容器中进行反应(此时容器内总压为200kPa),部分物质的分压随时间的变化曲线如图所示。
①若保持容器体积不变,t1时反应达到平衡,用H2的分压变化表示
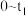 时间内的反应速率是
时间内的反应速率是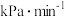
②t2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后
 分压变化趋势的曲线是
分压变化趋势的曲线是③该温度下,反应标准平衡常数
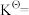
 ,其中
,其中 ,
,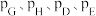 为各组分的平衡分压)。
为各组分的平衡分压)。Ⅱ.下列是大规模制取H2的方法之一:
 在一定体积的密闭容器中,其化学平衡常数K和温度T的关系如下表:
在一定体积的密闭容器中,其化学平衡常数K和温度T的关系如下表:| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 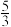 | 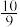 | 1.0 |  | 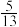 |
(3)图1表示不同温度条件下,CO平衡转化率随着
 的变化趋势。判断T1、T2和T3的大小关系并说明理由:
的变化趋势。判断T1、T2和T3的大小关系并说明理由:
(4)实验发现,其它条件不变,在相同时间内,向反应体系中投入一定量的CaO可以增大H2的体积分数,理由是:
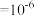 米,1纳米
米,1纳米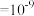 米)。投入纳米CaO比微米CaO,H2的体积分数更高的原因是
米)。投入纳米CaO比微米CaO,H2的体积分数更高的原因是
您最近一年使用:0次
名校
解题方法
7 . 下列说法正确的是
| A.凡是放热反应都是自发的,因为吸热反应都是非自发的 |
| B.自发反应的熵一定增大,非自发反应的熵一定减小 |
C.常温下,反应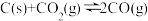 不能自发进行,则该反应的 不能自发进行,则该反应的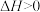 |
D.反应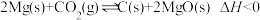 ,则该反应能在高温自发进行 ,则该反应能在高温自发进行 |
您最近一年使用:0次
2021-11-20更新
|
258次组卷
|
2卷引用:安徽省芜湖市第一中学2021-2022学年高二上学期第一次月末诊断测试化学试题
8 . 下列说法正确的是
| A.在合成氨工业中,移走NH3可增大正反应速率,提高原料转化率 |
B.恒温下进行的反应 达平衡时,缩小容器体积再达平衡时,气体的颜色比第一次平衡时的深,NO2的体积分数比原平衡大 达平衡时,缩小容器体积再达平衡时,气体的颜色比第一次平衡时的深,NO2的体积分数比原平衡大 |
C.常温下,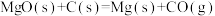 不能自发进行,则其 不能自发进行,则其 |
| D.在相同温度下,物质的量浓度相等的氨水、NaOH溶液,c(OH-)相等 |
您最近一年使用:0次
解题方法
9 . 下列说法正确的是
A. 在常温下可自发进行,则该反应的 在常温下可自发进行,则该反应的 |
B.一定条件下反应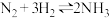 达到平衡时,3v正(H2)=2v逆(NH3) 达到平衡时,3v正(H2)=2v逆(NH3) |
C.向 溶液中加入少量水,溶液中 溶液中加入少量水,溶液中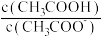 比值减小 比值减小 |
| D.Na2O2与足量的水反应生成0.2 mol O2,转移电子数目为0.8 NA |
您最近一年使用:0次
名校
10 . 在25℃,101kPa条件下,下列熵值的大小比较正确的是
| A.S(1molH2)>S(1molSO2) | B.S(2molH2)>S(3molH2) |
| C.S(2molNaCl)<S(1molCl2) | D.S(1molCaO)>S(1molCaCO3) |
您最近一年使用:0次
2021-11-15更新
|
65次组卷
|
2卷引用:安徽省A10联盟2021-2022学年高二上学期期中联考化学试题



