1 . 如图是元素周期表的一部分。回答下列问题:
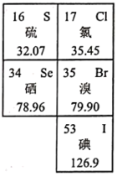
(1)溴被称为海洋元素。
①溴在元素周期表中位于第___________ 周期___________ 族。
②表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是___________ (填化学式)。
③能够证明溴单质的氧化性强于碘单质的离子方程式是___________ 。
(2)硒是人体必需的微量元素。
①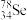 与
与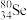 互称为
互称为___________ 。
②元素的气态氢化物的化学式为___________ 。
③SeO2溶于水生成H2SeO3,向所得溶液中通入SO2气体发生反应,生成硒单质和H2SO4.写出SO2与H2SeO3的反应方程式:___________ 。
(3)溴化硒是一种重要的电子元件材料,其分子的球棍模型如图所示。下列说法正确的是___________ (填字母)。
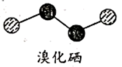
a.溴化硒属于离子化合物 b.原子半径r:r(Se)>r(Br)
c. Se元素的非金属性比Br的强 d.溴化硒的相对分子质量为317.72

(1)溴被称为海洋元素。
①溴在元素周期表中位于第
②表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是
③能够证明溴单质的氧化性强于碘单质的离子方程式是
(2)硒是人体必需的微量元素。
①
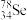 与
与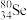 互称为
互称为②元素的气态氢化物的化学式为
③SeO2溶于水生成H2SeO3,向所得溶液中通入SO2气体发生反应,生成硒单质和H2SO4.写出SO2与H2SeO3的反应方程式:
(3)溴化硒是一种重要的电子元件材料,其分子的球棍模型如图所示。下列说法正确的是

a.溴化硒属于离子化合物 b.原子半径r:r(Se)>r(Br)
c. Se元素的非金属性比Br的强 d.溴化硒的相对分子质量为317.72
您最近一年使用:0次
2021-01-27更新
|
241次组卷
|
2卷引用:江苏省连云港市2020-2021学年高一上学期期末调研考试化学试题
2 . 表中为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语 回答下列问题:
(1)元素⑥位于第___________ 周期,第___________ 族,原子结构示意图___________ 。
(2)④、⑤、⑥的原子半径由大到小的顺序为___________ 。(用元素符号回答)。
(3)②、③、⑦的非金属性由强到弱顺序是___________ 。(用元素符号回答)
(4)⑨元素所形成单质的电子式为___________ 。
(5)⑥的单质与①、⑨两种元素形成化合物的水溶液反应的离子方程式为:___________ 。
(6)②元素与④元素形成的化合物中,化学键类型为___________ 。
 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)元素⑥位于第
(2)④、⑤、⑥的原子半径由大到小的顺序为
(3)②、③、⑦的非金属性由强到弱顺序是
(4)⑨元素所形成单质的电子式为
(5)⑥的单质与①、⑨两种元素形成化合物的水溶液反应的离子方程式为:
(6)②元素与④元素形成的化合物中,化学键类型为
您最近一年使用:0次
名校
3 . 下表是元素周期表的一部分,表中所列字母分别代表某一化学元素。回答问题:

(1)有人认为在元素周期表中,有一种元素也可以放在第ⅦA族,你认为该元素为_______ (填元素符号)。
(2)实验室制ca3的化学反应方程式为_______ 。
(3)g的氧化物与e的最高价氧化物对应水化物反应的离子方程式为_______ 。
(4)i在周期表中的位置为_______ ,带两个单位正电荷的i离子的电子排布式为_______ ,i对应的单质与h对应的单质反应的化学方程式为_______ 。
(5)e2d2的电子式为_______ ;a3d+离子的结构式为_______ 。
(6)写出工业冶炼元素g的单质的化学方程式_______ 。

(1)有人认为在元素周期表中,有一种元素也可以放在第ⅦA族,你认为该元素为
(2)实验室制ca3的化学反应方程式为
(3)g的氧化物与e的最高价氧化物对应水化物反应的离子方程式为
(4)i在周期表中的位置为
(5)e2d2的电子式为
(6)写出工业冶炼元素g的单质的化学方程式
您最近一年使用:0次
4 . 下图是元素周期表的一部分(号元素 ,用化学用语回答下列问题:
,用化学用语回答下列问题:

(1)D的基态电子排布式可简写为:___________ ;H代表的元素在周期表中的位置是___________ 。
(2)、G、J、K、M对应的简单离子的半径由大到小的顺序是___________ (用离子符号表示)
(3)在所列元素中,电负性最大的元素是___________ (填元素符号)。
(4)已知某原子的各级电离能如下:I1=577kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11578kJ/mol,则该原子在化合物中表现的化合价为___________
(5)元素周期表中位于斜对角线的两种元素及其性质十分相似,称之为对角线规则。根据元素周期表对角线规则,金属铍Be与铝单质及其化合物性质十分相似。Be(OH)2和Mg(OH)2可用试剂NaOH溶液鉴别。涉及的化学方程式为:___________ 。
 ,用化学用语回答下列问题:
,用化学用语回答下列问题:
(1)D的基态电子排布式可简写为:
(2)、G、J、K、M对应的简单离子的半径由大到小的顺序是
(3)在所列元素中,电负性最大的元素是
(4)已知某原子的各级电离能如下:I1=577kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11578kJ/mol,则该原子在化合物中表现的化合价为
(5)元素周期表中位于斜对角线的两种元素及其性质十分相似,称之为对角线规则。根据元素周期表对角线规则,金属铍Be与铝单质及其化合物性质十分相似。Be(OH)2和Mg(OH)2可用试剂NaOH溶液鉴别。涉及的化学方程式为:
您最近一年使用:0次
2020-12-15更新
|
1021次组卷
|
5卷引用:江苏省盐城第一中学2023-2024学年高二上学期第二次学情调研考试(期中)化学(选修)试卷
江苏省盐城第一中学2023-2024学年高二上学期第二次学情调研考试(期中)化学(选修)试卷辽宁省锦州市义县高级中学2020-2021学年高二12月月考化学试题(已下线)练习18 原子结构与元素的性质-2020-2021学年【补习教材·寒假作业】高二化学(人教版)(已下线)1.2 原子结构与元素的性质(C级检测练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)选择性必修第二册 期末学业水平检测
名校
5 . 下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)⑧的原子结构示意图为_________ 。
(2)②的气态氢化物分子的结构式为_____________ 。
(3)②、③的最高价含氧酸的酸性由强到弱的顺序是____________ 。(填化学式)
(4)⑤、⑥元素的金属性强弱依次___________ 。(填“增大”“减小”或“不变”)
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)⑧的原子结构示意图为
(2)②的气态氢化物分子的结构式为
(3)②、③的最高价含氧酸的酸性由强到弱的顺序是
(4)⑤、⑥元素的金属性强弱依次
您最近一年使用:0次
名校
解题方法
6 . 下表是元素周期表的一部分,按要求填空(填元素符号或化学式):
(1)在这些元素中,最活泼的非金属元素是________ ,最不活泼的元素是_______ 。
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是_________ (此空可填化学式或填物质名称),碱性最强的是________ 。
(3)写出⑥和⑨的单质反应产物的电子式________ ,其晶体属于__________ 晶体。
(4) 在周期表中的位置:
在周期表中的位置:_______ ,它的最简单气态氢化物的电子式_________ ;
(5)判断⑥与⑦的单质金属性强弱的实验依据是___________ ;
(6)②与③可形成A2B2型分子,该分子中各原子均达到最外层8电子稳定结构,则该分子的电子式为___________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在这些元素中,最活泼的非金属元素是
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是
(3)写出⑥和⑨的单质反应产物的电子式
(4)
 在周期表中的位置:
在周期表中的位置:(5)判断⑥与⑦的单质金属性强弱的实验依据是
(6)②与③可形成A2B2型分子,该分子中各原子均达到最外层8电子稳定结构,则该分子的电子式为
您最近一年使用:0次
7 . 如表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:(除特别注明外,其它一律用化学式表示)
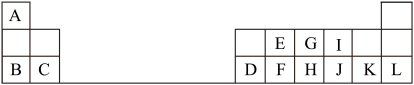
(1)在这些元素中,化学性质最不活泼的是:___ (填具体元素符号),其原子结构示意图为__ 。元素K名称为_____ ,在周期表中的位置是____ 。
(2)最高价氧化物水化物中碱性最强的化合物的电子式是:__ 。
(3)某元素二价阳离子的核外有10个电子,该元素是_____ (填元素名称)。
(4)G、H、I形成的气态氢化物稳定性由强到弱的顺序___ 。
(5)F、H、J的最高价氧化物对应水化物的酸性由强到弱的顺序__ 。
(6)I、J、K三种元素形成的离子,离子半径由大到小的顺序是__ 。
(7)元素I的氢化物是自然界中常见的物质,它的电子式为____ ;该氢化物常温下和元素K的单质反应的化学方程式为______ 。

(1)在这些元素中,化学性质最不活泼的是:
(2)最高价氧化物水化物中碱性最强的化合物的电子式是:
(3)某元素二价阳离子的核外有10个电子,该元素是
(4)G、H、I形成的气态氢化物稳定性由强到弱的顺序
(5)F、H、J的最高价氧化物对应水化物的酸性由强到弱的顺序
(6)I、J、K三种元素形成的离子,离子半径由大到小的顺序是
(7)元素I的氢化物是自然界中常见的物质,它的电子式为
您最近一年使用:0次
解题方法
8 . 下表为元素周期表的一部分, 回答下列问题。
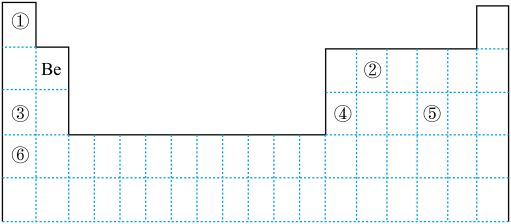
(1)我国科学家采用“铝铍测年法”测量“北京人”年龄。10Be 和9Be______________
a.是同一种核素 b.具有相同的中子数 c.互为同素异形体 d.互为同位素
(2)元素①和②可形成多种化合物。下列模型表示的分子中,不可能由①和②形成的是_______ (填序号)。
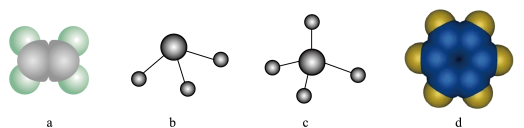
(3)元素①~⑥中,金属性最强的是___ (填元素符号)。②的单质和⑤的最高价氧化物对应水化物的浓溶液反应的化学方程式为______________ 。
(4)碘(53I) 是人体必需的微量元素之一。
①碘(53I) 在周期表中的位置是______
②CI-、Br-、I-的还原性由大到小的顺序为_______ 。
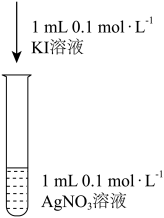
③资料显示: Ag+和I-会发生氧化还原反应生成两种单质,反应的离子方程式为_______ 。某同学用图实验验证上述反应,观察到两溶液混合后立即出现黄色浑浊,再加入淀粉溶液,不变蓝。分析产生上述现象的可能原因:________________

(1)我国科学家采用“铝铍测年法”测量“北京人”年龄。10Be 和9Be
a.是同一种核素 b.具有相同的中子数 c.互为同素异形体 d.互为同位素
(2)元素①和②可形成多种化合物。下列模型表示的分子中,不可能由①和②形成的是

(3)元素①~⑥中,金属性最强的是
(4)碘(53I) 是人体必需的微量元素之一。
①碘(53I) 在周期表中的位置是
②CI-、Br-、I-的还原性由大到小的顺序为
③资料显示: Ag+和I-会发生氧化还原反应生成两种单质,反应的离子方程式为

您最近一年使用:0次
9 . 叠氮化钠(NaN3)可用于汽车安全气囊的产气药。一种由氨基化钠(NaNH2)制备NaN3的工艺流程如下:
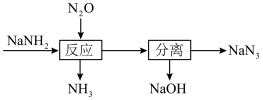
(1)生产NaNH2的化学方程式为2Na+ 2NH3(液)= 2NaNH2+ H2↑。
①钠元素位于周期表第___________ 周期___________ 族。
②NaNH2中氮元素的化合价为___________ .
(2) NaOH的电子式为___________ , 流程中“反应”的化学方程式为___________ 。
(3) NaN3晶体属于_____________ (填 “离子”、“分子”或“原子”)晶体,NaN3在撞击时能发生分解反应生成两种单质。计算理论上65gNaN3完全分解,释放出标准状况下的气体体积_________ (写出计算过程)。

(1)生产NaNH2的化学方程式为2Na+ 2NH3(液)= 2NaNH2+ H2↑。
①钠元素位于周期表第
②NaNH2中氮元素的化合价为
(2) NaOH的电子式为
(3) NaN3晶体属于
您最近一年使用:0次
10 . 短周期元素A、B、C在周期表中的位置关系如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数则:A、B、C的元素符号分别是___ 、___ 、___ 。


您最近一年使用:0次
2020-06-02更新
|
90次组卷
|
2卷引用:江苏省盐城市实验高级中学(新洋高级中学)2020-2021学年高一下学期期中考试化学试题



