解题方法
1 . 表中为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
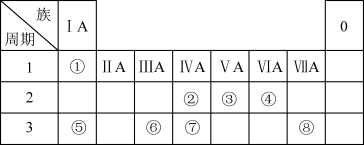
(1)地壳中含量居于第二位的元素在周期表中的位置是____ 。
(2)⑥的最高价氧化物的化学式为_____ ;⑧的最高价氧化物对应水化物的分子式为____ 。
(3)由①、④、⑤三种元素形成的既含离子键又含共价键的离子化合物,写出该化合物的电子式:_____ 。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是_____ (填字母)。
(5)已知Cs元素位于元素周期表中第六周期第IA族,请回答下列问题:
①预测铯单质的还原性比钠单质的还原性____ (填“弱”或“强”)。
②铯的原子序数为_____ 。
③铯单质与H2O反应的化学反应方程式为_____ 。
(6)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为____ 。

(1)地壳中含量居于第二位的元素在周期表中的位置是
(2)⑥的最高价氧化物的化学式为
(3)由①、④、⑤三种元素形成的既含离子键又含共价键的离子化合物,写出该化合物的电子式:
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是
| A.最高正化合价为+6 |
| B.气态氢化物比H2S稳定 |
| C.最高价氧化物对应水化物的酸性比硫酸弱 |
| D.单质的氧化性比S的弱 |
①预测铯单质的还原性比钠单质的还原性
②铯的原子序数为
③铯单质与H2O反应的化学反应方程式为
(6)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为
您最近半年使用:0次
解题方法
2 . W、X、Y、Z是原子序数依次增大的短周期主族元素,W与Z元素的原子序数之和等于X与Y元素的质子数之和,W是地壳中含量最多的元素,W与Z同主族,Y的氧化物具有两性。下列说法错误的是
A.原子半径: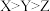 |
| B.W与X形成的化合物中都含离子键、共价键 |
| C.W与Z在自然界中均能以游离态存在 |
D.工业上电解熔融的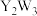 制备Y的单质 制备Y的单质 |
您最近半年使用:0次
名校
3 . 元素周期表有许多有趣的编排方式,有同学将短周期元素按照原子序数递增的顺序进行排列,得到如图所示的“蜗牛元素周期表”,图中每个圆圈代表一种元素,其中①代表氢元素。请回答下列问题:

(1)⑨在元素周期表中的位置为_______ 。
(2)④⑤⑦的离子半径由大到小的顺序为_______ 。
(3)③⑨⑩的最高价氧化物对应水化物的酸性由强到弱的顺序是_______ (填化学式)。
(4)用电子式表示由⑦和①组成的化合物的形成过程:_______ 。
(5)实验室制取④的简单氢化物的化学方程式为_______ 。
(6)可以验证⑦、⑧两元素金属性强弱的实验是_______(填字母)。

(1)⑨在元素周期表中的位置为
(2)④⑤⑦的离子半径由大到小的顺序为
(3)③⑨⑩的最高价氧化物对应水化物的酸性由强到弱的顺序是
(4)用电子式表示由⑦和①组成的化合物的形成过程:
(5)实验室制取④的简单氢化物的化学方程式为
(6)可以验证⑦、⑧两元素金属性强弱的实验是_______(填字母)。
| A.比较⑦、⑧两种元素的单质的硬度及熔点 |
| B.将除去氧化物薄膜的⑦、⑧的单质分别和热水作用,并滴入酚酞溶液 |
| C.将除去氧化物薄膜的⑦、⑧的单质分别和2mL1 mol∙L−1的盐酸反应 |
| D.比较⑦、⑧两种元素的最高价氧化物对应水化物的溶解性 |
您最近半年使用:0次
名校
解题方法
4 . X、Y、Z、W是原子序数依次增大的四种短周期元素,且Y、Z、W位于同周期,甲、乙、丁、戊、己是由这些元素组成的常见二元化合物,丙是一种气体单质,已知它们有如下转化关系(反应条件略):
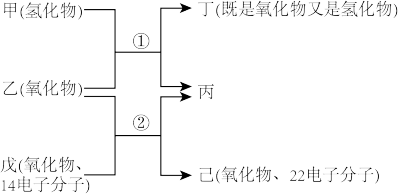
下列说法错误的是

下列说法错误的是
| A.元素Z与元素W至少可组成5种化合物 |
| B.乙可能是无色气体,也可能是有色气体 |
| C.上述四种元素可以组成离子化合物 |
| D.生成等物质的量的丙,反应①与反应②转移电子数相等 |
您最近半年使用:0次
2022-09-07更新
|
485次组卷
|
2卷引用:河南省焦作市第一中学2022-2023学年高三上学期定位考试化学试题
解题方法
5 . 短周期主族元素R、X、Y、Z、W的原子序数依次增大,X2R6、Y2R4和RZ-都是18电子微粒。ZXY-常用于检验Fe3+的存在。下列判断正确的是
| A.(XY)2分子的空间构型为直线形 |
| B.YR4W在水中能抑制水的电离 |
| C.元素的氧化物对应的水化物酸性:W>Z>X |
| D.(ZXY)2分子中σ键和π键数之比为4∶5 |
您最近半年使用:0次
解题方法
6 . D、E、X、Y、Z为原子序数依次增大的短周期主族元素,它们的简单氢化物分子的空间结构依次是正四面体形、三角锥形、正四面体形、V形、直线形。回答下列问题:
(1)Y的最高价氧化物的化学式为_______ 。
(2)上述五种元素中,能形成酸性最强的含氧酸的元素是_______ ,该元素的任意3种含氧酸的化学式为_______ 。
(3)D和Y形成的化合物,其分子的空间结构为_______ 。
(4)D和X形成的化合物,其化学键类型属于_______ (填“共价键”或“离子键”)。
(5)金属镁和E的单质在高温下反应得到的产物是_______ (写化学式)。该产物与水反应生成两种碱,反应的化学方程式是_______ 。
(1)Y的最高价氧化物的化学式为
(2)上述五种元素中,能形成酸性最强的含氧酸的元素是
(3)D和Y形成的化合物,其分子的空间结构为
(4)D和X形成的化合物,其化学键类型属于
(5)金属镁和E的单质在高温下反应得到的产物是
您最近半年使用:0次
7 . 2019年是化学元素周期表问世150周年,联合国宣布此年为“国际化学元素周期表年”。元素周期表在学习、研究中有很重要的作用,下表是元素周期表的一部分,用化学用语回答下列问题。
(1)e的元素符号是_______ ,d2b的电子式_______
(2)f、g的最高价氧化物对应的水化物中,酸性较强的物质的化学式是_______ 。
(3)c的金属性强于d的金属性,用原子结构解释原因:_______ ,失电子能力c大于d。
(4)下列对于a及其化合物的推断中,正确的是_______ (填序号)。
①a的最高正价和最低负价绝对值相等
②a的氢化物的稳定性强于f的氢化物的稳定性
③单质a比单质b难与氢气反应
(5)写出g单质与c的最高价氧化物对应水化物的化学方程式_______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | a | b | ||||||
| 3 | c | d | e | f | g |
(2)f、g的最高价氧化物对应的水化物中,酸性较强的物质的化学式是
(3)c的金属性强于d的金属性,用原子结构解释原因:
(4)下列对于a及其化合物的推断中,正确的是
①a的最高正价和最低负价绝对值相等
②a的氢化物的稳定性强于f的氢化物的稳定性
③单质a比单质b难与氢气反应
(5)写出g单质与c的最高价氧化物对应水化物的化学方程式
您最近半年使用:0次
8 . 短周期主族元素 X、Y、Z、W 的原子序数依次增大,Y 在短周期中原子半径最大,Z 是地壳中含量最高的金属元素,X 和 W 同主族,W 的最高正化合价与最低负化合价的代数和为6,下列说法正确的是
| A.原子半径由小到大的顺序:r(X)<r(Z)<r(W) |
| B.Y的最高价氧化物对应水化物的碱性大于Z的 |
| C.X的简单气态氢化物的稳定性小于W的 |
| D.W 与 Y形成的化合物属于共价化合物 |
您最近半年使用:0次
22-23高一上·全国·课时练习
9 . 已知元素W、X、Y、Z为原子序数依次增大的短周期主族元素,其中W的最高价氧化物的水化物能与其气态氢化物反应生成离子化合物,X原子的最外层电子数是次外层电子数的一半,Y与W同主族,Z元素的单质常温下为气体。
(1)W与X可以形成一种高温结构陶瓷材料甲,其中W、X的化合价分别是它们各自的最低价和最高价,其化学式为___________ 。
(2)X、Y、Z的气态氢化物的稳定性由强到弱的顺序是___________ (用分子式表示)。
(3)W、Z的气态氢化物分别为乙和丙,X与Z元素形成的化学物为丁。结构陶瓷材料甲的一种合成方法的反应如下:①丁+乙→丙+戊;②戊→甲+乙
其中,戊中含有三种元素,原子个数比为1︰4︰8,上述反应均在高温下进行。请写出反应的化学方程式:
①___________ 。
②___________ 。
(1)W与X可以形成一种高温结构陶瓷材料甲,其中W、X的化合价分别是它们各自的最低价和最高价,其化学式为
(2)X、Y、Z的气态氢化物的稳定性由强到弱的顺序是
(3)W、Z的气态氢化物分别为乙和丙,X与Z元素形成的化学物为丁。结构陶瓷材料甲的一种合成方法的反应如下:①丁+乙→丙+戊;②戊→甲+乙
其中,戊中含有三种元素,原子个数比为1︰4︰8,上述反应均在高温下进行。请写出反应的化学方程式:
①
②
您最近半年使用:0次
10 . 几种短周期元素的原子半径及主要化合价如表所示:
下列叙述正确的是
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 186 | 160 | 75 | 74 |
| 主要化合价 | +1 | +2 | +5、-3 | -2 |
| A.X、Y的最高价氧化物对应水化物的碱性:X<Y |
| B.简单离子半径:Z<W<X<Y |
| C.X与W形成的某种化合物可作呼吸面具的供氧剂 |
| D.Y与Z形成的化合物为共价化合物 |
您最近半年使用:0次



