名校
1 . 下列分子中,各原子均处于同一平面上的是( )
| A.NH3 | B.CCl4 | C.PCl3 | D.CH2O |
您最近一年使用:0次
2018-02-12更新
|
231次组卷
|
4卷引用:河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:2.2 第1课时
河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:2.2 第1课时(已下线)模块同步卷05 分子的立体构型及分子的性质-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)吉林省辽源市田家炳高级中学2020-2021学年高二下学期期中化学试题福建省厦门英才学校中学部22021-2022学年高二下学期4月月考化学试题
解题方法
2 . 已知:周期表中前四周期的六种元素A、B、C、D、E、F核电荷数依次增大,其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F2+离子核外各层电子均充满。请根据以上信息,回答下列问题:
(1)A、B、C、D的第一电离能由小到大的顺序为____ 。(用元素符号表示)
(2)B的氯化物的熔点比D的氯化物的熔点高,理由是____________________ 。
(3)E的最高价氧化物分子的空间构型是__________ ,是____ 分子(填“极性”“非极性”)。
(4)F原子的核外电子排布式是________________ 。
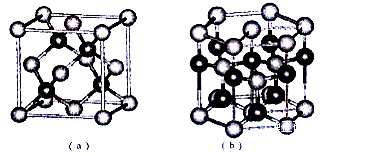
(5)E、F形成某种化合物有如图所示两种晶体结构(深色球表示F原子),其化学式为_________ 。(a)中E原子的配位数为____ 。若在(b)的结构中取出一个平行六面体作为晶胞,则平均一个晶胞中含有____ 个F原子。结构(a)与(b)中晶胞的原子空间利用率相比,(a)____ (b)(填“>”“<”或“=”)。
(1)A、B、C、D的第一电离能由小到大的顺序为
(2)B的氯化物的熔点比D的氯化物的熔点高,理由是
(3)E的最高价氧化物分子的空间构型是
(4)F原子的核外电子排布式是
(5)E、F形成某种化合物有如图所示两种晶体结构(深色球表示F原子),其化学式为

您最近一年使用:0次
2017-10-07更新
|
227次组卷
|
3卷引用:河北省五校联盟2018届高三上学期摸底考试理综化学试题
名校
3 . 下列说法正确的是
| A.VSEPR模型就是分子的空间构型 |
| B.在共价化合物分子中一定存在σ键 |
| C.Na3[AlF6]、Na2[SiF6]和[Cu(NH3)4]Cl2的配位数都是6 |
| D.共价键键长越短,键能一定越大 |
您最近一年使用:0次
2017-06-24更新
|
202次组卷
|
6卷引用:河北省蠡县中学2016-2017学年高二6月月考化学试题
名校
4 . 铁元素和碳元素形成的单质及化合物在生产、生活中有广泛的用途,
请回答下列问题:
(1)基态Fe原子的价层电子的电子排布图为_________________ ;其最外层电子的电子云形状为___________ 。
(2)(NH4)2Fe(SO4)2 • 6H2O俗称摩尔盐。其阴离子的VSEPR模型名称为____________________ 。
写出一种与NH4+互为等电子体的分子的电子式:________________________________ 。
(3)Fe(CO)5可用作催化剂、汽油抗暴剂等.其分子中σ键和π键的数目之比为______________ 。CO的沸点高于N2的原因是_________________________ 。
(4)碳元素可形成多种单质。
①石墨烯是从石墨中剥离出来的由单层碳原子构成的平面结构新型碳材料。其中碳原子的杂化方式为______________________ 。
料,其中碳原子的杂化方式为 ,
②金刚石的晶胞如图所示。若晶胞参数为a pm,阿伏伽德罗常数的值为NA,则该晶胞中原子的体积占晶胞体积的百分率为________________ ;1cm3晶体的平均质量为___________ (列出计算式即可)。
请回答下列问题:
(1)基态Fe原子的价层电子的电子排布图为
(2)(NH4)2Fe(SO4)2 • 6H2O俗称摩尔盐。其阴离子的VSEPR模型名称为
写出一种与NH4+互为等电子体的分子的电子式:
(3)Fe(CO)5可用作催化剂、汽油抗暴剂等.其分子中σ键和π键的数目之比为
(4)碳元素可形成多种单质。
①石墨烯是从石墨中剥离出来的由单层碳原子构成的平面结构新型碳材料。其中碳原子的杂化方式为
料,其中碳原子的杂化方式为 ,
②金刚石的晶胞如图所示。若晶胞参数为a pm,阿伏伽德罗常数的值为NA,则该晶胞中原子的体积占晶胞体积的百分率为
您最近一年使用:0次
16-17高二下·河北石家庄·阶段练习
解题方法
5 . 下列分子和离子中,中心原子价层电子对的几何构型为四面体型且分子或离子的立体构型为V形的是
| A.SO2 | B.H3O+ | C.BeCl2 | D.OF2 |
您最近一年使用:0次
名校
6 . 下列有关键角与分子空间构型的说法不正确的是
| A.键角为180°的分子,空间构型是直线形 |
| B.键角为120°的分子,空间构型是平面三角形 |
| C.键角为60°的分子,空间构型可能是正四面体形 |
| D.键角为90°~109°28'之间的分子,空间构型可能是V形 |
您最近一年使用:0次
2017-02-23更新
|
1082次组卷
|
4卷引用:2016-2017学年河北省衡水中学高二上学期五调考试化学试卷
2016-2017学年河北省衡水中学高二上学期五调考试化学试卷高二选择性必修2(人教版2019)第二章 分结构与性质 第二节 分子的空间结构 课时1 分子的空间结构 价层电子对互斥模型(已下线)第40练 分子的空间结构-2023年高考化学一轮复习小题多维练(全国通用)第二节 分子的空间结构 第1课时 分子结构的测定 多样的分子空间结构 价层电子对互斥模型
名校
7 . 氯的含氧酸根离子有ClO-、ClO2-、ClO3-、ClO4-等,下列说法中不正确的是
| A.ClO-中Cl显+1价 | B.ClO2-的空间构型为三角形 |
| C.ClO3-的空间构型为三角锥形 | D.ClO4-是SO42-的等电子体 |
您最近一年使用:0次
名校
解题方法
8 . 下列关于粒子结构的描述不 正确的是
| A.H2S和NH3均是价电子总数为8的极性分子 |
| B.HS-和HCl均是含一个极性键的18电子粒子 |
| C.CH2Cl2和CCl4均是四面体构型的非极性分子 |
| D.SO2和SO3杂化轨道类型均为sp2杂化,立体构型分别为V形、平面三角形 |
您最近一年使用:0次
2017-01-06更新
|
306次组卷
|
6卷引用:2016-2017学年河北省张家口一中高二12月月考化学卷
解题方法
9 . 【物质结构与性质】硼(B)、铝(Al)、镓(Ga)均属于硼族元素(第ⅢA族),它们的化合物或单质都有重要用途。回答下列问题:
(1)写出基态镓原子的电子排布式____________ 。
(2)已知:无水氯化铝在178℃升华,它的蒸气是缔合的双分于(Al2Cl6),结构如图
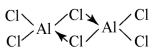
缔合双分子Al2Cl6中Al原子的轨道杂化类型是_______ 。
(3)B原子的电子有_____ 个不同的能级;晶体硼熔点为2300℃,则其为_____ 晶体。
(4)磷化硼(BP)是一种有价值的耐磨硬涂层材料,它是通过在高温氢气氛围下(>750℃)三溴化硼和三溴化磷反应制得。BP晶胞如图所示。
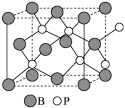
①画出三溴化硼和三溴化磷的空间结构式。
三溴化硼___________________ 三溴化磷____________________
②在BP晶胞中B的堆积方式为__________________ 。
③计算当晶胞晶格参数为a pm(即图中立方体的每条边长为 a pm)时,磷化硼中硼原子和磷原子之间的最近距离____________ 。
(1)写出基态镓原子的电子排布式
(2)已知:无水氯化铝在178℃升华,它的蒸气是缔合的双分于(Al2Cl6),结构如图

缔合双分子Al2Cl6中Al原子的轨道杂化类型是
(3)B原子的电子有
(4)磷化硼(BP)是一种有价值的耐磨硬涂层材料,它是通过在高温氢气氛围下(>750℃)三溴化硼和三溴化磷反应制得。BP晶胞如图所示。

①画出三溴化硼和三溴化磷的空间结构式。
三溴化硼
②在BP晶胞中B的堆积方式为
③计算当晶胞晶格参数为a pm(即图中立方体的每条边长为 a pm)时,磷化硼中硼原子和磷原子之间的最近距离
您最近一年使用:0次
2016-12-09更新
|
139次组卷
|
2卷引用:河北省保定市2017届高三第二次模拟考试理综化学试题
名校
10 . 根据价层电子对判断下列分子或者离子的空间构型是平面正三角形的是
| A.NH3 | B.CF4 | C.H2S | D.CO32- |
您最近一年使用:0次
2016-12-09更新
|
169次组卷
|
3卷引用:2015-2016学年河北省正定中学高二下第一次月考化学试卷



