名校
解题方法
1 . N、P、As都是VA族元素,且原子序数依次增大,它们的单质和化合物在生产、生活中有广泛应用。请回答下列相关问题。
(1)基态砷原子的价电子排布式为____ 。
(2)从结构分析硝酸符合形成氢键的条件但硝酸的沸点较低,其可能的原因是____ 。
(3) 与钴盐形成的配离子[Co(NO2)6]3-可用于检验K+的存在。
与钴盐形成的配离子[Co(NO2)6]3-可用于检验K+的存在。 离子的VSEPR模型名称为
离子的VSEPR模型名称为___ ,K3[Co(NO2)6]是黄色沉淀,该物质中四种元素的电负性由大到小的顺序是___ 。(用元素符号表示)
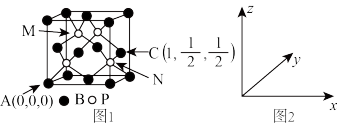
(4)磷化硼(BP)可作为金属表面的保护薄膜,其晶胞如图1所示,在BP晶胞中B原子配位数是___ ,P原子占据的是B原子堆积的____ (选填“立方体”“正四面体”或“正八面体”)空隙。建立如图2所示坐标系,可得晶胞中A、C处原子的分数坐标,则M处的P原子分数坐标为____ ,若晶胞中B原子和P原子之间的最近核间距为a pm,则晶胞边长为____ cm。
(1)基态砷原子的价电子排布式为
(2)从结构分析硝酸符合形成氢键的条件但硝酸的沸点较低,其可能的原因是
(3)
 与钴盐形成的配离子[Co(NO2)6]3-可用于检验K+的存在。
与钴盐形成的配离子[Co(NO2)6]3-可用于检验K+的存在。 离子的VSEPR模型名称为
离子的VSEPR模型名称为(4)磷化硼(BP)可作为金属表面的保护薄膜,其晶胞如图1所示,在BP晶胞中B原子配位数是

您最近一年使用:0次
2021-03-26更新
|
385次组卷
|
2卷引用:江西省抚州市临川第一中学2022届高三下学期4月模拟考试理科综合化学试题
解题方法
2 . S、Se 、N、Fe等元素及其化合物在科学研究和工业生产中具有重要的作用。
(1)臭鼬排放的臭气主要成分为3﹣MBT,键线式如图所示:

0.1mol 3﹣MBT中含有σ键数目为___________ (NA为阿伏加德罗常数的值)。3﹣MBT的沸点低于(CH3)2C=CHCH2OH,主要原因是___________ 。
(2)2020年12月17日,采撷月壤的嫦娥五号荣耀归来。嫦娥五号探测器采用太阳能电池板提供能量,在太阳能电池板材料中除单晶硅外,还有铜,铟,镓,硒等化学物质。硒为第四周期第VIA族元素,其氧化物有SeO2和SeO3两种,SeO3分子的立体构型为___________ ,与其互为等电子体的阴离子为 ___________ (举一例)。
(3)铁氰化钾,化学式为K3[Fe(CN)6],主要应用于制药、电镀、造纸、钢铁生产等工业,其煅烧分解生成KCN、FeC2、N2、(CN)2等物质。
①K3[Fe(CN)6]中所涉及的各元素的第一电离能由大到小的顺序为___________ 。
②(CN)2分子中存在碳碳键,C原子的杂化轨道类型为___________ 。
③下列选项是部分同学画的基态氮原子的核外电子排布图,其中违背泡利原理的是___________ (填序号,下同),违背洪特规则的是___________ 。
A.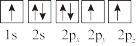 B.
B. 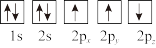 C.
C. 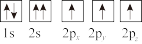
(4)如图是金属铁晶体中的一个晶胞。
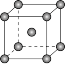
①该晶体中原子总体积占晶体体积的比值为___________ (用含π的最简代数式表示)。
②铁原子的半径为rpm,其晶体密度为___________ g•cm﹣3(用含有r、NA的最简代数式表示)。
(1)臭鼬排放的臭气主要成分为3﹣MBT,键线式如图所示:

0.1mol 3﹣MBT中含有σ键数目为
(2)2020年12月17日,采撷月壤的嫦娥五号荣耀归来。嫦娥五号探测器采用太阳能电池板提供能量,在太阳能电池板材料中除单晶硅外,还有铜,铟,镓,硒等化学物质。硒为第四周期第VIA族元素,其氧化物有SeO2和SeO3两种,SeO3分子的立体构型为
(3)铁氰化钾,化学式为K3[Fe(CN)6],主要应用于制药、电镀、造纸、钢铁生产等工业,其煅烧分解生成KCN、FeC2、N2、(CN)2等物质。
①K3[Fe(CN)6]中所涉及的各元素的第一电离能由大到小的顺序为
②(CN)2分子中存在碳碳键,C原子的杂化轨道类型为
③下列选项是部分同学画的基态氮原子的核外电子排布图,其中违背泡利原理的是
A.
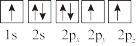 B.
B. 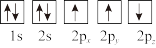 C.
C. 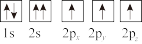
(4)如图是金属铁晶体中的一个晶胞。

①该晶体中原子总体积占晶体体积的比值为
②铁原子的半径为rpm,其晶体密度为
您最近一年使用:0次
名校
解题方法
3 . 美国化学家鲍林教授具有独特的化学想象力:只要给他物质的分子式,他就能大体上想象出这种物质的分子结构模型.多核离子所带电荷可以认为是中心原子得失电子所致,根据VSEPR模型,下列离子中所有原子都在同一平面上的一组是( )
A.NO 和NH 和NH | B.H3O+和ClO |
C.NO 和CO 和CO | D.PO 和SO 和SO |
您最近一年使用:0次
2020-06-17更新
|
492次组卷
|
16卷引用:江西省宜春市铜鼓中学2022-2023学年高二下学期第一次段考化学试题
江西省宜春市铜鼓中学2022-2023学年高二下学期第一次段考化学试题2016届山东省青岛市胶州一中高三上学期11月模拟化学试卷山西省沁县中学2018-2019学年高二下学期第一次月考化学试题宁夏回族自治区吴忠市吴忠中学2020年高二化学人教版选修3第二章《分子结构与性质》单元测试山西省孝义市2019-2020学年高二下学期3月阶段性考试化学试题新疆博尔塔拉蒙古自治州第五师高级中学2019-2020学年高二下学期期中考试化学试题河南省驻马店市正阳县高级中学2019-2020高二下学期第一次素质检测化学试题甘肃省静宁县第一中学2019-2020学年高二下学期期中考试(第二次月考)化学试题(实验班)新疆维吾尔自治区新源县第二中学2019-2020学年高二上学期第一次阶段测试化学试题广东省广州市真光中学2021-2022学年高二下学期3月月考化学试题吉林省白城市镇赉县第一中学校2021-2022学年高二下学期第一次月考化学试题(已下线)黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(1-10)湖南省长沙市长郡中学2022-2023学年高二上学期期末考试化学试题河南省淮滨高级中学2022-2023学年高二下学期期中教学质量检测化学试题广东省珠海市第一中学2022-2023学年高三下学期2月月考化学试题河南省信阳市第十高级中学2022-2023学年高二下学期期中教学质量检测化学试卷
名校
解题方法
4 . Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的巨大作用。
(1)N位于周期表中的位置为_____________ ,NF3的分子立体构型名称是____________ 。类比NH3·H2O表示出代表性分子NH4F含有的氢键________________________ 。
(2)写出N2O的等电子体__________________ (1个分子和1个离子)。
(3)Cu原子的基态外围电子排布式为____________ ;已知:CuO在高温下会分解成Cu2O,试从洪特规则角度解释其原因__________________________________________________ 。
(4) 在Cu的催化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中H—C=O的键角______ (填“大于”“等于”或“小于”)乙醇分子中的H—C—O的键角。
(5) 某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质。其水溶液中的N4H44+遇碱生成一种形似白磷的N4分子。画出N4H44+的结构式(标明其中的配位键)__________________ 。
(1)N位于周期表中的位置为
(2)写出N2O的等电子体
(3)Cu原子的基态外围电子排布式为
(4) 在Cu的催化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中H—C=O的键角
(5) 某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质。其水溶液中的N4H44+遇碱生成一种形似白磷的N4分子。画出N4H44+的结构式(标明其中的配位键)
您最近一年使用:0次
名校
解题方法
5 . 过渡金属在生产生活中的应用十分广泛。
Ⅰ.Cr元素形成的氯化铬酰(CrO2Cl2)有重要用途,在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
(1)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,由以上实验事实可以判断CrO2Cl2分子是_____________ (填“极性”或“非极性”)分子,该分子的立体构型的名称为___________ 。
Ⅱ.Cu可形成多种配合物,根据下列信息回答问题:
(2)向盛有硫酸铜水溶液的试管里逐滴加入氨水,首先出现蓝色沉淀,继续滴加氨水,蓝色沉淀溶解,得到深蓝色的透明溶液,先后发生的离子方程式为Cu2++2NH3.H2O=Cu(OH)2↓+2NH4+,_______________ 。
(3)再向深蓝色透明溶液加入乙醇,析出深蓝色的晶体。深蓝色晶体的化学式为__________________________ ;析出晶体的原因是_______________________________________________________ 。若将Cu单质的粉末加入NH3的浓溶液中,通入O2,充分反应后溶液呈深蓝色,该反应的离子方程式是____________________ 。
(4)根据以上实验过程,判断NH3和H2O与Cu2+的配位能力:NH3____ H2O(填“大于”、“等于”或“小于”)。
Ⅲ.Ni(CO)6为正八面体结构,其中的镍原子位于正八面体的中心,配位体CO分子则在正八面体的六个顶点上。
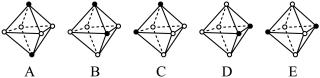
(5)若把其中两个CO配位体换成 NH3 得到新的配合物,则以下物质中互为同分异构体的是_________ 。(填字母编号,任填一组。图中黑点为NH3,圆圈为CO,Ni略去)
Ⅰ.Cr元素形成的氯化铬酰(CrO2Cl2)有重要用途,在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
(1)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,由以上实验事实可以判断CrO2Cl2分子是
Ⅱ.Cu可形成多种配合物,根据下列信息回答问题:
(2)向盛有硫酸铜水溶液的试管里逐滴加入氨水,首先出现蓝色沉淀,继续滴加氨水,蓝色沉淀溶解,得到深蓝色的透明溶液,先后发生的离子方程式为Cu2++2NH3.H2O=Cu(OH)2↓+2NH4+,
(3)再向深蓝色透明溶液加入乙醇,析出深蓝色的晶体。深蓝色晶体的化学式为
(4)根据以上实验过程,判断NH3和H2O与Cu2+的配位能力:NH3
Ⅲ.Ni(CO)6为正八面体结构,其中的镍原子位于正八面体的中心,配位体CO分子则在正八面体的六个顶点上。

(5)若把其中两个CO配位体换成 NH3 得到新的配合物,则以下物质中互为同分异构体的是
您最近一年使用:0次
解题方法
6 . 催化剂在现代化学工业中占有极其重要的地位,主要涉及过渡元素及其化合物、硅、铝化合物等。中国科学家创造性地构建了硅化物晶格限域的单铁中心催化剂,成功地实现了甲烷在无氧条件下选择活化,一步高效生产乙烯、芳烃和氢气等化学品。
(1)硅、碳位于同一主族,用“>”“<”或“=”填空:
(2)CN-能与Fe3+形成配合物,与CN-互为等电子体的分子有_____________ (任写一种);1mol[Fe(CN)6]3-中含____________ mol σ键。
(3)已知:反应2CH4 CH2=CH2+2H2,碳原子的杂化类型转化过程为
CH2=CH2+2H2,碳原子的杂化类型转化过程为___________ ;
(4)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过___________ 方法区分晶体、准晶体和非晶体。
(5)基态F原子的价层电子排布图为___________ 。
(6)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为____________ 。
(7)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g·cm-3。
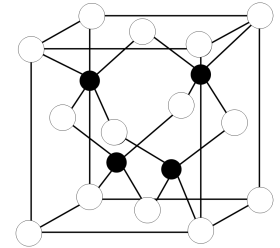
①CuF的熔点比CuCl的高,原因是____________________________________________ 。
②已知NA为阿伏加 德罗常数的值,CuF的晶胞结构如图所示,则CuF的晶胞参数a=__________ nm(列出计算式)。
(1)硅、碳位于同一主族,用“>”“<”或“=”填空:
| 性质 | 原子半径 | 第一电离能 | 熔点 | 键能 |
| 项目 | ①Si | ②C | ③CO2 | ④H-Si |
(2)CN-能与Fe3+形成配合物,与CN-互为等电子体的分子有
(3)已知:反应2CH4
 CH2=CH2+2H2,碳原子的杂化类型转化过程为
CH2=CH2+2H2,碳原子的杂化类型转化过程为(4)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(5)基态F原子的价层电子排布图为
(6)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为
(7)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g·cm-3。

①CuF的熔点比CuCl的高,原因是
②已知NA为阿伏加 德罗常数的值,CuF的晶胞结构如图所示,则CuF的晶胞参数a=
您最近一年使用:0次
名校
7 . 关于CO2和CO32-的下列说法正确的是
| A.两种微粒的中心原子均无孤电子对 | B.两种微粒价层电子对数相同 |
| C.键角:CO32-> CO2 | D.两种微粒的中心原子杂化方式相同 |
您最近一年使用:0次
2020-05-17更新
|
84次组卷
|
2卷引用:江西省抚州市资溪县第一中学2022-2023学年高二下学期5月期中考试化学试题
名校
8 . 下列分子中的中心原子杂化轨道的类型相同的是( )
| A.CO2与NO2 | B.AlCl3与C2H2 |
| C.H2O与BF3 | D.CH4与NH3 |
您最近一年使用:0次
2020-04-22更新
|
101次组卷
|
3卷引用:江西省都昌县第三中学2019-2020学年高二下学期4月考试化学试题
9 . 2019年的化学诺贝尔奖颁给了为锂电池研究作出贡献的三位科学家。有两种常见锂电池:一种是采用镍钴锰酸锂Li(NiCoMn)O2或镍钴铝酸锂为正极的“三元材料锂电池”;另一种是采用磷酸铁锂为正极的磷酸铁锂电池。请回答下列问题:
(1)基态钴原子的价电子排布式为____ ,Mn位于元素周期表的____ 区(填“s”或“p”或“d”或“ds”或“f”)。
(2)磷元素可以形成多种含氧酸H3PO4、H3PO2、H3PO3、HPO3,这四种酸中酸性最强的是___ 。PO43-的空间构型是 ___ ,中心原子的杂化方式是 ____ 。
(3)CoO、MnO两种氧化物的熔点由高到低的顺序是___ ,原因是 ___ 。
(4)PH3是____ 分子(填“极性”或“非极性”),其在水中的溶解性比NH3小,原因是 _____
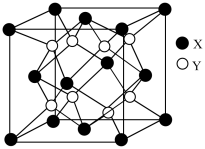
(5)硫化锂Li2S(摩尔质量Mg∙mol-1)的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如图。若硫化锂晶体的密度为ag.cm-3,则距离最近的两个S2-的距离是___ nm。(用含a、M、NA的计算式表示)
(1)基态钴原子的价电子排布式为
(2)磷元素可以形成多种含氧酸H3PO4、H3PO2、H3PO3、HPO3,这四种酸中酸性最强的是
(3)CoO、MnO两种氧化物的熔点由高到低的顺序是
(4)PH3是
(5)硫化锂Li2S(摩尔质量Mg∙mol-1)的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如图。若硫化锂晶体的密度为ag.cm-3,则距离最近的两个S2-的距离是

您最近一年使用:0次
2020-04-04更新
|
1920次组卷
|
5卷引用:江西省井冈山中学2020届高三四月检测理综化学试题
名校
解题方法
10 . 铂钴合金是以铂为基含钴二元合金,在高温下,铂与钴可无限互溶,其固体为面心立方晶格。铂钴合金磁性极强,磁稳定性较高,耐化学腐蚀性很好,主要用于航天航空仪表、电子钟表、磁控管等。氟及其化合物用途非常广泛。回答下列问题:
(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过____ 方法区分晶体准晶体和非晶体。
(2)基态F原子的价层电子排布图(轨道表达式)为______ 。
(3)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为______ ,与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是______ (各举一例)。
(4)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。NH4+中中心原子的杂化类型是______ ;氟化铵中存在______ (填字母)。
A.离子键 B.σ键 C.π键 D.氢键
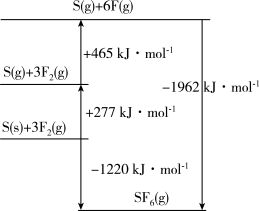
(5)SF6被广泛用作高压电气设备的绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则F-F键的键能为______ kJ•mol-1,S-F键的键能为______ kJ•mol-1。
(6)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g•cm-3。
①CuF的熔点比CuCl的高,原因是______
②已知NA为阿伏加 德罗常数的值,CuF的晶胞结构如图(b)所示,则CuF的晶胞参数a=______ nm(列出计算式)。

(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)基态F原子的价层电子排布图(轨道表达式)为
(3)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为
(4)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。NH4+中中心原子的杂化类型是
A.离子键 B.σ键 C.π键 D.氢键
(5)SF6被广泛用作高压电气设备的绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则F-F键的键能为

(6)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g•cm-3。
①CuF的熔点比CuCl的高,原因是
②已知NA为阿伏加 德罗常数的值,CuF的晶胞结构如图(b)所示,则CuF的晶胞参数a=

您最近一年使用:0次
2019-11-13更新
|
271次组卷
|
4卷引用:江西省南昌市新建区第二中学2020届高三下学期第四次线上测试(全国I卷)理综化学试题



