30. 二甲醚是一种重要的化工原料,利用水煤气(CO、H
2)合成二甲醚是工业上的常用方法,该方法由以下几步组成:
2H
2(g)+CO(g)
⇌CH
3OH(g)△H=﹣90.0kJ•mol
﹣1①
2CH
3OH(g)
⇌CH
3OCH
3(g)+H
2O(g)△H=﹣24.5kJ•mol
﹣1②
CO(g)+H
2O(g)
⇌CO
2(g)+H
2(g)△H=﹣41.1kJ•mol
﹣1③
(1)反应①的
△S
________________0(填“>”、“<”或“=”).在
________________(填“较高”或“较低”)温度下该反应自发进行.
(2)在250℃的恒容密闭容器中,下列事实可以作为反应③已达平衡的是
________________(填选项字母).
A.容器内气体密度保持不变B.CO与CO
2的物质的量之比保持不变
C.H
2O与CO
2的生成速率之比为1:1D.该反应的平衡常数保持不变
(3)当合成气中CO与H
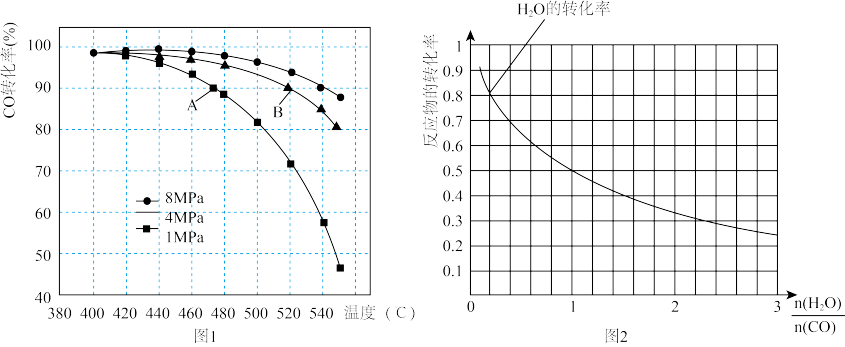
2的物质的量之比恒定时,温度、压强对CO转化率的影响如图1所示.图1中A点的v(逆)
________________B点的v(正)(填“>”、“<”或“=”),说明理由
________________.实际工业生产中该合成反应的条件为500℃、4MPa请回答采用500℃的可能原因
________________
(4)一定温度下,密闭容器中发生反应③,水蒸气的转化率与
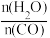
的关系如图2:计算该温度下反应③的平衡常数K=
________________.在图2中作出一氧化碳的转化率与
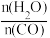
的曲线
____________。