1 . 10℃时加热NaHCO3饱和溶液,测得该溶液的pH随温度的升高发生如下变化:
甲同学认为,该溶液pH升高的原因是随温度的升高HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为____________________ 。
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度________ (填“大于”或“小于”)NaHCO3,该分解反应的化学方程式为_______________ 。
丙同学认为甲、乙的判断都不充分。丙认为:
(1)只要在加热煮沸的溶液中加入足量的BaCl2溶液,若产生沉淀,则乙判断正确。为什么?能不能选用Ba(OH)2溶液?_____________________________________________ 。
(2)将加热后的溶液冷却到10 ℃,若溶液的pH______ (填“高于”、“低于”或“等于”)8.3,则__________ (填“甲”或“乙”)判断正确。
温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
pH | 8.3 | 8.4 | 8.5 | 8.8 |
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度
丙同学认为甲、乙的判断都不充分。丙认为:
(1)只要在加热煮沸的溶液中加入足量的BaCl2溶液,若产生沉淀,则乙判断正确。为什么?能不能选用Ba(OH)2溶液?
(2)将加热后的溶液冷却到10 ℃,若溶液的pH
您最近一年使用:0次
2020-02-17更新
|
180次组卷
|
4卷引用:贵州省雷山县第四中学2019-2020学年高二上学期期末考试化学试题
名校
解题方法
2 . 明矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,含有少量氧化铁,利用明矾石制备K2SO4的工艺流程如图所示:

据此流程图回答下列问题:
(1)①焙烧炉中Al2(SO4)3与S反应的产物是两种氧化物,该反应的化学方程式为______ ;写出炉气的一种用途________ 。
(2)②中Al2O3参与反应的离子方程式为__________ 。
(3)③中调节pH不能用CO2的理由是____________________ 。
(4)工业冶炼金属铝需要定期更换补充阳极碳块的原因是__________________ 。
(5)纯净氢氧化铝经历两次__________________ (填反应类型)可制得铝。以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池负极的电极反应式是__________________ 。
(6)现有明矾石1 625 t,按上述流程制得780 t Al(OH)3,忽略铝元素的损失,请计算明矾石中钾元素的质量分数为____________ %。

据此流程图回答下列问题:
(1)①焙烧炉中Al2(SO4)3与S反应的产物是两种氧化物,该反应的化学方程式为
(2)②中Al2O3参与反应的离子方程式为
(3)③中调节pH不能用CO2的理由是
(4)工业冶炼金属铝需要定期更换补充阳极碳块的原因是
(5)纯净氢氧化铝经历两次
(6)现有明矾石1 625 t,按上述流程制得780 t Al(OH)3,忽略铝元素的损失,请计算明矾石中钾元素的质量分数为
您最近一年使用:0次
2020-01-14更新
|
315次组卷
|
9卷引用:贵州省剑河县第二中学2019-2020学年高二上学期期末考试化学试题
贵州省剑河县第二中学2019-2020学年高二上学期期末考试化学试题云南省西双版纳傣族自治州勐腊县第一中学2019-2020学年高二上学期期末考试化学试题贵州省雷山县第四中学2019-2020学年高一上学期期末考试化学试题人教版高中化学必修1第三章《金属及其化合物》测试卷1云南省昭通市彝良县一中2019—2020学年高一上学期期末考试化学试题云南省镇雄县民族中学2019-2020学年高一上学期期末考试化学试题云南省曲靖市马龙区第二中学2019-2020学年 高一上学期期末考试化学试题云南省玉溪市三中2021-2022学年高一下学期3月份入学考试 化学试题云南省玉溪市通海县第三中学2020-2021学年高一上学期期中考试化学试题
3 . 某化学兴趣小组利用如图1实验装置进行制取氯酸钾和验证元素的非金属性相对强弱的实验。已知氯气在加热条件下与氢氧化钾反应生成氯酸钾、水和氯化钾。
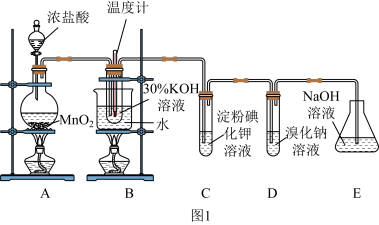
(1)A装置中反应的离子方程式为_______ ,B装置中反应的离子方程式为_______ ,B装置采用水浴加热的优点是_______ 。
(2)若对调B和C装置的位置,_____ (填“能”或“不能”)提高B中氯酸钾的产率。
(3)验证非金属性:Cl>I的实验现象是_______ ,该装置______ (填“能”或“不能”)验证非金属性:Cl>Br>I。
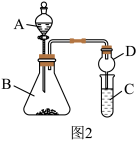
(4)利用如图2装置验证非金属性:C>Si,B中加Na2CO3,C中加Na2SiO3溶液,A中应该加入_____ ,C中反应的化学方程式:_____ ,D装置的作用是______ 。

(1)A装置中反应的离子方程式为
(2)若对调B和C装置的位置,
(3)验证非金属性:Cl>I的实验现象是
(4)利用如图2装置验证非金属性:C>Si,B中加Na2CO3,C中加Na2SiO3溶液,A中应该加入

您最近一年使用:0次
4 . 利用下图装置(夹持装置略)制取和收集纯净、干燥的氨气,并探究氨气的性质。

(1)关闭装置Ⅰ中的止水夹,向分液漏斗中加适量水,打开活塞,说明Ⅰ气密性良好的现象是______________________ 。
(2)利用装置Ⅰ制取氨气,不能选用的试剂为浓氨水和________ (填字母)。
A.氢氧化钠 B.碱石灰 C.硝酸钾 D.生石灰
(3)根据实验要求,仪器连接的顺序(用字母编号表示):a接________、________接________、______接______。______
(4)收集氨气,按如图装置进行NH3性质的探究实验。

①打开旋塞1,B瓶中的现象是_________________________________________ ,原因是_____________________________________________ ,稳定后,关闭旋塞1;
②再打开旋塞2,B瓶中的现象是__________________________________________ 。

(1)关闭装置Ⅰ中的止水夹,向分液漏斗中加适量水,打开活塞,说明Ⅰ气密性良好的现象是
(2)利用装置Ⅰ制取氨气,不能选用的试剂为浓氨水和
A.氢氧化钠 B.碱石灰 C.硝酸钾 D.生石灰
(3)根据实验要求,仪器连接的顺序(用字母编号表示):a接________、________接________、______接______。
(4)收集氨气,按如图装置进行NH3性质的探究实验。

①打开旋塞1,B瓶中的现象是
②再打开旋塞2,B瓶中的现象是
您最近一年使用:0次
2019-09-26更新
|
195次组卷
|
3卷引用:贵州省余庆中学2019-2020学年高二上学期开学考试化学试题
名校
解题方法
5 . 已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
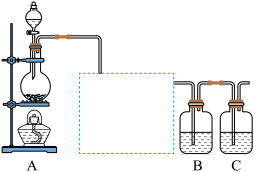
(1)装置A的分液漏斗中盛装的试剂是______ ,烧瓶中发生的反应的化学方程式是________ 。
(2)画出虚线框内的实验装置图,所加试剂为____________ ,该装置的作用是_______ 。
(3)装置B中盛放的试剂是____________ (填序号),实验现象为____________ ,该反应的离子方程式是_____________ ,该反应属于四种基本反应类型中的__________ 反应。
A Na2S溶液 B Na2SO3溶液 C Na2SO4溶液
(4)已知:①硫酸比次氯酸稳定;②高氯酸的酸性比硫酸强;③S2-比Cl-易被氧化;④HCl比H2S稳定;⑤铜与盐酸不反应,但能与浓硫酸反应;⑥铁与氯气在加热条件下反应生成三氯化铁,铁与硫在加热条件下反应生成硫化亚铁;⑦硫原子与氯原子的电子层数相同,氯的原子半径小于硫原子。能说明氯的非金属性比硫强的是________ (填序号)。
A 全部 B ②③④⑥⑦ C ①②④⑤⑥ D ②③④⑤⑥⑦
(5)装置C中盛放烧碱溶液,目地是吸收反应后剩余的气体,防止污染空气,写出该装置中所发生反应的离子方程式:_____________ 。

(1)装置A的分液漏斗中盛装的试剂是
(2)画出虚线框内的实验装置图,所加试剂为
(3)装置B中盛放的试剂是
A Na2S溶液 B Na2SO3溶液 C Na2SO4溶液
(4)已知:①硫酸比次氯酸稳定;②高氯酸的酸性比硫酸强;③S2-比Cl-易被氧化;④HCl比H2S稳定;⑤铜与盐酸不反应,但能与浓硫酸反应;⑥铁与氯气在加热条件下反应生成三氯化铁,铁与硫在加热条件下反应生成硫化亚铁;⑦硫原子与氯原子的电子层数相同,氯的原子半径小于硫原子。能说明氯的非金属性比硫强的是
A 全部 B ②③④⑥⑦ C ①②④⑤⑥ D ②③④⑤⑥⑦
(5)装置C中盛放烧碱溶液,目地是吸收反应后剩余的气体,防止污染空气,写出该装置中所发生反应的离子方程式:
您最近一年使用:0次
2019-07-03更新
|
822次组卷
|
8卷引用:贵州省从江县第一民族中学2018-2019学年高二上学期期末考试化学试题
解题方法
6 . 已知由短周期元素构成的三种粒子:甲a(单核带一个单位正电荷)、乙I(四核不带电荷)、丙e(双核带一个单位负电荷),它们都有10个电子。物质A由甲、丙构成,B、C、D、K都是单质,反应①~⑤都是用于工业生产的反应,各有关物质之间的相互反应转化关系如下图所示:

请填写下列空白:
(1)写出下列物质的化学式:B________ ,I________ ,J________ 。
(2)A的化学式是__________________ 。
(3)写出下列反应的离子方程式:
①H+E(溶液)→M_________________________________________________________ 。
②I溶于G_______________________________________________________ 。
(4)写出反应④的化学方程式____________________________________________ 。

请填写下列空白:
(1)写出下列物质的化学式:B
(2)A的化学式是
(3)写出下列反应的离子方程式:
①H+E(溶液)→M
②I溶于G
(4)写出反应④的化学方程式
您最近一年使用:0次
解题方法
7 . 下图表示在没有通风橱时制取纯净的氯气时设计的装置图,图中A、B是可控制的弹簧铁夹。
(1)烧杯中盛放的液体是__________ ,其作用是_________ ,水槽中盛放的液体是_________ 。
(2)简述操作过程:(从氯气已经产生开始)在收集氯气之前,应__________________________ ;当氯气纯度合乎要求时,应__________________________________ ,当氯气收集完毕时,应______ 。
(3)将8.7 g二氧化锰与含氯化氢14.6 g的浓盐酸共热制氯气,甲同学认为可制得氯气 7.1 g,乙同学认为制得氯气的质量小于7.1 g,你认为________ (填“甲”或“乙”)同学正确,原因是_________ 。
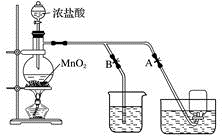
(1)烧杯中盛放的液体是
(2)简述操作过程:(从氯气已经产生开始)在收集氯气之前,应
(3)将8.7 g二氧化锰与含氯化氢14.6 g的浓盐酸共热制氯气,甲同学认为可制得氯气 7.1 g,乙同学认为制得氯气的质量小于7.1 g,你认为
您最近一年使用:0次
2019-01-12更新
|
127次组卷
|
3卷引用:贵州省剑河县二中2018-2019学年高二上学期期末考试化学试题
贵州省剑河县二中2018-2019学年高二上学期期末考试化学试题贵州省剑河县第二中学2018-2019学年高一上学期12月份考试化学试题(已下线)3.1.1 氯气的发现与制备 练习(1)——《高中新教材同步备课》(苏教版 必修第一册)
解题方法
8 . 现有原子序数之和为51的5种短周期元素A,B,C,D,E。已知A的单质在常温下为无色气体;B原子的最外层电子数比次外层电子数多3个;C和B属于同一主族;D的最高正价与负价的代数和为4,其最高价氧化物对应的水化物的酸性在同主族元素中最强,E元素最外层电子数与其K层电子数相同。
(1)试写出它们的元素符号。__________________________________________ 。
(2)写出B的氢化物的电子式_____________________________ 。
(3)由A、D两种元素形成的化合物是________ 化合物(填“离子”或“共价”),化合物内存在________ 键(填“离子”或“共价”)。
(4)由D、E两种元素形成的化合物的电子式为________ ,它属于________ 化合物,化合物内存在________ 键。
(5)下列关于A,B,C,D,E 5种元素形成的物质的有关叙述正确的是________ (多选)。
a.A,B,C,D都能通过共价键形成单质,其中B形成的单质性质最稳定,是因为其原子半径最小
b.A,B,D 3种元素为非金属元素,它们共同组成的化合物一定是共价化合物
c.B,E形成的化合物E3B2应为离子化合物
d.5种元素两两组合形成的化合物中既有共价化合物,又有离子化合物
e.5种元素形成简单离子的离子半径大小为C>D>B>E>A
(1)试写出它们的元素符号。
(2)写出B的氢化物的电子式
(3)由A、D两种元素形成的化合物是
(4)由D、E两种元素形成的化合物的电子式为
(5)下列关于A,B,C,D,E 5种元素形成的物质的有关叙述正确的是
a.A,B,C,D都能通过共价键形成单质,其中B形成的单质性质最稳定,是因为其原子半径最小
b.A,B,D 3种元素为非金属元素,它们共同组成的化合物一定是共价化合物
c.B,E形成的化合物E3B2应为离子化合物
d.5种元素两两组合形成的化合物中既有共价化合物,又有离子化合物
e.5种元素形成简单离子的离子半径大小为C>D>B>E>A
您最近一年使用:0次
名校
9 . 元素A、B、C都是短周期元素,它们的原子序数大小为A<B<C。A元素原子的最外层电子数为次外层电子数的2倍;B元素原子的次外层电子数是最外层电子数的2倍。B与C可形成共价化合物BC4。请回答下列问题:
(1)这三种元素所对应的气态氢化物中最不稳定的是__________ (填化学式),该氢化物在空气中燃烧的化学方程式为__________________________________________________________ 。
(2)它们的最高价氧化物对应的水化物中酸性最强的是__________ ,最弱的是__________ (填酸的化学式)。
(3)BC4的化学式是__________ 。BC4不稳定,遇水易形成B的含氧酸及C的氢化物。近代海战中为了掩蔽军事目标,通常采用喷BC4和液氨的方法以形成烟幕,有关化学反应用方程式表示为________ 。
(1)这三种元素所对应的气态氢化物中最不稳定的是
(2)它们的最高价氧化物对应的水化物中酸性最强的是
(3)BC4的化学式是
您最近一年使用:0次
2018-12-22更新
|
128次组卷
|
4卷引用:贵州省织金县一中2018-2019学年高二上学期12月份考试化学试题
10 . 今有A,B两种元素,A的+1价阳离子与B的-2价阴离子的电子层结构与氖相同。
(1)用电子式表示A与B两种元素构成的两种化合物分别为__________________ 和__________________ ,前者只有__________ 键;后者既有________ 键,又有________ 键。
(2)A的氢化物的电子式为_______ ,其中含有________ 键,它与水反应的化学方程式为____________ 。
(3)元素B的气态氢化物的电子式为___________________________________________ ,该分子中的键属于________ (填“极性”或“非极性”)键,该氢化物与H+形成的键属于________ 。
(4)元素A的最高价氧化物的水化物的电子式为____________ ,其中既有________ 键,又有________ 键。
(5)B元素的单质有__________ 和__________ ,二者互称为______________________ 。
(1)用电子式表示A与B两种元素构成的两种化合物分别为
(2)A的氢化物的电子式为
(3)元素B的气态氢化物的电子式为
(4)元素A的最高价氧化物的水化物的电子式为
(5)B元素的单质有
您最近一年使用:0次
2018-12-19更新
|
175次组卷
|
2卷引用:贵州省遵义市正安县第一中学2018-2019学年高二上学期期中考试化学试题



