解题方法
1 . 磺酰氯( )是一种重要的有机合成试剂,也是锂电池正极活性物质。实验室可利用
)是一种重要的有机合成试剂,也是锂电池正极活性物质。实验室可利用 与
与 在活性炭作用下制取少量的
在活性炭作用下制取少量的 ,装置如图所示(有些夹持装置省略)。
,装置如图所示(有些夹持装置省略)。 的熔点为-54.1℃,沸点为69.1℃,常温较稳定。100℃以上易分解。
的熔点为-54.1℃,沸点为69.1℃,常温较稳定。100℃以上易分解。
②
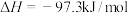
③ 遇水发生剧烈反应,并产生大量白雾。
遇水发生剧烈反应,并产生大量白雾。
回答下列问题:
(1)装置丙中发生反应的化学方程式为___________ 。
(2)仪器A的名称为___________ ,装置乙中盛放的试剂为___________ ,仪器F中盛放的试剂为___________ ,装置丁中应采取的控制温度的方式为___________ 。
(3)上述仪器的正确连接顺序是___________ 。(填仪器接口字母编号,仪器可重复使用)e→___________→g,h←___________←f
(4)某实验小组利用该装置消耗了标准状况下氯气1120mL( 足量),最后得到纯净的磺酰氯4.0g,则磺酰氯的产率为
足量),最后得到纯净的磺酰氯4.0g,则磺酰氯的产率为___________ (保留3位有效数字)。
(5)某公司开发的Li― 电池,其示意图如图。
电池,其示意图如图。 。则电池工作时,正极的电极反应式为
。则电池工作时,正极的电极反应式为___________ 。
 )是一种重要的有机合成试剂,也是锂电池正极活性物质。实验室可利用
)是一种重要的有机合成试剂,也是锂电池正极活性物质。实验室可利用 与
与 在活性炭作用下制取少量的
在活性炭作用下制取少量的 ,装置如图所示(有些夹持装置省略)。
,装置如图所示(有些夹持装置省略)。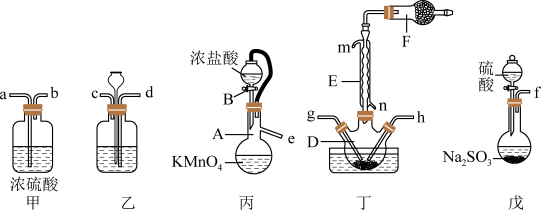
 的熔点为-54.1℃,沸点为69.1℃,常温较稳定。100℃以上易分解。
的熔点为-54.1℃,沸点为69.1℃,常温较稳定。100℃以上易分解。②

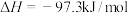
③
 遇水发生剧烈反应,并产生大量白雾。
遇水发生剧烈反应,并产生大量白雾。回答下列问题:
(1)装置丙中发生反应的化学方程式为
(2)仪器A的名称为
(3)上述仪器的正确连接顺序是
(4)某实验小组利用该装置消耗了标准状况下氯气1120mL(
 足量),最后得到纯净的磺酰氯4.0g,则磺酰氯的产率为
足量),最后得到纯净的磺酰氯4.0g,则磺酰氯的产率为(5)某公司开发的Li―
 电池,其示意图如图。
电池,其示意图如图。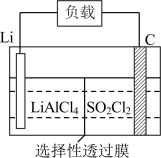
 。则电池工作时,正极的电极反应式为
。则电池工作时,正极的电极反应式为
您最近一年使用:0次
解题方法
2 . 为早日实现“碳中和碳达峰”目标,科学家提出用钌(Ru)基催化剂催化 和
和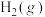 反应生成HCOOH.反应机理如图所示,已知当生成46g液态HCOOH时放出31.2kJ的热量。下列说法正确的是
反应生成HCOOH.反应机理如图所示,已知当生成46g液态HCOOH时放出31.2kJ的热量。下列说法正确的是
 和
和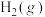 反应生成HCOOH.反应机理如图所示,已知当生成46g液态HCOOH时放出31.2kJ的热量。下列说法正确的是
反应生成HCOOH.反应机理如图所示,已知当生成46g液态HCOOH时放出31.2kJ的热量。下列说法正确的是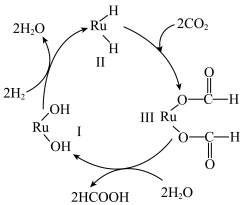
| A.反应历程中存在极性键、非极性键的断裂与形成 |
| B.物质Ⅰ为该反应的催化剂,物质Ⅱ、Ⅲ为中间产物 |
| C.催化剂能降低活化能,加快反应速率,改变反应热,从而提高转化率 |
D.通过 和 和 反应制备液态HCOOH,每转移1mol 反应制备液态HCOOH,每转移1mol ,放出31.2kJ的热量 ,放出31.2kJ的热量 |
您最近一年使用:0次
解题方法
3 . 烯烃是重要的化工原料,如乙烯、苯乙烯、丁二烯等。
(1)目前生产苯乙烯的方法主要是乙苯脱氢法,反应原理如下:
①则
___________ 。
②实际生产过程中,通常向乙苯中掺入水蒸气,保持体系总压为常压(101kPa)的条件下进行反应。掺入水蒸气的目的是___________ 。
③乙苯的平衡转化率与温度、投料比 的关系如图所示。
的关系如图所示。 ,保持体系总压为常压(101kPa),则A点温度下,该反应的平衡常数
,保持体系总压为常压(101kPa),则A点温度下,该反应的平衡常数
___________ kPa(列出计算式即可, 为用平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数)。
为用平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数)。
(2) 经催化加氢合成乙烯:
经催化加氢合成乙烯:
 。恒容条件下,按
。恒容条件下,按 投料,各物质平衡浓度变化与温度的关系如图所示:
投料,各物质平衡浓度变化与温度的关系如图所示:___________ 、___________ 的浓度。
②升高温度,平衡常数K___________ (填“减小”、“增大”或“不变”)。A点,
___________ (用 表示)。写出能提高乙烯平衡产率的措施
表示)。写出能提高乙烯平衡产率的措施___________ (任举两种)。
(3)丁二烯与卤素反应为有机合成的重要步骤,1,3-丁二烯和 反应的能量随反应过程的变化关系如图所示:
反应的能量随反应过程的变化关系如图所示: 反应会生成两种产物,一种称为动力学产物,由速率更快的反应生成;一种称为热力学产物,由产物更加稳定的反应生成。则动力学产物结构简式为
反应会生成两种产物,一种称为动力学产物,由速率更快的反应生成;一种称为热力学产物,由产物更加稳定的反应生成。则动力学产物结构简式为___________ 。
②T℃时在2L刚性密闭容器中充入1,3-丁二烯(g)( )和
)和 各2mol,发生反应。1,3-丁二烯及产物的物质的量分数随时间的变化如下表:
各2mol,发生反应。1,3-丁二烯及产物的物质的量分数随时间的变化如下表:
在0~20min内,反应体系中1,4-加成产物的平均反应速率v(1,4-加成产物)=___________ 。
(1)目前生产苯乙烯的方法主要是乙苯脱氢法,反应原理如下:
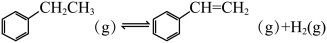
 。
。
| 共价键 |  |  |  |  |
键能 | 347.7 | 413.4 | 615 | 436 |

②实际生产过程中,通常向乙苯中掺入水蒸气,保持体系总压为常压(101kPa)的条件下进行反应。掺入水蒸气的目的是
③乙苯的平衡转化率与温度、投料比
 的关系如图所示。
的关系如图所示。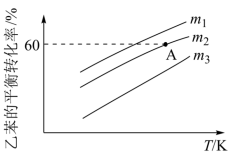
 ,保持体系总压为常压(101kPa),则A点温度下,该反应的平衡常数
,保持体系总压为常压(101kPa),则A点温度下,该反应的平衡常数
 为用平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数)。
为用平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数)。(2)
 经催化加氢合成乙烯:
经催化加氢合成乙烯:
 。恒容条件下,按
。恒容条件下,按 投料,各物质平衡浓度变化与温度的关系如图所示:
投料,各物质平衡浓度变化与温度的关系如图所示: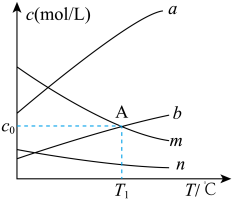
②升高温度,平衡常数K

 表示)。写出能提高乙烯平衡产率的措施
表示)。写出能提高乙烯平衡产率的措施(3)丁二烯与卤素反应为有机合成的重要步骤,1,3-丁二烯和
 反应的能量随反应过程的变化关系如图所示:
反应的能量随反应过程的变化关系如图所示: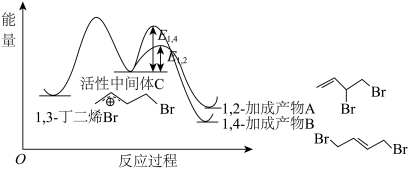
 反应会生成两种产物,一种称为动力学产物,由速率更快的反应生成;一种称为热力学产物,由产物更加稳定的反应生成。则动力学产物结构简式为
反应会生成两种产物,一种称为动力学产物,由速率更快的反应生成;一种称为热力学产物,由产物更加稳定的反应生成。则动力学产物结构简式为②T℃时在2L刚性密闭容器中充入1,3-丁二烯(g)(
 )和
)和 各2mol,发生反应。1,3-丁二烯及产物的物质的量分数随时间的变化如下表:
各2mol,发生反应。1,3-丁二烯及产物的物质的量分数随时间的变化如下表:| 时间(min) | 0 | 10 | 20 | 30 | 40 |
| 1,3-丁二烯 | 100% | 72% | 0% | 0% | 0% |
| 1,2-加成产物 | 0% | 26% | 10% | 4% | 4% |
| 1,4-加成产物 | 0% | 2% | 90% | 96% | 96% |
您最近一年使用:0次
4 . 利用平衡移动原理,分析一定温度下 在不同pH的
在不同pH的 体系中的可能产物。
体系中的可能产物。 体系中各含碳粒子的物质的量分数与pH的关系。
体系中各含碳粒子的物质的量分数与pH的关系。
ii.图2中曲线Ⅰ的离子浓度关系符合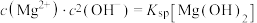 ;曲线Ⅱ的离子浓度关系符合;
;曲线Ⅱ的离子浓度关系符合; [注:起始
[注:起始 ,不同pH下
,不同pH下 由图1得到]。
由图1得到]。
iii. 。下列说法不正确的是
。下列说法不正确的是
 在不同pH的
在不同pH的 体系中的可能产物。
体系中的可能产物。
 体系中各含碳粒子的物质的量分数与pH的关系。
体系中各含碳粒子的物质的量分数与pH的关系。ii.图2中曲线Ⅰ的离子浓度关系符合
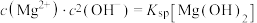 ;曲线Ⅱ的离子浓度关系符合;
;曲线Ⅱ的离子浓度关系符合; [注:起始
[注:起始 ,不同pH下
,不同pH下 由图1得到]。
由图1得到]。iii.
 。下列说法不正确的是
。下列说法不正确的是A. |
B.初始状态 , ,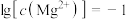 时,发生反应: 时,发生反应: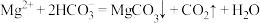 |
C.初始状态 、 、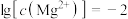 ,平衡后溶液中存在 ,平衡后溶液中存在 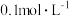 |
D.反应 的平衡常数 的平衡常数 |
您最近一年使用:0次
5 . 湿法炼锌的主要工序有焙烧、浸出、净化和电积,浸出后获得大量的含Zn、Co、Ni、Fe、Mn、Cd等金属的钴镍渣,为有效回收钴镍渣中的有价金属,设计如图所示的工艺流程:___________ (填1条即可)。“酸溶”时却不宜采用加热的方法来加快反应速率,其原因是___________ 。
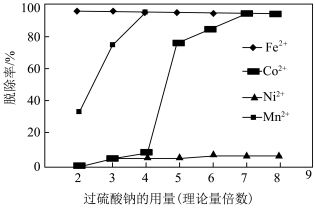
(2)“氧化分离”时,过硫酸钠的用量与溶液中金属离子的脱除率的关系如图所示。___________ (填字母)倍。
a.2~3 b.4~5 c.7~8
(3)滤渣1中主要含MnO2、_______ ,写出生成MnO2的离子方程式:_________ 。
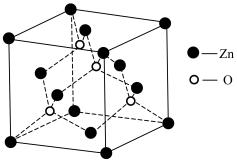
(4)由碱式碳酸锌可制备ZnO,ZnO的晶胞结构如图,则锌的配位数为___________ ;已知晶胞参数为acm,该晶体的密度为___________ g∙cm-3 (列出计算式,阿伏加德罗常数的值为NA)。
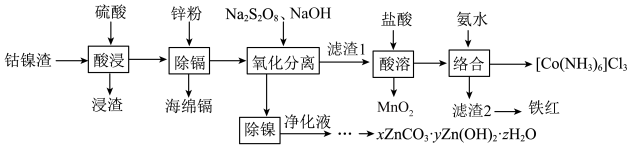
(2)“氧化分离”时,过硫酸钠的用量与溶液中金属离子的脱除率的关系如图所示。
①氧化剂Na2S2O8的阴离子结构为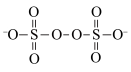 ,其中硫元素化合价为
,其中硫元素化合价为
a.2~3 b.4~5 c.7~8
(3)滤渣1中主要含MnO2、
(4)由碱式碳酸锌可制备ZnO,ZnO的晶胞结构如图,则锌的配位数为
您最近一年使用:0次
解题方法
6 . 草酸镍晶体( ,
,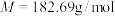 )是一种难溶于水的浅绿色粉末,常用于制镍催化剂和镍粉等。工业上用废镍催化剂(主要成分为Ni,含有一定量的
)是一种难溶于水的浅绿色粉末,常用于制镍催化剂和镍粉等。工业上用废镍催化剂(主要成分为Ni,含有一定量的 、FeO、
、FeO、 、CaO等)制备草酸镍晶体的流程如图所示:
、CaO等)制备草酸镍晶体的流程如图所示:
②
③pH增大, 被氧化的速率加快,同时生成的
被氧化的速率加快,同时生成的 水解形成更多的胶体能吸附
水解形成更多的胶体能吸附 。
。
④当某物质浓度小于 时,视为完全沉淀。
时,视为完全沉淀。
回答下列问题:
(1)写出一种能提高“酸浸”速率的措施___________ 。
(2)“氧化”过程中,控制70℃、pH小于3的条件下进行。
① 的电子式为
的电子式为___________ 。
②“氧化”过程的离子方程式为___________ 。
③pH为3~4时,镍的回收率降低的原因是___________ 。
(3)“调pH”的范围为___________ ,“沉钙”过程中,当 沉淀完全时,溶液中
沉淀完全时,溶液中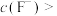
___________  (列出计算式即可)。
(列出计算式即可)。
(4)操作a包含过滤、用乙醇洗涤、110℃下烘干等步骤。过滤后检验草酸镍晶体是否洗涤干净的方法是___________ 。
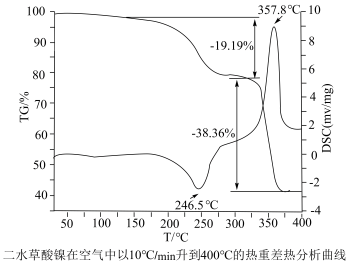
(5)在空气中加热草酸镍晶体得到如下TG-DSC热分解曲线如图所示,已知:TG指的是在程序控制温度下测量待测样品的质量与温度变化关系,DSC指通过单独的加热器补偿样品在加热过程中发生的热量变化,以保持样品和参比物的温差为零。这种补偿能量即样品吸收(峰向下)或放出(峰向上)的热量。则300℃时,反应的化学方程式为___________ 。
 ,
,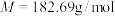 )是一种难溶于水的浅绿色粉末,常用于制镍催化剂和镍粉等。工业上用废镍催化剂(主要成分为Ni,含有一定量的
)是一种难溶于水的浅绿色粉末,常用于制镍催化剂和镍粉等。工业上用废镍催化剂(主要成分为Ni,含有一定量的 、FeO、
、FeO、 、CaO等)制备草酸镍晶体的流程如图所示:
、CaO等)制备草酸镍晶体的流程如图所示: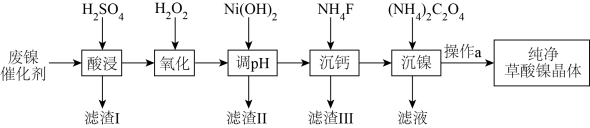
| 金属离子 |  |  |  |  |
| 开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
| 完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |

③pH增大,
 被氧化的速率加快,同时生成的
被氧化的速率加快,同时生成的 水解形成更多的胶体能吸附
水解形成更多的胶体能吸附 。
。④当某物质浓度小于
 时,视为完全沉淀。
时,视为完全沉淀。回答下列问题:
(1)写出一种能提高“酸浸”速率的措施
(2)“氧化”过程中,控制70℃、pH小于3的条件下进行。
①
 的电子式为
的电子式为②“氧化”过程的离子方程式为
③pH为3~4时,镍的回收率降低的原因是
(3)“调pH”的范围为
 沉淀完全时,溶液中
沉淀完全时,溶液中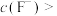
 (列出计算式即可)。
(列出计算式即可)。(4)操作a包含过滤、用乙醇洗涤、110℃下烘干等步骤。过滤后检验草酸镍晶体是否洗涤干净的方法是
(5)在空气中加热草酸镍晶体得到如下TG-DSC热分解曲线如图所示,已知:TG指的是在程序控制温度下测量待测样品的质量与温度变化关系,DSC指通过单独的加热器补偿样品在加热过程中发生的热量变化,以保持样品和参比物的温差为零。这种补偿能量即样品吸收(峰向下)或放出(峰向上)的热量。则300℃时,反应的化学方程式为
您最近一年使用:0次
7 . 下列实验操作及现象所得结论正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向碳酸钙的悬浊液中通入NO2,悬浊液逐渐变澄清 |  酸性强于 酸性强于 |
| B | 向新制的Cu(OH)2中滴入用碱中和后的蔗糖水解液,加热,产生砖红色沉淀 | 蔗糖已完全水解 |
| C | 取某补铁剂溶于硝酸,向所得溶液中滴加KSCN溶液,溶液变红色 | 该补铁剂中铁元素的化合价为+3价 |
| D | 向CuCl2、MgCl2的混合溶液中滴加NaOH溶液,溶液中先生成蓝色沉淀 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 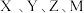 是原子序数依次增大的短周期主族元素,
是原子序数依次增大的短周期主族元素, 与
与 同主族,
同主族, 原子的最外层电子数是次外层电子数的2倍,
原子的最外层电子数是次外层电子数的2倍, 原子的最外层电子数等于其电子层数,
原子的最外层电子数等于其电子层数, 与
与 原子的质子数之和等于
原子的质子数之和等于 与
与 原子的质子数之和。下列说法不正确的是
原子的质子数之和。下列说法不正确的是
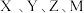 是原子序数依次增大的短周期主族元素,
是原子序数依次增大的短周期主族元素, 与
与 同主族,
同主族, 原子的最外层电子数是次外层电子数的2倍,
原子的最外层电子数是次外层电子数的2倍, 原子的最外层电子数等于其电子层数,
原子的最外层电子数等于其电子层数, 与
与 原子的质子数之和等于
原子的质子数之和等于 与
与 原子的质子数之和。下列说法不正确的是
原子的质子数之和。下列说法不正确的是A.电负性: |
B. 与 与 形成的化合物中 形成的化合物中 的杂化方式为 的杂化方式为 |
C.简单氢化物的沸点: |
| D.X、Y的最高价氧化物对应的水化物均为强酸 |
您最近一年使用:0次
解题方法
9 . 有机物 为药物合成的中间体,其结构简式为
为药物合成的中间体,其结构简式为 ,下列说法不正确的是
,下列说法不正确的是
A. 的分子式为 的分子式为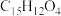 |
B.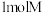 分别与足量 分别与足量 溶液、金属钠反应,产生相同状况下的体体积比为 溶液、金属钠反应,产生相同状况下的体体积比为 |
| C.M可发生氧化反应、取代反应 |
D.与浓溴水反应,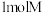 最多可消耗 最多可消耗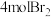 |
您最近一年使用:0次
10 . 化合物G是合成抗HIV药物福沙那韦的关键中间体,其一种合成路线如下:___________ 。D→E的反应类型是___________ 。
(2)化合物B分子式为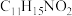 ,B的结构简式是
,B的结构简式是___________ ;化合物X分子式为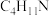 ,X的结构简式是
,X的结构简式是___________ 。
(3)满足下列条件的A的同分异构体有___________ 种。
①比A少一个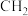 ;
;
②能发生银镜反应;
③与 溶液不能发生显色反应,但能发生水解反应,且水解反应的产物之一可以与
溶液不能发生显色反应,但能发生水解反应,且水解反应的产物之一可以与 溶液发生显色反应。
溶液发生显色反应。
请写出其中核磁共振氢谱图峰面积之比为1∶2∶2∶2∶2的M的结构简式___________ 。
(4)写出以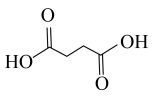 为原料制备
为原料制备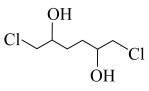 的合成路线流程图(无机试剂和流程中的有机试剂任用,合成路线流程图示例见本题题干)
的合成路线流程图(无机试剂和流程中的有机试剂任用,合成路线流程图示例见本题题干)___________ 。

已知:①―Boc为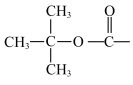 的简写;②
的简写;②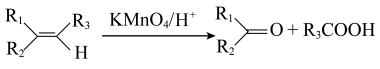
(2)化合物B分子式为
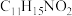 ,B的结构简式是
,B的结构简式是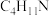 ,X的结构简式是
,X的结构简式是(3)满足下列条件的A的同分异构体有
①比A少一个
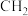 ;
;②能发生银镜反应;
③与
 溶液不能发生显色反应,但能发生水解反应,且水解反应的产物之一可以与
溶液不能发生显色反应,但能发生水解反应,且水解反应的产物之一可以与 溶液发生显色反应。
溶液发生显色反应。请写出其中核磁共振氢谱图峰面积之比为1∶2∶2∶2∶2的M的结构简式
(4)写出以
 为原料制备
为原料制备 的合成路线流程图(无机试剂和流程中的有机试剂任用,合成路线流程图示例见本题题干)
的合成路线流程图(无机试剂和流程中的有机试剂任用,合成路线流程图示例见本题题干)
您最近一年使用:0次



