名校
解题方法
1 . 石柱黄连是重庆市石柱土家族自治县特产,其中含有的一种有机物M的结构如图所示,下列有关M的说法正确的是
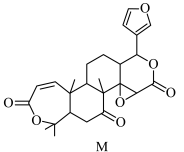
| A.含氧官能团有2种 | B.易溶于水和有机溶剂 |
| C.碳原子的杂化类型有2种 | D.所有碳原子有可能在同一平面上 |
您最近一年使用:0次
名校
解题方法
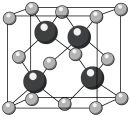
2 . M、W、X、Y、Z是五种短周期原子序数依次增大的主族元素,基态W原子的价层电子排布式为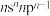 ,Y是空气中含量最多的元素,液态Z2为浅蓝色液体。五种元素形成的一种化合物F的结构如图所示。下列说法错误的是
,Y是空气中含量最多的元素,液态Z2为浅蓝色液体。五种元素形成的一种化合物F的结构如图所示。下列说法错误的是
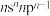 ,Y是空气中含量最多的元素,液态Z2为浅蓝色液体。五种元素形成的一种化合物F的结构如图所示。下列说法错误的是
,Y是空气中含量最多的元素,液态Z2为浅蓝色液体。五种元素形成的一种化合物F的结构如图所示。下列说法错误的是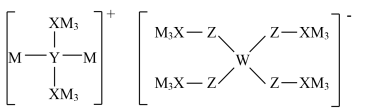
| A.最简单氢化物键角:X>Y |
| B.晶体F为离子晶体 |
| C.Y的氢化物的VSEPR模型名称为三角锥形 |
| D.F中X、Y和Z原子采取的杂化类型相同 |
您最近一年使用:0次
名校
解题方法
3 . 半导体在集成电路、消费电子、通信系统、光伏发电、照明、大功率电源转换等领域都有应用。
(1)硅是常见的半导体材料。金刚石和硅相比较,熔点更高的是___________ ,原因是___________ 。硅有晶体硅和无定形硅,可以用___________ (填方法名称)来区分晶体硅和无定形硅。
(2)2022年,科研人员发现立方砷化硼是科学界已知的最好的半导体之一,其结构如图所示。基态As原子核外电子有___________ 种空间运动状态;立方砷化硼中,___________ (填“含有”或“不含有”)配位键。
(4)砷化镓被誉为“半导体贵族”,是雷达、电子计算机、人造卫星、宇宙飞船等高新产品中不可或缺的材料。已知GaAs晶胞结构如图所示,其晶胞棱长为apm。1号原子的分数坐标为___________ ;1号原子和2号原子之间的距离为___________ pm;晶胞密度为___________  (阿伏加德罗常数的值用
(阿伏加德罗常数的值用 表示)。
表示)。
(1)硅是常见的半导体材料。金刚石和硅相比较,熔点更高的是
(2)2022年,科研人员发现立方砷化硼是科学界已知的最好的半导体之一,其结构如图所示。基态As原子核外电子有
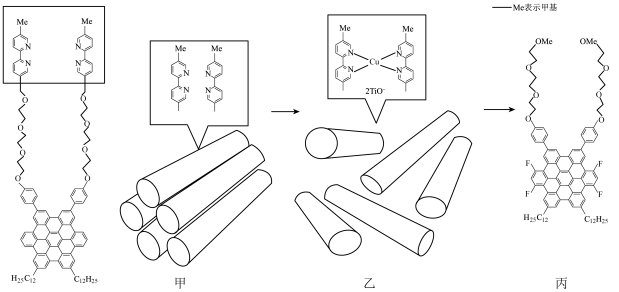
| A.分子识别和自组装是超分子的重要特征 |
| B.甲分子中的氮原子的杂化方式均为sp2 |
C.乙分子图示结构部分中,1个 形成了2个配位键 形成了2个配位键 |
| D.丙分子中存在氢键 |
(4)砷化镓被誉为“半导体贵族”,是雷达、电子计算机、人造卫星、宇宙飞船等高新产品中不可或缺的材料。已知GaAs晶胞结构如图所示,其晶胞棱长为apm。1号原子的分数坐标为
 (阿伏加德罗常数的值用
(阿伏加德罗常数的值用 表示)。
表示)。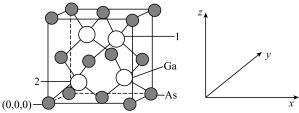
您最近一年使用:0次
4 . 某同学利用下列装置(加热和夹持装置已省略)分离CH2Cl2(沸点为39.8℃)和CCl4(沸点为76.5℃),下列说法错误的是
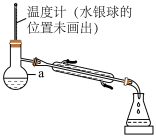
| A.仪器a的名称为蒸馏烧瓶 |
| B.冷凝水从下口进 |
| C.实验中可以用水浴进行加热,且温度计的水银球应靠近支管口 |
| D.可以用球形冷凝管代替直形冷凝管进行实验 |
您最近一年使用:0次
5 . 下列化学用语或有机物的命名正确的是
A. 的系统命名为2,4-二乙基戊烷 的系统命名为2,4-二乙基戊烷 |
B.甲烷的空间填充模型为 |
C.新戊烷的结构简式为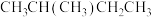 |
D.化学式为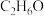 且核磁共振氢谱有三组峰的物质的结构式为 且核磁共振氢谱有三组峰的物质的结构式为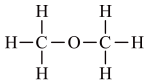 |
您最近一年使用:0次
6 . 铋的配合物具有较低的毒性,已被应用于多种药物中,一种Bi(Ⅲ)的配合物R的制备方法如图,下列说法错误的是
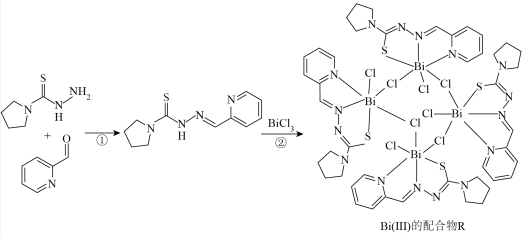
| A.反应①为加成反应 | B.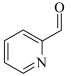 分子中含有醛基 分子中含有醛基 |
C.配合物R中, 的配位数为6 的配位数为6 | D.基态83Bi的价层电子排布式为6s26p3 |
您最近一年使用:0次
7 . 某矿石中富含 和
和 ,还含有Fe、Al、Si、Ca的氧化物。以该矿石为原料制备
,还含有Fe、Al、Si、Ca的氧化物。以该矿石为原料制备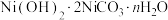 的流程如图所示,请回答下列问题:
的流程如图所示,请回答下列问题:
②Ni2O3在酸性条件下具有强氧化性。
(1)基态Ni原子的简化电子排布式为___________ ;基态 的价层电子轨道表示式为
的价层电子轨道表示式为___________ 。
(2)滤渣1的主要成分为___________ ;加入Ni2O3后生成 的离子方程式为
的离子方程式为___________ 。
(3)“萃取”时发生的反应: ,“反萃取”时加入稀硫酸的目的是
,“反萃取”时加入稀硫酸的目的是___________ 。一种有机萃取剂M及萃取 后生成的N的结构如图所示,M中碳原子的杂化方式有
后生成的N的结构如图所示,M中碳原子的杂化方式有___________ 种;N中Cu元素的化合价为___________ 价,N中提供孤电子对形成配位键的原子有___________ (填标号)。___________ 。
 和
和 ,还含有Fe、Al、Si、Ca的氧化物。以该矿石为原料制备
,还含有Fe、Al、Si、Ca的氧化物。以该矿石为原料制备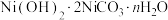 的流程如图所示,请回答下列问题:
的流程如图所示,请回答下列问题: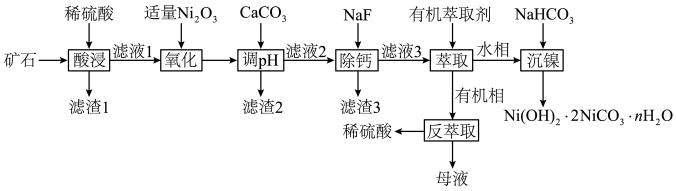
| 金属离子 |  |  |  |  |  |
| 开始沉淀的pH | 7.5 | 2.2 | 3.7 | 4.7 | 7.0 |
| 完全沉淀的pH | 9.0 | 3.3 | 4.5 | 6.5 | 8.7 |
(1)基态Ni原子的简化电子排布式为
 的价层电子轨道表示式为
的价层电子轨道表示式为(2)滤渣1的主要成分为
 的离子方程式为
的离子方程式为(3)“萃取”时发生的反应:
 ,“反萃取”时加入稀硫酸的目的是
,“反萃取”时加入稀硫酸的目的是 后生成的N的结构如图所示,M中碳原子的杂化方式有
后生成的N的结构如图所示,M中碳原子的杂化方式有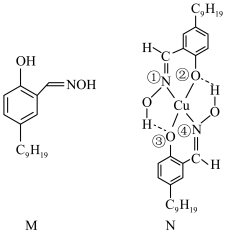
您最近一年使用:0次
名校
解题方法
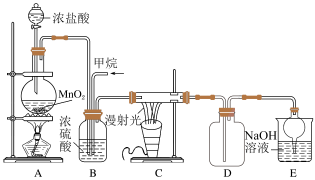
8 . 某化学兴趣小组利用如图所示实验装置探究甲烷与Cl2的反应。
(1)CH4中C的杂化类型为___________ ,H2O为___________ (填“极性”或“非极性”)分子。
(2)A中生成Cl2反应的离子方程式为___________ ;D中收集到的液体呈黄绿色,原因是___________ 。
(3)B装置有三种功能:①控制气流速率;②___________ ;③___________ 。
(4)C中生成CH3Cl反应的化学方程式为___________ ;若反应消耗了1 molCH4,且生成4种物质的量相等的有机物,则C中消耗了___________ molCl2。
(1)CH4中C的杂化类型为
(2)A中生成Cl2反应的离子方程式为
(3)B装置有三种功能:①控制气流速率;②
(4)C中生成CH3Cl反应的化学方程式为
您最近一年使用:0次
名校
解题方法
9 . 下列说法错误的是
| A.相同质量的H2O(l)的体积小于H2O(s)的,原因之一是H2O(l)中含有更多的氢键 |
B.等物质的量的 、 、 中含σ键的个数之比为3:4 中含σ键的个数之比为3:4 |
C.已知 的4s轨道和4p轨道可以形成sp3杂化轨道,则 的4s轨道和4p轨道可以形成sp3杂化轨道,则 的空间结构可能为正四面体形 的空间结构可能为正四面体形 |
| D.晶体具有自范性,能自发地呈现多面体外形 |
您最近一年使用:0次

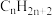 的有机物一定是烷烃
的有机物一定是烷烃

