名校
1 . 恒温恒容条件下,对于反应
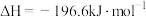 ,能量变化如图所示。下列说法中不正确的是
,能量变化如图所示。下列说法中不正确的是
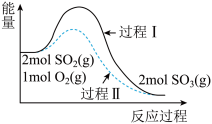

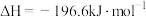 ,能量变化如图所示。下列说法中不正确的是
,能量变化如图所示。下列说法中不正确的是
A.由题意可知,反应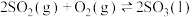 的 的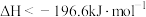 |
B.增大氧气浓度,平衡正向移动,平衡常数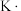 增大 增大 |
| C.与过程I相比,过程II加入了催化剂,增大了活化分子百分数 |
| D.若恒温恒压条件下充入惰性气体,反应速率会降低 |
您最近一年使用:0次
2023-12-14更新
|
272次组卷
|
2卷引用:重庆市第十一中学校2023-2024学年高二上学期期中考试化学试题
名校
2 . 不同温度下,向恒容密闭容器中按物质的量之比3:1充入 和
和 ,发生反应:
,发生反应: 。反应相同的时间,
。反应相同的时间, 转化率随温度的变化关系如图所示。下列说法正确的是
转化率随温度的变化关系如图所示。下列说法正确的是

 和
和 ,发生反应:
,发生反应: 。反应相同的时间,
。反应相同的时间, 转化率随温度的变化关系如图所示。下列说法正确的是
转化率随温度的变化关系如图所示。下列说法正确的是
A. 在M点和N点有相同的转化率,可知化学平衡常数 在M点和N点有相同的转化率,可知化学平衡常数 |
B.由图像可知,该反应的焓变 |
C. 的转化率随温度的变化关系与上图完全一致 的转化率随温度的变化关系与上图完全一致 |
D.若 和 和 的初始投料量分别为3mol、1mol,列三段式可求N点的平衡常数 的初始投料量分别为3mol、1mol,列三段式可求N点的平衡常数 |
您最近一年使用:0次
名校
解题方法
3 . 下列实验方案和实验目的(或结论)正确的是
| 序号 | 实验方案 | 实验目的(或结论) |
| A | 向等体积等浓度的 溶液中分别加入6滴等浓度的 溶液中分别加入6滴等浓度的 和 和 溶液,观察气体产生的速度 溶液,观察气体产生的速度 | 比较 和 和 的催化效果 的催化效果 |
| B | 向5mLKI溶液中加入5滴同浓度的 溶液,充分反应后再加入几滴KSCN溶液,溶液显红色 溶液,充分反应后再加入几滴KSCN溶液,溶液显红色 |  与KI的反应是可逆反应 与KI的反应是可逆反应 |
| C | 向碳酸氢钠溶液中滴加醋酸溶液,有气泡产生 | 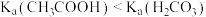 |
| D | 相同温度下,用pH计分别测定HCl溶液和 溶液的pH值 溶液的pH值 | 比较 和HCl的酸性强弱 和HCl的酸性强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 常温下用浓度为 的NaOH标准溶液滴定10mL浓度均为
的NaOH标准溶液滴定10mL浓度均为 的HCl和
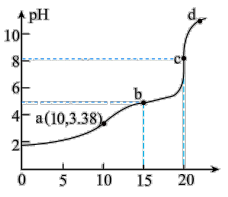
的HCl和 的混合溶液,滴定过程中溶液的pH随NaOH加入体积(V)的变化曲线如图所示。下列说法错误的是
的混合溶液,滴定过程中溶液的pH随NaOH加入体积(V)的变化曲线如图所示。下列说法错误的是
 的NaOH标准溶液滴定10mL浓度均为
的NaOH标准溶液滴定10mL浓度均为 的HCl和
的HCl和 的混合溶液,滴定过程中溶液的pH随NaOH加入体积(V)的变化曲线如图所示。下列说法错误的是
的混合溶液,滴定过程中溶液的pH随NaOH加入体积(V)的变化曲线如图所示。下列说法错误的是
| A.起点到a点的过程中,水的电离一直受到抑制 |
B.10mL处溶液的溶质组成为NaCl、 |
| C.c点可选择甲基橙溶液作为指示制 |
D.忽略水的电离,由图可计算出 的电离平衡常数 的电离平衡常数 约为 约为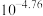 |
您最近一年使用:0次
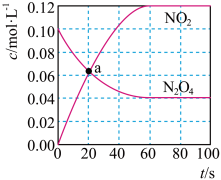
5 . T℃时,将 气体充入1L刚性密闭容器中发生反应
气体充入1L刚性密闭容器中发生反应
 、
、 的浓度随时间的变化关系如图,已知两物质的消耗速率与各自的分压有如下关系:
的浓度随时间的变化关系如图,已知两物质的消耗速率与各自的分压有如下关系: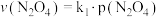 ,
,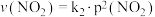 ,
, 、
、 为速率常数。已知
为速率常数。已知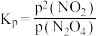 ,p表示对应物质的分压,下列说法正确的是
,p表示对应物质的分压,下列说法正确的是
 气体充入1L刚性密闭容器中发生反应
气体充入1L刚性密闭容器中发生反应
 、
、 的浓度随时间的变化关系如图,已知两物质的消耗速率与各自的分压有如下关系:
的浓度随时间的变化关系如图,已知两物质的消耗速率与各自的分压有如下关系: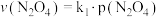 ,
,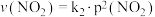 ,
, 、
、 为速率常数。已知
为速率常数。已知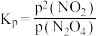 ,p表示对应物质的分压,下列说法正确的是
,p表示对应物质的分压,下列说法正确的是
A.若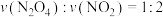 时,说明该反应达到平衡状态 时,说明该反应达到平衡状态 |
B.a点:反应物和生成物浓度相等,所以 |
C.该温度下反应的平衡常数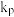 与 与 、 、 间的关系为 间的关系为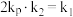 |
D.若反应开始时总压为p,则反应 的压强平衡常数为 的压强平衡常数为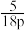 |
您最近一年使用:0次
名校
6 . 室温下,下列各组离子在指定溶液中一定能大量共存的是
A.由水电离产生的 为 为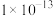 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C.加甲基橙呈红色的溶液中: 、 、 、 、 、 、 |
D.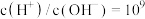 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
7 . 以下对图像的描述错误的是
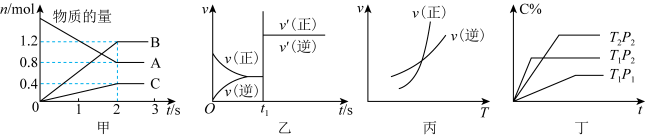

A.若图甲容器的体积为2L,发生反应 ,则0~2s内的平均反应速率 ,则0~2s内的平均反应速率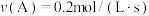 |
B.图乙:某温度下发生反应 , , 时刻改变的条件可以是加入催化剂或者增大体系压强(缩小容器体积) 时刻改变的条件可以是加入催化剂或者增大体系压强(缩小容器体积) |
| C.图丙:对图中反应升高温度,该反应平衡常数增大,正反应为吸热反应 |
D.图丁:对于反应 , , , ,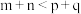 |
您最近一年使用:0次
名校
8 . 在80℃时,在甲、乙、丙三个恒容密闭容器中投入 和
和 混合气体,发生反应:
混合气体,发生反应: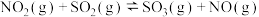 。起始浓度如下表所示,其中甲经5min达到平衡,平衡时
。起始浓度如下表所示,其中甲经5min达到平衡,平衡时 的转化率为60%。下列判断错误的是
的转化率为60%。下列判断错误的是
 和
和 混合气体,发生反应:
混合气体,发生反应: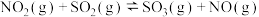 。起始浓度如下表所示,其中甲经5min达到平衡,平衡时
。起始浓度如下表所示,其中甲经5min达到平衡,平衡时 的转化率为60%。下列判断错误的是
的转化率为60%。下列判断错误的是| 容器 | 甲 | 乙 | 丙 |
 | 0.10 | 0.20 | 0.20 |
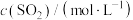 | 0.10 | 0.10 | 0.20 |
A.达平衡时,乙中 的转化率小于60% 的转化率小于60% |
B.达平衡时,丙中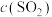 是甲中的2倍 是甲中的2倍 |
| C.温度升至90℃,上述反应的平衡常数的数值变为2,则正反应为吸热反应 |
D.保持其他条件不变,若起始时容器乙中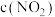 为 为 , , 为 为 ,则达到平衡时 ,则达到平衡时 与乙的原平衡相同 与乙的原平衡相同 |
您最近一年使用:0次
2023-12-13更新
|
215次组卷
|
2卷引用:重庆市第十一中学校2023-2024学年高二上学期期中考试化学试题
名校
解题方法
9 . 工业上用CO或 与
与 反应可得到多种有机物。
反应可得到多种有机物。
(1)已知CO和 制备甲醇的有关反应以及在不同温度下的平衡常数如下表所示:
制备甲醇的有关反应以及在不同温度下的平衡常数如下表所示:
 、
、 、
、 之间的关系为:
之间的关系为:
_______ 。
(2)在密闭容器中充入2molCO与 ,发生反应,
,发生反应, ,CO的平衡转化率与温度、压强的关系如图所示:
,CO的平衡转化率与温度、压强的关系如图所示:

① 是
是_______ 反应。(填“放热”或“吸热”)
②下列叙述能说明反应达到平衡状态的是_______ 。
A.CO的体积分数不再发生变化 B.恒容条件下混合气体的密度不再发生变化
C.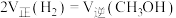 D.恒容条件下混合气体的压强不再发生变化
D.恒容条件下混合气体的压强不再发生变化
③A、B、C三点的平衡常数 、
、 、
、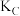 的由大到小的关系是
的由大到小的关系是_______ 。
④若A点时容器的容积为2L。则A点的平衡常数为_______ 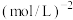 。
。
(3)若在2L恒容密闭容器中充入2molCO和4molH2,反应过程中,体系的压强与时间的关系如图所示,平衡时的温度与起始温度相同,曲线Ⅱ为只改变某一条件的变化曲线。

①曲线Ⅱ改变的条件可能是_______ ;
②该条件下 的平衡转化率为
的平衡转化率为_______ ;
③曲线Ⅰ在前10分钟内以 表示的平均速率为
表示的平均速率为_______ 。
 与
与 反应可得到多种有机物。
反应可得到多种有机物。(1)已知CO和
 制备甲醇的有关反应以及在不同温度下的平衡常数如下表所示:
制备甲醇的有关反应以及在不同温度下的平衡常数如下表所示:| 化学反应 | 平衡常数 | 温度/℃ | |
| 500 | 800 | ||
① |  | 2.5 | 0.15 |
② |  | 1.0 | 2.5 |
③ |  | ||
 、
、 、
、 之间的关系为:
之间的关系为:
(2)在密闭容器中充入2molCO与
 ,发生反应,
,发生反应, ,CO的平衡转化率与温度、压强的关系如图所示:
,CO的平衡转化率与温度、压强的关系如图所示:
①
 是
是②下列叙述能说明反应达到平衡状态的是
A.CO的体积分数不再发生变化 B.恒容条件下混合气体的密度不再发生变化
C.
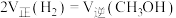 D.恒容条件下混合气体的压强不再发生变化
D.恒容条件下混合气体的压强不再发生变化③A、B、C三点的平衡常数
 、
、 、
、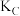 的由大到小的关系是
的由大到小的关系是④若A点时容器的容积为2L。则A点的平衡常数为
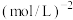 。
。(3)若在2L恒容密闭容器中充入2molCO和4molH2,反应过程中,体系的压强与时间的关系如图所示,平衡时的温度与起始温度相同,曲线Ⅱ为只改变某一条件的变化曲线。

①曲线Ⅱ改变的条件可能是
②该条件下
 的平衡转化率为
的平衡转化率为③曲线Ⅰ在前10分钟内以
 表示的平均速率为
表示的平均速率为
您最近一年使用:0次
名校
解题方法
10 . 化学反应中均伴随着能量的变化,回答下列问题:
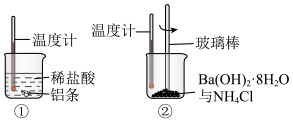
(1)某同学进行如下实验,图①和②中温度计示数降低的是_______ ;
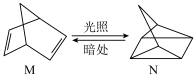
(2)有机物M可转化成N,转化过程如下,则M、N相比,较稳定的是_______ ;
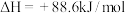
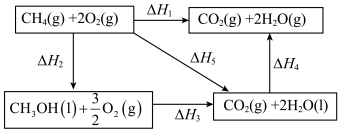
(3)已知 在一定条件下可发生如图的一系列反应,下列说法正确的是_______;
在一定条件下可发生如图的一系列反应,下列说法正确的是_______;
(4)金属Ni可活化 放出
放出 ,其反应历程如图所示:
,其反应历程如图所示:
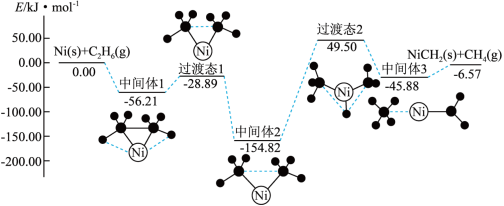
下列关于活化历程的说法正确的是_______。
(5) 与
与 经催化重整,制得合成气:
经催化重整,制得合成气: 已知上述反应中相关的化学键键能数据如下,则该反应的
已知上述反应中相关的化学键键能数据如下,则该反应的
_______ kJ/mol。
(6)在25℃、101kPa下,1g乙烷气体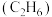 燃烧生成
燃烧生成 和液态水时放热QkJ,则表示乙烷燃烧热的热化学方程式为
和液态水时放热QkJ,则表示乙烷燃烧热的热化学方程式为_______ 。
(7)中和热的测定实验中,取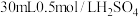 溶液与50mL0.5mol/LNaOH溶液进行中和反应,三次实验温度平均升高4℃,已知溶液的比热容近似为
溶液与50mL0.5mol/LNaOH溶液进行中和反应,三次实验温度平均升高4℃,已知溶液的比热容近似为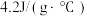 ,溶液的密度均近似为
,溶液的密度均近似为 。通过计算可得稀硫酸和稀NaOH溶液的中和热
。通过计算可得稀硫酸和稀NaOH溶液的中和热
_______ kJ/mol。
(1)某同学进行如下实验,图①和②中温度计示数降低的是

(2)有机物M可转化成N,转化过程如下,则M、N相比,较稳定的是

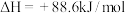
(3)已知
 在一定条件下可发生如图的一系列反应,下列说法正确的是_______;
在一定条件下可发生如图的一系列反应,下列说法正确的是_______;
A. | B.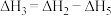 |
C. | D. |
(4)金属Ni可活化
 放出
放出 ,其反应历程如图所示:
,其反应历程如图所示:
下列关于活化历程的说法正确的是_______。
| A.中间体1→中间体2的过程是放热过程 |
| B.加入催化剂可降低该反应的反应热,加快反应速率 |
C.1molNi和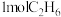 的总能量小于 的总能量小于 和 和 的总能量 的总能量 |
| D.中间体2→中间体3的过程是决速步骤 |
(5)
 与
与 经催化重整,制得合成气:
经催化重整,制得合成气: 已知上述反应中相关的化学键键能数据如下,则该反应的
已知上述反应中相关的化学键键能数据如下,则该反应的
| 化学键 |  |  |  | 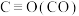 |
| 键能/(kJ/mol) | 413 | 745 | 436 | 1075 |
(6)在25℃、101kPa下,1g乙烷气体
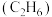 燃烧生成
燃烧生成 和液态水时放热QkJ,则表示乙烷燃烧热的热化学方程式为
和液态水时放热QkJ,则表示乙烷燃烧热的热化学方程式为(7)中和热的测定实验中,取
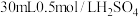 溶液与50mL0.5mol/LNaOH溶液进行中和反应,三次实验温度平均升高4℃,已知溶液的比热容近似为
溶液与50mL0.5mol/LNaOH溶液进行中和反应,三次实验温度平均升高4℃,已知溶液的比热容近似为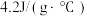 ,溶液的密度均近似为
,溶液的密度均近似为 。通过计算可得稀硫酸和稀NaOH溶液的中和热
。通过计算可得稀硫酸和稀NaOH溶液的中和热
您最近一年使用:0次



