名校
解题方法
1 . 物质世界丰富多彩,原子间通过化学键构成了各种各样的物质。请根据下列物质,完成填空。
A.干冰 B.二氧化硅 C.冰 D.金刚石 E.铜 F.氢氧化钠 G.氧化镁 H.固体碘 I.硫酸铵
(1)熔化时不需要破坏化学键的是___________ ,晶体中既有离子键,又有共价键的是___________ (用字母序号填空)。
(2)MgO、Cu和干冰的晶胞示意图如下,晶体中粒子之间主要以范德华力结合的晶体是___________ 。
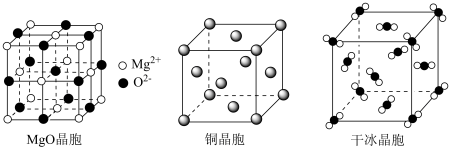
(3)基态氧原子能量最高的电子所占据的原子轨道形状为___________ ,与 相邻且最近的
相邻且最近的 个数为
个数为___________ 。
(4)基态铜原子的价电子轨道表示式为___________ 。
(5)如图是冰的结构。下列事实能解释干冰的密度比冰大的是___________ (填字母序号)。
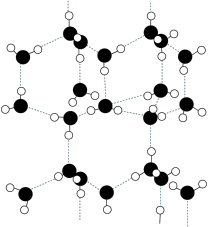
a.二氧化碳分子的质量大于水分子
b.干冰晶胞中二氧化碳分子堆积得更密集
c.水分子极性强,分子间作用力大
d.冰中氢键存在方向性,晶体有较大空隙,空间利用率低
(6)GaN晶体结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被Ga原子代替,如下图所示。若GaN晶胞边长为 ,
, 为阿伏加德罗常数,GaN的密度为
为阿伏加德罗常数,GaN的密度为___________  (1pm=1-10cm)。
(1pm=1-10cm)。
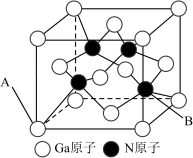
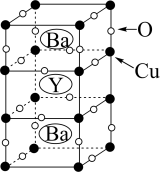
(7)钇钡铜氧是一种新型节能高温超导体,其晶胞结构如图所示。研究发现,此高温超导体中的Cu元素有两种价态,分别为+2和+3,Y元素的化合价为+3,Ba元素的化合价为+2,该物质中Cu2+与Cu3+的个数比为___________ 。
A.干冰 B.二氧化硅 C.冰 D.金刚石 E.铜 F.氢氧化钠 G.氧化镁 H.固体碘 I.硫酸铵
(1)熔化时不需要破坏化学键的是
(2)MgO、Cu和干冰的晶胞示意图如下,晶体中粒子之间主要以范德华力结合的晶体是

(3)基态氧原子能量最高的电子所占据的原子轨道形状为
 相邻且最近的
相邻且最近的 个数为
个数为(4)基态铜原子的价电子轨道表示式为
(5)如图是冰的结构。下列事实能解释干冰的密度比冰大的是

a.二氧化碳分子的质量大于水分子
b.干冰晶胞中二氧化碳分子堆积得更密集
c.水分子极性强,分子间作用力大
d.冰中氢键存在方向性,晶体有较大空隙,空间利用率低
(6)GaN晶体结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被Ga原子代替,如下图所示。若GaN晶胞边长为
 ,
, 为阿伏加德罗常数,GaN的密度为
为阿伏加德罗常数,GaN的密度为 (1pm=1-10cm)。
(1pm=1-10cm)。
(7)钇钡铜氧是一种新型节能高温超导体,其晶胞结构如图所示。研究发现,此高温超导体中的Cu元素有两种价态,分别为+2和+3,Y元素的化合价为+3,Ba元素的化合价为+2,该物质中Cu2+与Cu3+的个数比为

您最近一年使用:0次
名校
解题方法
2 . 活性氧化锌能对太阳光线和其他大气物质形成防护,常用于敏感皮肤的面霜和化妆品。工业上用菱锌矿(主要成分为ZnCO3,还含有Ni、Cd、Fe、Cu等元素及少量不溶于水的杂质)制备ZnO,工艺流程图所示:

(1)为了提高“溶浸”效果,可采取的措施有___________ (任写两条)。
(2)常温下Fe2+比Fe3+更容易被氧化变质,请从结构角度加以解释___________ 。
(3)“除铁”时,先加入H2O2溶液发生反应的离子方程式为___________ ;“调pH”时除ZnO外还可以选用的物质是___________ 。
a.氨水 b.氢氧化钠 c.氢氧化锌
(4)常温下pH=5时,Fe3+的浓度降到了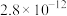 mo1/L,此时Fe(OH)3的溶度积常数的数值为
mo1/L,此时Fe(OH)3的溶度积常数的数值为___________ ,证明Fe3+已除尽的化学方法是___________ 。
(5)已知沉锌时固体产物是Zn2(OH)2CO3,写出该过程的离子方程式:___________ 。
(6)粗锌中含有少量Al、Fe、Cu等杂质,可用电解法制备高纯度锌,下列叙述正确的是___________。

(1)为了提高“溶浸”效果,可采取的措施有
(2)常温下Fe2+比Fe3+更容易被氧化变质,请从结构角度加以解释
(3)“除铁”时,先加入H2O2溶液发生反应的离子方程式为
a.氨水 b.氢氧化钠 c.氢氧化锌
(4)常温下pH=5时,Fe3+的浓度降到了
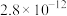 mo1/L,此时Fe(OH)3的溶度积常数的数值为
mo1/L,此时Fe(OH)3的溶度积常数的数值为(5)已知沉锌时固体产物是Zn2(OH)2CO3,写出该过程的离子方程式:
(6)粗锌中含有少量Al、Fe、Cu等杂质,可用电解法制备高纯度锌,下列叙述正确的是___________。
| A.电解过程中,阳极质量的减少与阴极质量的增加相等 |
| B.电解后,溶液中存在的金属阳离子只有Al3+、Fe2+和Zn2+ |
| C.粗锌作阳极,纯锌作阴极,电解质溶液是硫酸锌溶液 |
| D.电解后,电解槽底部的阳极泥中只有Cu |
您最近一年使用:0次
名校
解题方法
3 . A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请用化学用语回答下列问题。
(1)元素F简单离子的价电子排布式为___________ ;写出元素G在周期表中的位置___________ 。
(2)B与氢元素形成的简单气态氢化物的空间构型为___________ ,C与氢元素形成的简单气态氢化物的VSEPR模型为___________ 。
(3)C、D、E三种元素的简单离子半径由大到小的顺序为___________ (用元素符号表示)。
(4)已知元素A、B形成的 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为___________ 。
(5)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是___________ 化合物(填“离子”或“共价”);M的最高价氧化物对应的水化物与NaOH溶液反应的化学方程式为___________ 。
(6)FC—常用作消毒剂,单质砷(As)在碱性溶液中可被FC—氧化为AsO ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 电离能数据(单位: ):738、1451、7733、10540、13630…… ):738、1451、7733、10540、13630…… |
| E | 基态原子最外层电子排布式为: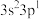 |
| F | 基态原子的最外层p轨道上2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 其中一种氧化物是有磁性的黑色固体 |
(2)B与氢元素形成的简单气态氢化物的空间构型为
(3)C、D、E三种元素的简单离子半径由大到小的顺序为
(4)已知元素A、B形成的
 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为(5)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是
(6)FC—常用作消毒剂,单质砷(As)在碱性溶液中可被FC—氧化为AsO
 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
名校
4 . 回答下列问题:
(1)根据对角线规则,在周期表中,与Li化学性质最相似的邻族元素是___________ (填元素符号),MgO的电子式为___________ 。
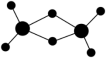
(2)实验测得AlCl3的实际存在形式为Al2Cl6,其分子的球棍模型如图所示。已知Al2Cl6分子中正负电荷中心重合,则Al2Cl6属于___________ 分子(填“极性”或“非极性”)分子,分子中Al采取___________ 杂化。
(3)下列不同状态的硼中,失去一个电子需要吸收能量最多的是___________(填标号)。
(4)PH3的电子式为___________ ;NH3很容易液化(常用作冷库中的制冷剂),而同主族的PH3却没有这样的性质,原因是:___________ 。
(5)亚硒酸钠(Na2SeO3)能消除加速人体衰老的活性氧,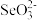 的键角小于气态分子SeO3的原因是:
的键角小于气态分子SeO3的原因是:___________ 。
(1)根据对角线规则,在周期表中,与Li化学性质最相似的邻族元素是
(2)实验测得AlCl3的实际存在形式为Al2Cl6,其分子的球棍模型如图所示。已知Al2Cl6分子中正负电荷中心重合,则Al2Cl6属于

(3)下列不同状态的硼中,失去一个电子需要吸收能量最多的是___________(填标号)。
A.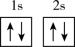 | B.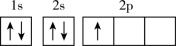 |
C.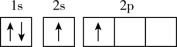 | D.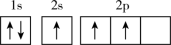 |
(5)亚硒酸钠(Na2SeO3)能消除加速人体衰老的活性氧,
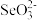 的键角小于气态分子SeO3的原因是:
的键角小于气态分子SeO3的原因是:
您最近一年使用:0次
5 . 某小组用硫铜矿煅烧废渣(主要含Fe2O3、CuO、FeO)为原料制取Cu2O,流程如图:
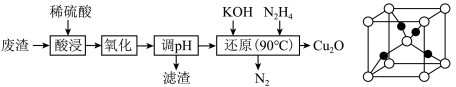
下列说法错误的是

下列说法错误的是
| A.“调节pH”时可以选择CuO或Cu(OH)2 |
| B.“还原”过程中消耗的CuSO4、N2H4的物质的量之比为4:1 |
| C.用N2H4还原制取Cu2O的优点是产生N2氛围,可防止产品被氧化 |
| D.Cu2O的晶胞结构如上图所示,1个Cu2O晶胞中含1个氧原子 |
您最近一年使用:0次
6 . 下列说法中,正确的是
| A.稀有气体中只含原子,稀有气体的晶体属于共价晶体 |
| B.共价晶体中,共价键越强,熔点越高 |
| C.CO2晶体是分子晶体,可推测SiO2晶体也是分子晶体 |
| D.分子晶体中,共价键键能越大,该分子晶体的熔沸点一定越高,分子间作用力越大,对应的物质越稳定 |
您最近一年使用:0次
名校
解题方法
7 . 下列各组物质中,都是由极性键构成的非极性分子的是
| A.CH4和Br2 | B.PH3和H2O | C.NF3和CCl4 | D.BeCl2和BF3 |
您最近一年使用:0次
名校
8 . 下列反应的离子方程式表述正确的是
A.金属钠投入 溶液中: 溶液中: |
B.氯化铝溶液与过量浓氨水混合: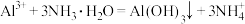 |
C.向NaHSO3溶液中滴 溶液: 溶液: |
D.向酸性高锰酸钾溶液中滴加过氧化氢: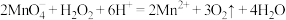 |
您最近一年使用:0次
9 . 我国“祝融号”火星车探测发现火星上存在大量黄钾铁矾[ ]及橄榄石矿物(
]及橄榄石矿物(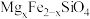 ),下列有关说法正确的是
),下列有关说法正确的是
 ]及橄榄石矿物(
]及橄榄石矿物(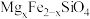 ),下列有关说法正确的是
),下列有关说法正确的是A.原子半径: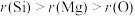 | B.气态氢化物的稳定性: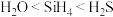 |
| C.在周期表中Fe元素附近,寻找新催化剂 | D. 的简化电子排布式为:[Ar]3d44s2 的简化电子排布式为:[Ar]3d44s2 |
您最近一年使用:0次
名校
解题方法
10 . 下列化学用语描述错误的是
A.中子数为18的硫原子: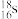 |
B.二氧化碳的空间填充模型: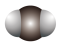 |
C.用电子云轮廓图表示H-H的s-s σ键形成的示意图: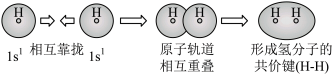 |
D.用电子式表示K2S的形成: |
您最近一年使用:0次



