1 . 硒和碲广泛用于玻璃工业、橡胶和半导体工业.实验室中以碲碱渣(主要含 、
、 ,还有微量的
,还有微量的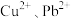 及部分不溶性杂质)为原料分离硒回收碲的工艺流程如图所示.
及部分不溶性杂质)为原料分离硒回收碲的工艺流程如图所示. 与
与 ;
;
② 为两性氧化物;③盐酸“酸浸”后硒以
为两性氧化物;③盐酸“酸浸”后硒以 形式存在.
形式存在.
下列说法错误的是
 、
、 ,还有微量的
,还有微量的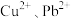 及部分不溶性杂质)为原料分离硒回收碲的工艺流程如图所示.
及部分不溶性杂质)为原料分离硒回收碲的工艺流程如图所示.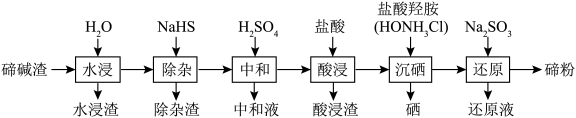
 与
与 ;
;②
 为两性氧化物;③盐酸“酸浸”后硒以
为两性氧化物;③盐酸“酸浸”后硒以 形式存在.
形式存在.下列说法错误的是
| A.流程中涉及的六种工序中,进行物质分离时均需用到烧杯、漏斗和玻璃棒 |
| B.粉碎碲碱渣、延长水浸时间均可以提高硒和碲元素的浸出率 |
C.“中和”时加入过量硫酸,可以提高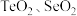 的转化率 的转化率 |
D.“沉硒”时同时生成了 和HCl,则其主要的化学方程式为 和HCl,则其主要的化学方程式为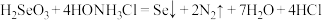 |
您最近一年使用:0次
2 .  是阿伏加德罗常数的值,下列说法错误的是
是阿伏加德罗常数的值,下列说法错误的是
 是阿伏加德罗常数的值,下列说法错误的是
是阿伏加德罗常数的值,下列说法错误的是A.标准状况下,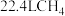 和 和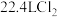 在光照条件下充分反应后体系中的分子总数为 在光照条件下充分反应后体系中的分子总数为 |
B.含有12g碳原子的甲醇与丙三醇的混合物中羟基数目为 |
C.1mol乙醇中含有 杂化的原子数为 杂化的原子数为 |
D.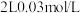 的 的 溶液中所含 溶液中所含 的数目为 的数目为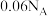 |
您最近一年使用:0次
名校
3 . 砷的化合物可用于半导体领域。一种从酸性高浓度含砷废水[砷主要以亚砷酸( )形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下:
)形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下:
I. ;
;
II.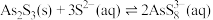 ;
;
III.砷酸( )在酸性条件下有强氧化性,能被
)在酸性条件下有强氧化性,能被 等还原;
等还原;
IV.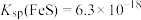 ,
,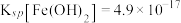 。
。
回答下列问题:
(1)“沉砷”时,亚砷酸转化为 的化学方程式为
的化学方程式为_______ 。
(2)“沉砷”时产生的废气可用_______ 溶液吸收处理(填化学式)。
(3)“NaOH溶液浸取”后,所得“滤渣”的主要成分是_______ (填化学式),“滤渣”中_______  (填“含有”或“不含有”)。
(填“含有”或“不含有”)。
(4)向滤液II中通入氧气进行“氧化脱硫”,反应的离子方程式为_______ 。
(5)“沉砷”过程中FeS不可用过量的 替换,原因是
替换,原因是_______ (从平衡移动的角度解释)。
(6)该流程最后一步用 还原”砷酸,发生反应的化学方程式为
还原”砷酸,发生反应的化学方程式为_______ 。
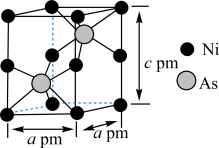
(7)某含砷化合物晶体的晶胞如图所示,As原子位于紧邻Ni原子构成的正三棱柱的体心。晶胞参数为apm、apm、cpm,则该晶体的密度为_______ 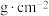 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
 )形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下:
)形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下: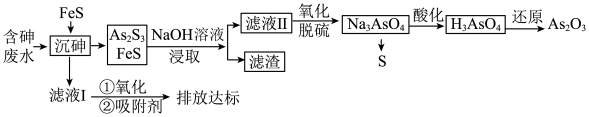
I.
 ;
;II.
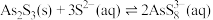 ;
;III.砷酸(
 )在酸性条件下有强氧化性,能被
)在酸性条件下有强氧化性,能被 等还原;
等还原;IV.
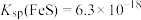 ,
,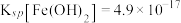 。
。回答下列问题:
(1)“沉砷”时,亚砷酸转化为
 的化学方程式为
的化学方程式为(2)“沉砷”时产生的废气可用
(3)“NaOH溶液浸取”后,所得“滤渣”的主要成分是
 (填“含有”或“不含有”)。
(填“含有”或“不含有”)。(4)向滤液II中通入氧气进行“氧化脱硫”,反应的离子方程式为
(5)“沉砷”过程中FeS不可用过量的
 替换,原因是
替换,原因是(6)该流程最后一步用
 还原”砷酸,发生反应的化学方程式为
还原”砷酸,发生反应的化学方程式为(7)某含砷化合物晶体的晶胞如图所示,As原子位于紧邻Ni原子构成的正三棱柱的体心。晶胞参数为apm、apm、cpm,则该晶体的密度为
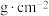 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
名校
4 . 常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C.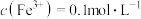 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.水电离出来的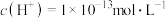 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
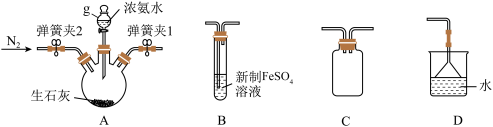
5 . 氢氧化亚铁为白色固体,难溶于水,在空气中极易被氧化为氢氧化铁。回答下列问题;
(一)实验室制备氢氧化亚铁_______________ 。选择上图中的装置制备氢氧化亚铁,连接顺序为__________ (按气流方向从左到右,填写装置标号)。装置C的作用是_______________________ 。
(2)装置B中发生反应的离子方程式为___________________________ 。反应结束后,继续通一段时间的 ,目的是
,目的是______________ 。
(二)探究灰绿色沉淀的成因
反应后将装置B中的固体过滤时,白色沉淀会逐渐转变为灰绿色,实验小组为探究灰绿色沉淀的成因,查阅到以下资料;
① 沉淀具有较强的吸附性;
沉淀具有较强的吸附性;
②若存在固体杂质,会导致 沉淀不够紧密,沉淀与溶液的接触面积会更大。
沉淀不够紧密,沉淀与溶液的接触面积会更大。
甲同学猜测灰绿色可能是 吸附
吸附 引起的,设计并完成了实验1~实验3。
引起的,设计并完成了实验1~实验3。
(3)依据甲同学的猜测,实验1中沉淀无灰绿色的原因是____________________ 。
(4)实验3中立即出现灰绿色浑浊的原因是_______________ 。
(5)根据以上实验探究,若尽可能制得白色 沉淀,需要控制的实验条件除了隔绝氧气外,还有
沉淀,需要控制的实验条件除了隔绝氧气外,还有________________ 。
(一)实验室制备氢氧化亚铁
(2)装置B中发生反应的离子方程式为
 ,目的是
,目的是(二)探究灰绿色沉淀的成因
反应后将装置B中的固体过滤时,白色沉淀会逐渐转变为灰绿色,实验小组为探究灰绿色沉淀的成因,查阅到以下资料;
①
 沉淀具有较强的吸附性;
沉淀具有较强的吸附性;②若存在固体杂质,会导致
 沉淀不够紧密,沉淀与溶液的接触面积会更大。
沉淀不够紧密,沉淀与溶液的接触面积会更大。甲同学猜测灰绿色可能是
 吸附
吸附 引起的,设计并完成了实验1~实验3。
引起的,设计并完成了实验1~实验3。实验 | 操作 | 试剂(均为0.1 | 实验现象 |
1 |
| ⅰ.1滴 ⅱ.4滴NaOH溶液 | 玻璃片夹缝中有白色浑浊 |
2 | ⅰ.4滴 ⅱ.1滴NaOH溶液 | 玻璃片夹缝中有白色浑浊,一段时间后变为灰绿色 | |
3 | ⅰ.2滴 溶液,1滴 溶液,1滴 溶液 溶液ⅱ.2滴NaOH溶液 | 玻璃片夹缝中立即有灰绿色浑浊 |
(3)依据甲同学的猜测,实验1中沉淀无灰绿色的原因是
(4)实验3中立即出现灰绿色浑浊的原因是
(5)根据以上实验探究,若尽可能制得白色
 沉淀,需要控制的实验条件除了隔绝氧气外,还有
沉淀,需要控制的实验条件除了隔绝氧气外,还有
您最近一年使用:0次
7日内更新
|
211次组卷
|
2卷引用:河北省衡水市部分示范性高中2024届高三下学期三模化学试题
名校
解题方法
6 . 水合肼( )及其衍生物产品在许多工业中得到广泛的使用,可用作还原剂、抗氧剂、发泡剂等。一种利用NaClO溶液与氨气反应制备水合肼的装置如图所示。下列说法不正确的是
)及其衍生物产品在许多工业中得到广泛的使用,可用作还原剂、抗氧剂、发泡剂等。一种利用NaClO溶液与氨气反应制备水合肼的装置如图所示。下列说法不正确的是
 )及其衍生物产品在许多工业中得到广泛的使用,可用作还原剂、抗氧剂、发泡剂等。一种利用NaClO溶液与氨气反应制备水合肼的装置如图所示。下列说法不正确的是
)及其衍生物产品在许多工业中得到广泛的使用,可用作还原剂、抗氧剂、发泡剂等。一种利用NaClO溶液与氨气反应制备水合肼的装置如图所示。下列说法不正确的是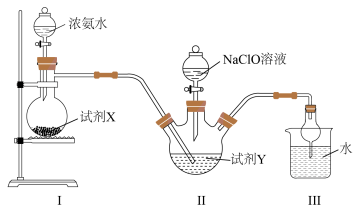
| A.Ⅰ中盛放浓氨水的仪器为分液漏斗 |
| B.试剂X可选择CaO固体 |
| C.为防倒吸,试剂Y可选择苯 |
D.Ⅱ中发生反应的化学方程式为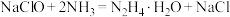 |
您最近一年使用:0次
7日内更新
|
237次组卷
|
2卷引用:河北省衡水市部分示范性高中2024届高三下学期三模化学试题
名校
7 . 硅单质及其化合物应用广泛。请回答下列问题:
(1) 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是(用化学方程式表示)
是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是(用化学方程式表示)___________ 。
(2)硅单质可作为硅半导体材料。三氯甲硅烷( )还原法是当前制备高纯硅的主要方法,生产过程如图:
)还原法是当前制备高纯硅的主要方法,生产过程如图:
石英砂 粗硅
粗硅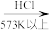
 (粗)
(粗)
 (纯)
(纯) 高纯硅
高纯硅
①写出制粗硅的化学方程式___________ 。
②整个制备过程必须严格控制无水无氧。 遇水剧烈反应生成
遇水剧烈反应生成 、HCl和一种气体单质,写出发生反应的化学方程式
、HCl和一种气体单质,写出发生反应的化学方程式___________ 。
(3)新型陶瓷材料氮化硅( )可应用于原子反应堆,一种制备氮化硅的反应为:
)可应用于原子反应堆,一种制备氮化硅的反应为:
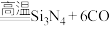 。若生成标准状况下33.6L CO时,反应过程中转移的电子数为
。若生成标准状况下33.6L CO时,反应过程中转移的电子数为___________ 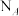 。
。
(1)
 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是(用化学方程式表示)
是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是(用化学方程式表示)(2)硅单质可作为硅半导体材料。三氯甲硅烷(
 )还原法是当前制备高纯硅的主要方法,生产过程如图:
)还原法是当前制备高纯硅的主要方法,生产过程如图:石英砂
 粗硅
粗硅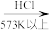
 (粗)
(粗)
 (纯)
(纯) 高纯硅
高纯硅①写出制粗硅的化学方程式
②整个制备过程必须严格控制无水无氧。
 遇水剧烈反应生成
遇水剧烈反应生成 、HCl和一种气体单质,写出发生反应的化学方程式
、HCl和一种气体单质,写出发生反应的化学方程式(3)新型陶瓷材料氮化硅(
 )可应用于原子反应堆,一种制备氮化硅的反应为:
)可应用于原子反应堆,一种制备氮化硅的反应为:
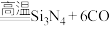 。若生成标准状况下33.6L CO时,反应过程中转移的电子数为
。若生成标准状况下33.6L CO时,反应过程中转移的电子数为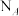 。
。
您最近一年使用:0次
解题方法
8 . 下列混合物分离(或除杂)的方法正确的是
| A.除去Mg粉中的Al粉:加入足量NaOH溶液后,过滤、洗涤 |
| B.除去BaCO3固体中混有的BaSO4:加入过量盐酸后,过滤、洗涤 |
| C.除去NaHCO3溶液中的Na2CO3:加入适量稀盐酸 |
| D.除去Al2O3中的少量Fe2O3:加入过量氢氧化钠溶液,过滤、洗涤 |
您最近一年使用:0次
名校
解题方法
9 . 下列过程中的化学反应,有关离子方程式书写正确的是
A.向 溶液中加入过量氨水: 溶液中加入过量氨水: |
B.过量铁粉加入稀硝酸中: |
C.向Na2SiO3溶液中加入过量CO2: +H2O+CO2=H2SiO3↓+ +H2O+CO2=H2SiO3↓+ |
D.向纯碱溶液中滴加少量盐酸: |
您最近一年使用:0次
2024-04-20更新
|
432次组卷
|
2卷引用:河北省衡水市枣强中学2023-2024学年高一下学期第二次调研考试化学试题
解题方法
10 . 下列对应离子方程式书写正确的是
A.向酸性高锰酸钾溶液中加双氧水: |
B.向硫代硫酸钠溶液中滴加稀硝酸: |
C.向 溶液中滴加盐酸,有气泡产生: 溶液中滴加盐酸,有气泡产生: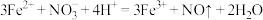 |
D.已知酸性强弱顺序: ,则向NaCN溶液中通入少量 ,则向NaCN溶液中通入少量 : : |
您最近一年使用:0次

 )
)