解题方法
1 . 三氯化铬( )是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。某化学小组用
)是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。某化学小组用 和
和 (沸点76.8℃)在高温下制备无水
(沸点76.8℃)在高温下制备无水 ,实验装置如图所示。
,实验装置如图所示。

已知: 气体有毒,遇水发生水解产生两种酸性气体。
气体有毒,遇水发生水解产生两种酸性气体。
回答下列问题:
(1)实验装置合理的连接顺序为a→i→j→_______ (填仪器接口字母标号,部分仪器可重复使用)。
(2)仪器M中发生反应的化学方程式为_________ 。在实验过程中需要持续通入 ,其作用是
,其作用是___________ 。
(3)从安全的角度考虑,整套装置的不足是___________ 。
(4)Cr(III)的存在形态的物质的量分数随溶液pH的分布如图所示。

请补充完整由 溶液制备纯净的
溶液制备纯净的 的实验方案:取适量
的实验方案:取适量 溶液,
溶液,___________ ;充分反应后过滤,用蒸馏水洗涤沉淀,___________ ,则证明沉淀已洗涤干净;低温烘干沉淀,得到 晶体。
晶体。
(5)铬、钙、氧可形成一种具有特殊导电性的复合氧化物,其晶胞结构如图甲所示。

①该化合物的化学式为___________ 。
②请在图乙中画出该晶胞沿z轴方向的投影图___________ 。
③氧离子与钙离子的最近距离为a pm,阿伏加德罗常数为 ,则该复合氧化物晶体的密度为
,则该复合氧化物晶体的密度为___________ g⋅cm-3(列出计算式)。
 )是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。某化学小组用
)是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。某化学小组用 和
和 (沸点76.8℃)在高温下制备无水
(沸点76.8℃)在高温下制备无水 ,实验装置如图所示。
,实验装置如图所示。
已知:
 气体有毒,遇水发生水解产生两种酸性气体。
气体有毒,遇水发生水解产生两种酸性气体。回答下列问题:
(1)实验装置合理的连接顺序为a→i→j→
(2)仪器M中发生反应的化学方程式为
 ,其作用是
,其作用是(3)从安全的角度考虑,整套装置的不足是
(4)Cr(III)的存在形态的物质的量分数随溶液pH的分布如图所示。

请补充完整由
 溶液制备纯净的
溶液制备纯净的 的实验方案:取适量
的实验方案:取适量 溶液,
溶液, 晶体。
晶体。(5)铬、钙、氧可形成一种具有特殊导电性的复合氧化物,其晶胞结构如图甲所示。

①该化合物的化学式为
②请在图乙中画出该晶胞沿z轴方向的投影图
③氧离子与钙离子的最近距离为a pm,阿伏加德罗常数为
 ,则该复合氧化物晶体的密度为
,则该复合氧化物晶体的密度为
您最近一年使用:0次
2 . 硫化钠在造纸工业中用作纸张的蒸煮剂,在制药工业中用于生产解热药,还可用于制备硫代硫酸钠、多硫化钠等。久置的 固体会潮解、变质、颜色变黄。某实验小组为探究
固体会潮解、变质、颜色变黄。某实验小组为探究 固体在空气中变质后的固体成分进行了如下实验。下列说法正确的是
固体在空气中变质后的固体成分进行了如下实验。下列说法正确的是
已知:硫化钠溶液能溶解单质硫,生成多硫化钠( )。。多硫化物的溶液颜色通常为黄色。
)。。多硫化物的溶液颜色通常为黄色。 与酸反应生成S和
与酸反应生成S和 。
。
 固体会潮解、变质、颜色变黄。某实验小组为探究
固体会潮解、变质、颜色变黄。某实验小组为探究 固体在空气中变质后的固体成分进行了如下实验。下列说法正确的是
固体在空气中变质后的固体成分进行了如下实验。下列说法正确的是| 实验步骤 | 实验操作 | 实验现象 | |
| 操作I | 取适量久置于空气中的 固体,分为两份 固体,分为两份 | ①一份加入 溶解 溶解 | 搅拌后,固体表面的少量淡黄色固体消失 |
| ②另一份加水溶解 | 搅拌后,固体完全溶解,得到略带黄色的溶液。取略带黄色的溶液,滴加稀硫酸,产生淡黄色浑浊M | ||
| 操作II | 向②中固体溶解得到的略带黄色的溶液中加入过量的 溶液 溶液 | 得到灰黑色悬浊液 | |
| 操作III | 将灰黑色悬浊液离心分离 | 离心管底部出现深褐色沉淀,溶液中出现淡黄色浑浊 | |
| 操作IV | 向上述离心分离获得的溶液中加入足量的氯化钡溶液 | 产生大量白色沉淀 | |
| 操作V | 过滤,用无水乙醇洗涤;然后加入稀盐酸,将产生的气体通入少量酸性高锰酸钾溶液中 | 固体部分溶解,酸性高锰酸钾溶液褪色 | |
 )。。多硫化物的溶液颜色通常为黄色。
)。。多硫化物的溶液颜色通常为黄色。 与酸反应生成S和
与酸反应生成S和 。
。| A.①中黄色固体和②中黄色溶液的化学成分相同 |
B.②中现象淡黄色浑浊M不一定是 与稀硫酸反应产生 与稀硫酸反应产生 |
C.操作II中发生反应的离子方程式为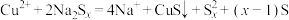 |
| D.实验室可用稀硝酸和硫化亚铁反应制备硫化氢 |
您最近一年使用:0次
解题方法
3 . 次磷酸钠( )广泛应用于化学镀镍,在生产
)广泛应用于化学镀镍,在生产 的过程中会产生大量废渣[主要含
的过程中会产生大量废渣[主要含 和
和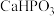 ,还含有少量
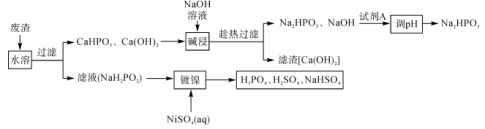
,还含有少量 ],一种回收次磷酸钠以及化学镀镍过程的工艺流程如图所示。
],一种回收次磷酸钠以及化学镀镍过程的工艺流程如图所示。
已知:①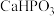 和
和 的
的 分别为
分别为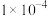 和
和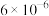 ;
;
② 为一元弱酸,
为一元弱酸, 为二元弱酸;
为二元弱酸;
③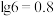 。
。
下列叙述错误的是
 )广泛应用于化学镀镍,在生产
)广泛应用于化学镀镍,在生产 的过程中会产生大量废渣[主要含
的过程中会产生大量废渣[主要含 和
和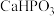 ,还含有少量
,还含有少量 ],一种回收次磷酸钠以及化学镀镍过程的工艺流程如图所示。
],一种回收次磷酸钠以及化学镀镍过程的工艺流程如图所示。
已知:①
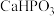 和
和 的
的 分别为
分别为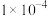 和
和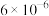 ;
;②
 为一元弱酸,
为一元弱酸, 为二元弱酸;
为二元弱酸;③
 。
。下列叙述错误的是
A.“趁热过滤”的目的是防止滤渣中的 溶解 溶解 |
B.“趁热过滤”后,要使滤液中 的浓度不小于0.01 mol⋅L 的浓度不小于0.01 mol⋅L ,则滤液的pH应不低于11.6 ,则滤液的pH应不低于11.6 |
C.试剂A可以是 , , 是正盐 是正盐 |
D.“镀镍”时,发生反应的离子方程式为 |
您最近一年使用:0次
名校
解题方法
4 . 工业生产中利用方铅矿(主要成分为 ,含有
,含有 等杂质)制备
等杂质)制备 晶体的工艺流程如图:
晶体的工艺流程如图:

已知: ;
;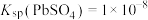 ,
,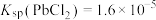 。
。
下列说法错误的是
 ,含有
,含有 等杂质)制备
等杂质)制备 晶体的工艺流程如图:
晶体的工艺流程如图:
已知:
 ;
;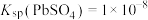 ,
,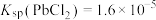 。
。下列说法错误的是
A.浸取时发生反应: |
B.物质M为 ,试剂 ,试剂 为 为 ,滤液a一定能循环使用 ,滤液a一定能循环使用 |
C.由该工艺流程可知, 反应吸热 反应吸热 |
D.“沉淀转化”过程达平衡时,溶液中 |
您最近一年使用:0次
解题方法
5 . 金属钒主要用于冶炼特种钢,被誉为“合金的维生素”。人们在化工实践中,以富钒炉渣(其中的钒以FeO•V2O3、V2O5等形式存在,还有少量的SiO2、Al2O3等)为原料提取金属钒的工艺流程如图所示:

提示:①钒有多种价态,其中+5价最稳定;
②V2O5在碱性条件下可转化为VO 。
。
(1)可加快“高温氧化”速率的措施有______ (填一条)。
(2)“气体X”和“气体Y”的化学式分别为______ 、______ 。
(3)“沉硅、沉铝”中得到含铝沉淀的离子方程式为_______ 。
(4)写出“高温氧化”过程中发生反应的化学方程式______ 。
(5)写出“热解”时的化学方程式_______ 。
(6)在“高温还原”反应中,氧化钙最终转化为______ (写化学式)。
(7)已知:25℃时,NH3•H2O的电离平衡常数Kb=1.8×10-5,H2CO3的电离平衡常数Ka1=4.3×10-7,Ka2=5.6×10-11,判断NH4HCO3溶液呈______ (填“酸性”“碱性”或“中性”)。

提示:①钒有多种价态,其中+5价最稳定;
②V2O5在碱性条件下可转化为VO
 。
。(1)可加快“高温氧化”速率的措施有
(2)“气体X”和“气体Y”的化学式分别为
(3)“沉硅、沉铝”中得到含铝沉淀的离子方程式为
(4)写出“高温氧化”过程中发生反应的化学方程式
(5)写出“热解”时的化学方程式
(6)在“高温还原”反应中,氧化钙最终转化为
(7)已知:25℃时,NH3•H2O的电离平衡常数Kb=1.8×10-5,H2CO3的电离平衡常数Ka1=4.3×10-7,Ka2=5.6×10-11,判断NH4HCO3溶液呈
您最近一年使用:0次
名校
6 . 以含锌废液(主要成分为 ,含少量的
,含少量的 、
、 )为原料制备
)为原料制备 的实验流程如下。
的实验流程如下。 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是
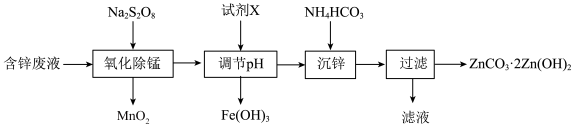
 ,含少量的
,含少量的 、
、 )为原料制备
)为原料制备 的实验流程如下。
的实验流程如下。 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是
A. 过二硫酸钠 过二硫酸钠 中含有过氧键( 中含有过氧键( )数目为 )数目为 |
B.“氧化除锰”后的溶液中一定存在: 、 、 、 、 、 、 |
C.“调节pH”时试剂X可以选用 、 、 、 、 等物质 等物质 |
D.“氧化除锰”过程中生成 的离子方程式: 的离子方程式: |
您最近一年使用:0次
2023-05-05更新
|
428次组卷
|
2卷引用:湖南省长沙市雅礼中学2023届高三模拟考试(一)化学试题
解题方法
7 . 实验室模拟工业制备BaCl2•2H2O的一种工艺流程如图所示,已知常温下CaS的溶解度为0.2g/L,CaCl2的溶解度较大,且随温度变化不大。下列说法错误的是
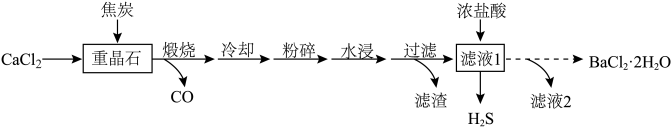
A.“煅烧”过程中发生的反应为BaSO4+CaCl2+4C BaCl2+CaS+4CO↑ BaCl2+CaS+4CO↑ |
| B.“粉碎”时可在瓷坩埚中进行 |
| C.滤渣中除了CaS,还可能含有未反应完的BaSO4 |
| D.滤液1通过蒸发浓缩、冷却结晶、过滤洗涤等操作可得BaCl2•2H2O |
您最近一年使用:0次
8 . 下列反应方程式书写错误的是
| A.少许Al2S3固体溶于水中,有白色沉淀产生:Al2S3+6H2O=2Al(OH)3↓+3H2S↑ |
B.工业上用Na2CO3溶液吸收含NO2尾气:CO +2NO2=NO +2NO2=NO +NO +NO +CO2 +CO2 |
C.乙醛与银氨溶液反应:  |
D.KClO3溶液与过量NaHSO3溶液反应:2ClO +5HSO +5HSO =Cl2+5SO =Cl2+5SO +3H++H2O +3H++H2O |
您最近一年使用:0次
9 . 二草酸合铜(Ⅱ)酸钾晶体 是一种重要的化工原料,微溶于冷水,易溶于热水。某种制备方法如下:
是一种重要的化工原料,微溶于冷水,易溶于热水。某种制备方法如下:

(1)“操作Ⅰ”包括加热煮沸、冷却、过滤、洗涤、检验,加热煮沸的目的是___________ ;检验 是否洗涤干净的方法为
是否洗涤干净的方法为___________ 。
(2) 需在“操作Ⅱ”加入,为防止加入时反应过于剧烈而引起喷溅,应采取的方法为
需在“操作Ⅱ”加入,为防止加入时反应过于剧烈而引起喷溅,应采取的方法为___________ 。
(3)“操作Ⅲ”为水浴加热(80~85℃),该反应的方程式为___________ 。
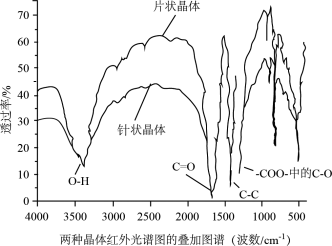
(4)“系列操作”后,得到二草酸合铜酸钾晶体。溶液的浓缩程度及冷却速度对配合物晶型有影响。急速冷却得到灰蓝色针状晶体,常温缓慢冷却得到深蓝色片状晶体,两种晶体的红外光谱图如图,由图可知,两种晶型的晶体成分均为二草酸合铜酸钾晶体,依据是___________ 。
(5)探究二草酸合铜酸钾晶体 热分解产物的装置如下:
热分解产物的装置如下:

该实验观察到的现象:B、G澄清石灰水变浑浊,但D无明显现象;F中固体变为红色;实验结束后,取A中残留物加水溶解、过滤、洗涤,得到砖红色沉淀和无色溶液,通过实验证明无色溶液中含有 和
和 ,砖红色沉淀加入稀硫酸,产生蓝色溶液且有红色固体生成。据此写出二草酸合铜晶体受热分解的化学方程式
,砖红色沉淀加入稀硫酸,产生蓝色溶液且有红色固体生成。据此写出二草酸合铜晶体受热分解的化学方程式___________ 。若A中放入提纯后的晶体35.4g,完全分解后,充分反应,测得F中固体质量减少2.4g,则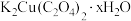 中
中
___________ 。
 是一种重要的化工原料,微溶于冷水,易溶于热水。某种制备方法如下:
是一种重要的化工原料,微溶于冷水,易溶于热水。某种制备方法如下:
(1)“操作Ⅰ”包括加热煮沸、冷却、过滤、洗涤、检验,加热煮沸的目的是
 是否洗涤干净的方法为
是否洗涤干净的方法为(2)
 需在“操作Ⅱ”加入,为防止加入时反应过于剧烈而引起喷溅,应采取的方法为
需在“操作Ⅱ”加入,为防止加入时反应过于剧烈而引起喷溅,应采取的方法为(3)“操作Ⅲ”为水浴加热(80~85℃),该反应的方程式为
(4)“系列操作”后,得到二草酸合铜酸钾晶体。溶液的浓缩程度及冷却速度对配合物晶型有影响。急速冷却得到灰蓝色针状晶体,常温缓慢冷却得到深蓝色片状晶体,两种晶体的红外光谱图如图,由图可知,两种晶型的晶体成分均为二草酸合铜酸钾晶体,依据是

(5)探究二草酸合铜酸钾晶体
 热分解产物的装置如下:
热分解产物的装置如下:
该实验观察到的现象:B、G澄清石灰水变浑浊,但D无明显现象;F中固体变为红色;实验结束后,取A中残留物加水溶解、过滤、洗涤,得到砖红色沉淀和无色溶液,通过实验证明无色溶液中含有
 和
和 ,砖红色沉淀加入稀硫酸,产生蓝色溶液且有红色固体生成。据此写出二草酸合铜晶体受热分解的化学方程式
,砖红色沉淀加入稀硫酸,产生蓝色溶液且有红色固体生成。据此写出二草酸合铜晶体受热分解的化学方程式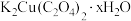 中
中
您最近一年使用:0次
名校
10 . 某小组探究 与
与 在不同条件下的反应,实验操作和现象记录如下:
在不同条件下的反应,实验操作和现象记录如下:
下列说法错误的是
 与
与 在不同条件下的反应,实验操作和现象记录如下:
在不同条件下的反应,实验操作和现象记录如下:| 实验 | 操作 | 现象 |
| Ⅰ | 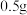  、 、 30% 30% 溶液混合 溶液混合 | 10h后,铜片表面附着黑色固体 |
| Ⅱ | 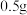  、 、 30% 30% 溶液、 溶液、  氨水混合 氨水混合 | 立即产生大量气泡,溶液变为浅蓝色,铜表面光洁 |
| Ⅲ | 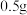  、 、 30% 30% 溶液、 溶液、  氨水和 氨水和  固体混合 固体混合 | 立即产生大量气泡,溶液蓝色较深,铜片依然保持光亮 |
A.Ⅰ中 与 与 可以缓慢反应,可能生成 可以缓慢反应,可能生成 |
B.Ⅱ中可能发生的反应为 |
C.增大 , , 的氧化性增强 的氧化性增强 |
D.增大 有利于 有利于 的生成 的生成 |
您最近一年使用:0次
2023-04-23更新
|
506次组卷
|
2卷引用:湖南省怀化市2023届高三下学期二模仿真考试化学试题



