1 . 甲学生对 与
与 和KSCN混合溶液的反应进行实验探究。
和KSCN混合溶液的反应进行实验探究。
(1)B中反应的离子方程式是____________________ 。
(2)A中溶液变红的原因是(用离子方程式回答)①___________ ;②___________
(3)为了探究现象Ⅱ的原因,甲同学进行如下实验:
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在______ 。
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。
甲同学的实验证明产生现象Ⅱ的原因是 与Cl2发生了反应。
与Cl2发生了反应。
(4)甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究。
资料显示:SCN-的电子式为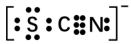 。
。
①甲同学认为SCN-中碳元素没有被氧化,理由是___________ 。
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中的___________ 元素被氧化。
 与
与 和KSCN混合溶液的反应进行实验探究。
和KSCN混合溶液的反应进行实验探究。| 操作 | 现象 |
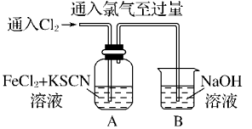 | Ⅰ.A中溶液变红 Ⅱ.稍后,溶液由红色变为黄色 |
(2)A中溶液变红的原因是(用离子方程式回答)①
(3)为了探究现象Ⅱ的原因,甲同学进行如下实验:
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。
甲同学的实验证明产生现象Ⅱ的原因是
 与Cl2发生了反应。
与Cl2发生了反应。(4)甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究。
资料显示:SCN-的电子式为
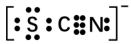 。
。①甲同学认为SCN-中碳元素没有被氧化,理由是
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中的
您最近一年使用:0次
2 . 长期存放的亚硫酸钠可能会被空气中的氧气氧化。某化学兴趣小组通过实验来测定某无水亚硫酸钠试剂的质量分数,设计了如图所示实验装置:
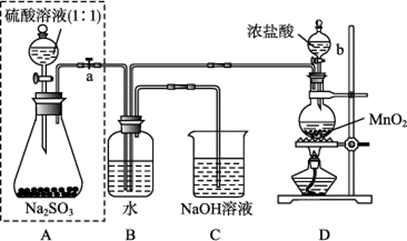
请回答下面的问题:
(1)若将虚线框内的分液漏斗换成长颈漏斗,则应该怎样检查虚线框内装置的气密性?___________ 。
(2)D装置中反应的化学方程式为:___________ ,其中氧化剂是___________ 。B装置中反应的离子方程式为___________ 。
(3)C中NaOH溶液的作用是___________ 。
(4)称量agNa2SO3样品放入锥形瓶中进行实验,向B装置反应后的溶液中加入足量的BaCl2溶液充分反应,过滤、洗涤、干燥,得白色沉淀bg,原样品中Na2SO3的质量分数为___________ 。

请回答下面的问题:
(1)若将虚线框内的分液漏斗换成长颈漏斗,则应该怎样检查虚线框内装置的气密性?
(2)D装置中反应的化学方程式为:
(3)C中NaOH溶液的作用是
(4)称量agNa2SO3样品放入锥形瓶中进行实验,向B装置反应后的溶液中加入足量的BaCl2溶液充分反应,过滤、洗涤、干燥,得白色沉淀bg,原样品中Na2SO3的质量分数为
您最近一年使用:0次
名校
3 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。
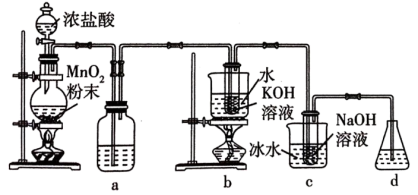
回答下列问题:
(1)盛放 粉末的仪器名称是
粉末的仪器名称是___________ ,a中的试剂为___________ 。
(2)b中采用的加热方式是___________ ,c中化学反应的离子方程式是___________ 。
(3)d的作用是___________ ,可选用试剂___________ (填标号)。
A. B.
B. C.
C. D.
D.
(4)取少量 和
和 溶液分别置于1号和2号试管中,滴加中性
溶液分别置于1号和2号试管中,滴加中性 溶液:
溶液:
1号试管溶液颜色不变。
2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显
层显___________ 色。可知该条件下 的氧化能力
的氧化能力___________  (填“大于”或“小于”)。
(填“大于”或“小于”)。
 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。
回答下列问题:
(1)盛放
 粉末的仪器名称是
粉末的仪器名称是(2)b中采用的加热方式是
(3)d的作用是
A.
 B.
B. C.
C. D.
D.
(4)取少量
 和
和 溶液分别置于1号和2号试管中,滴加中性
溶液分别置于1号和2号试管中,滴加中性 溶液:
溶液:1号试管溶液颜色不变。
2号试管溶液变为棕色,加入
 振荡,静置后
振荡,静置后 层显
层显 的氧化能力
的氧化能力 (填“大于”或“小于”)。
(填“大于”或“小于”)。
您最近一年使用:0次
2021-10-13更新
|
287次组卷
|
3卷引用:海南省华中师范大学琼中附属中学2022届高三第二次月考化学试题
名校
解题方法
4 . 二氯异氰尿酸钠[(CNO)3Cl2Na]是常用的杀菌消毒剂,常温下为白色固体,难溶于冷水。某同学利用高浓度的NaClO溶液和(CNO)3H3固体,在10℃时反应制备二氯异氰尿酸钠,实验装置如下图所示(部分夹持装置略)。
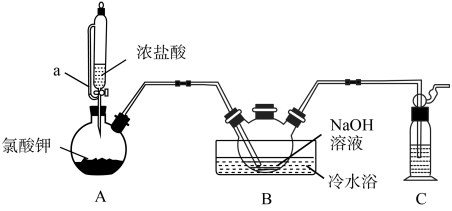
已知:2NaClO + (CNO)3H3 = (CNO)3Cl2Na + NaOH + H2O
回答下列问题:
(1)仪器a的名称为恒压滴液漏斗,与分液漏斗相比其优点是___________ 。
(2)待装置B中出现___________ 现象时,可由三颈烧瓶上口加入(CNO)3H3固体;反应过程中仍需不断通入 Cl2的理由是___________ 。
(3)反应结束后,装置B中的浊液经过滤、___________ 、干燥得粗产品。上述装置存在一处缺陷会导致装置B中NaOH利用率降低,改进的方法是___________ 。
(4)通过下列实验测定二氯异氰尿酸钠样品中有效氯的含量。
反应原理: [(CNO)3Cl2]-+ H+ +2H2O = (CNO)3H3 + 2HClO, HClO + 2I- + H+ = I2 + Cl-+ H2O, I2 + 2S2O = S4O
= S4O + 2I-
+ 2I-
实验步骤:准确称取m g样品,用容量瓶配成250 mL溶液;取25.00 mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,充分反应后,用 c mol/L Na2S2O3标准溶液滴定至溶液呈微黄色。加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液平均为 V mL。
①滴定终点现象为___________ 。
②该样品的有效氯含量表达式为___________ 。(该样品的有效氯=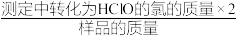 ×100%)
×100%)

已知:2NaClO + (CNO)3H3 = (CNO)3Cl2Na + NaOH + H2O
回答下列问题:
(1)仪器a的名称为恒压滴液漏斗,与分液漏斗相比其优点是
(2)待装置B中出现
(3)反应结束后,装置B中的浊液经过滤、
(4)通过下列实验测定二氯异氰尿酸钠样品中有效氯的含量。
反应原理: [(CNO)3Cl2]-+ H+ +2H2O = (CNO)3H3 + 2HClO, HClO + 2I- + H+ = I2 + Cl-+ H2O, I2 + 2S2O
 = S4O
= S4O + 2I-
+ 2I-实验步骤:准确称取m g样品,用容量瓶配成250 mL溶液;取25.00 mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,充分反应后,用 c mol/L Na2S2O3标准溶液滴定至溶液呈微黄色。加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液平均为 V mL。
①滴定终点现象为
②该样品的有效氯含量表达式为
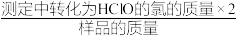 ×100%)
×100%)
您最近一年使用:0次
2021-05-18更新
|
347次组卷
|
2卷引用:海南省海口市2021年高三高考调研测试化学试题
5 . 氯气是一种重要的化工原料。如图为实验室制取氯气的装置。请回答:
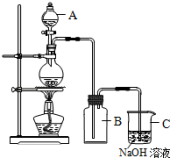
(1)仪器A的名称是___________ 。
(2)当装置B中充满黄绿色气体时,说明氯气收集满了,是因为___________ 。
(3)装置C的作用___________ (只有一项正确,填序号)。
①干燥气体 ②吸收尾气 ③防止倒吸
(4)装置C的烧杯中可以得到以次氯酸钠(NaClO)为有效成分的漂白液,写出反应的化学方程式___________ 。
(5)氯气可以与溴化钠溶液发生反应:2NaBr+Cl2=2NaCl+Br2,在该反应中氯气作___________ 剂(填“氧化”或“还原”)。

(1)仪器A的名称是
(2)当装置B中充满黄绿色气体时,说明氯气收集满了,是因为
(3)装置C的作用
①干燥气体 ②吸收尾气 ③防止倒吸
(4)装置C的烧杯中可以得到以次氯酸钠(NaClO)为有效成分的漂白液,写出反应的化学方程式
(5)氯气可以与溴化钠溶液发生反应:2NaBr+Cl2=2NaCl+Br2,在该反应中氯气作
您最近一年使用:0次
2021-05-07更新
|
76次组卷
|
2卷引用:海南省昌江县部分学校2023届高三联合质检二模化学试题
解题方法
6 . 铁、铝的混合物进行如下实验:
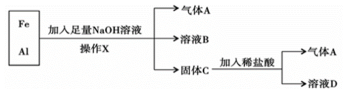
(1)操作X的名称是____ ;
(2)气体A是_____ (填化学式);
(3)A与Cl2混合光照可能发生爆炸,生成___ (填化学式),A在该反应中作为____ (填“氧化剂”或“还原剂”);
(4)溶液B中阴离子除OH-外还有____ (填离子符号),溶液D中存在的金属离子为___ (填离子符号);
(5)加入足量NaOH溶液时发生反应的离子方程式为:____ ;

(1)操作X的名称是
(2)气体A是
(3)A与Cl2混合光照可能发生爆炸,生成
(4)溶液B中阴离子除OH-外还有
(5)加入足量NaOH溶液时发生反应的离子方程式为:
您最近一年使用:0次
7 . 如图为实验室制取和收集纯净干燥的氯气,并进行氯气性质探究的实验装置图。

(1)反应前在___ 中装浓盐酸(填写仪器名称),___ 中装MnO2(填写仪器名称)。
(2)写出制备氯气的化学方程式___ 。
(3)装置A中所装试剂是饱和食盐水,其作用是___ 。
(4)若去掉B装置,C中放一干燥有色布条,请问,布条能否褪色___ (填“能”或“不能”),请说明“能”或“不能”褪色的原因___ 。
(5)装置B中所装的试剂是___ ,其作用是吸收水蒸气。
(6)装置D中所装试剂是___ ,写出反应的离子方程式___ 。

(1)反应前在
(2)写出制备氯气的化学方程式
(3)装置A中所装试剂是饱和食盐水,其作用是
(4)若去掉B装置,C中放一干燥有色布条,请问,布条能否褪色
(5)装置B中所装的试剂是
(6)装置D中所装试剂是
您最近一年使用:0次
解题方法
8 . 如图为物质转化关系,其中甲是一种金属单质,燃烧时,火焰为黄色。A、C、F常温下为气体;其中C为黄绿色,且A与C点燃时产生苍白色火焰,并且在瓶口有白雾出现。F为温室效应气体,乙为厨房中常用的一种盐,热稳定性强,灼烧时火焰为黄色。
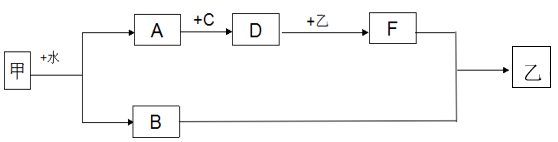
回答下列问题:
(1)写出下列的化学式:A:___ ,B:___ ,D:___ ,F:___ 。
(2)写出甲与水反应的化学方程式:___ 。
(3)写出D与乙反应的化学方程式:___ 。
(4)反应B和F反应的离子方程式:___ 。
(5)写出甲与氧气燃烧的产物与二氧化碳反应的化学方程式___ 。

回答下列问题:
(1)写出下列的化学式:A:
(2)写出甲与水反应的化学方程式:
(3)写出D与乙反应的化学方程式:
(4)反应B和F反应的离子方程式:
(5)写出甲与氧气燃烧的产物与二氧化碳反应的化学方程式
您最近一年使用:0次
9 . 某研究性学习小组欲探究氯气的化学性质,设计的实验装置如图所示。

已知:该装置气密性良好,铁粉放在耐高温托盘内(防止硬质玻璃管炸裂)。
请回答下列问题:
(1)为防止铁粉被空气中的氧气氧化,在加热之前应该进行的操作为___________ 。
(2)实验中,观察到紫色石蕊溶液颜色的变化为___________ 。
(3)实验装置中空试管的作用是___________ 。
(4)烧杯中氢氧化钠溶液的作用是___________ ,此处发生反应的化学方程式为___________ 。
(5)实验进行一段时间后,盛水的试管中液体的颜色为___________ ,说明氯气___________ (填“能”或“不能”)溶于水。

已知:该装置气密性良好,铁粉放在耐高温托盘内(防止硬质玻璃管炸裂)。
请回答下列问题:
(1)为防止铁粉被空气中的氧气氧化,在加热之前应该进行的操作为
(2)实验中,观察到紫色石蕊溶液颜色的变化为
(3)实验装置中空试管的作用是
(4)烧杯中氢氧化钠溶液的作用是
(5)实验进行一段时间后,盛水的试管中液体的颜色为
您最近一年使用:0次
2021-03-01更新
|
144次组卷
|
3卷引用:海南省2020-2021学年高二上学期期末考试化学试题
解题方法
10 . 碱式次氯酸镁[BMH,化学式为Mg2ClO(OH)3·H2O]是一种白色粉末,难溶于水,也是新一代无机抗菌剂。可以Cl2、NaOH及MgCl2为原料制取。
(1)甲组同学拟利用下列装置制备质量分数约为5%的次氯酸钠溶液。
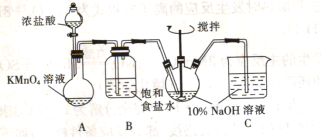
①盛KMnO4溶液的仪器名称为_______ 。
②B装置中饱和食盐水的作用为_______ 。
③已知Cl2和NaOH在较高的温度下反应会生成NaClO3,因此控制反应在0~5℃范围内进行,实验中适宜的措施是_______ 。
(2)乙组同学拟利用甲组同学制得的含NaClO的溶液制取碱式次氯酸镁,步骤如下:
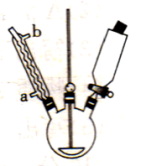
步骤l:往烧瓶中加入氯化镁,开动搅拌器并升温到80℃;
步骤2:逐滴滴入NaClO的溶液;
步骤3:调节溶液pH=10,回流反应4h;
步骤4:过滤,烘干。
①图中回流时,水从接口_______ (填“a”或“b”)进入。
②过滤时,需用到的玻璃仪器除烧杯外,还需_______ 。
③写出MgCl2、NaOH、Cl2反应制取Mg2ClO(OH)3·H2O的化学方程式:_______
(1)甲组同学拟利用下列装置制备质量分数约为5%的次氯酸钠溶液。

①盛KMnO4溶液的仪器名称为
②B装置中饱和食盐水的作用为
③已知Cl2和NaOH在较高的温度下反应会生成NaClO3,因此控制反应在0~5℃范围内进行,实验中适宜的措施是
(2)乙组同学拟利用甲组同学制得的含NaClO的溶液制取碱式次氯酸镁,步骤如下:

步骤l:往烧瓶中加入氯化镁,开动搅拌器并升温到80℃;
步骤2:逐滴滴入NaClO的溶液;
步骤3:调节溶液pH=10,回流反应4h;
步骤4:过滤,烘干。
①图中回流时,水从接口
②过滤时,需用到的玻璃仪器除烧杯外,还需
③写出MgCl2、NaOH、Cl2反应制取Mg2ClO(OH)3·H2O的化学方程式:
您最近一年使用:0次



