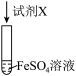
1 . 验证FeSO4的性质,进行如下实验。
实验序号 | 验证性质 | 实验装置 | 试剂X | 实验现象 |
① | 能与某些盐反应 |
| BaCl2溶液 | 产生白色沉淀 |
② | 能与碱反应 | NaOH溶液 | 产生白色絮状沉淀,迅速变为灰绿色,一段时间后变成红褐色 | |
③ | 具有氧化性 | 锌粒 | 锌粒表面变黑,溶液浅绿色褪去 | |
④ | 具有还原性 | KSCN溶液氯水 | 滴加KSCN溶液,无明显现象,再滴加氯水,溶液变为红色 |
下列关于该实验的说法不正确的是
A.①中产生白色沉淀的原因: |
B.②中沉淀变成红褐色的原因: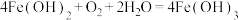 |
| C.③中用镁条(已打磨)替换锌粒,也可以证明FeSO4具有氧化性 |
| D.④中调换试剂的加入顺序,也可以证明FeSO4具有还原性 |

| A.可存在f→d→e的转化 |
B.高温下a与 反应制备c 反应制备c |
| C.KSCN溶液可用于鉴别f和g |
| D.a在g溶液中反应生成f |
3 . 有关铁的化合物的说法中,正确的是
A. 是一种黑色固体,不稳定,在空气中易被氧化转变为红褐色 是一种黑色固体,不稳定,在空气中易被氧化转变为红褐色 |
B. 与 与 产生血红色沉淀 产生血红色沉淀 |
C. 、 、 都可以由化合反应制得 都可以由化合反应制得 |
D.向煮沸的氢氧化钠溶液中逐滴加入5滴 饱和溶液,继续煮沸至液体呈红褐色,停止加热,制得 饱和溶液,继续煮沸至液体呈红褐色,停止加热,制得 胶体 胶体 |
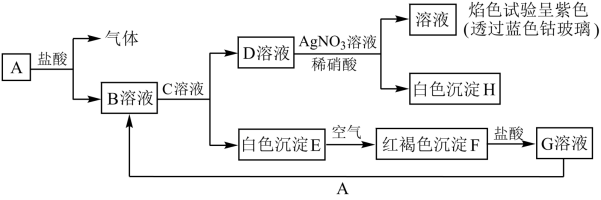
(1)写出B和D 的化学式:B
(2)写出E
 F的化学方程式:
F的化学方程式:(3)向G溶液中加入A,写出反应的离子方程式
(4)设计实验检验A与盐酸反应后溶液中存在的阳离子
5 . 硫酸亚铁铵是一种重要的化工原料,用途广泛,其晶体为浅绿色,俗名摩尔盐,化学式为 。某小组设计如下实验进行探究:
。某小组设计如下实验进行探究:
I.制备
(1)向新制的
 溶液中加入一定质量的
溶液中加入一定质量的 固体,在
固体,在 条件下溶解后,趁热倒入50mL乙醇中,析出晶体。实验时所采用的加热方式是
条件下溶解后,趁热倒入50mL乙醇中,析出晶体。实验时所采用的加热方式是Ⅱ.i.测定 含量(蒸馏法,装置如图)
含量(蒸馏法,装置如图)

①称取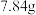 晶体加水溶解后,将溶液注入三颈烧瓶中;
晶体加水溶解后,将溶液注入三颈烧瓶中;
②准确量取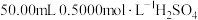 溶液于锥形瓶中;
溶液于锥形瓶中;
③向三颈烧瓶中加入足量NaOH溶液,通入氮气,加热,蒸氨结束后取下锥形瓶,用蒸馏水冲洗冷凝管内通道2~3次,将洗涤液注入锥形瓶中;
④用 的NaOH标准溶液滴定锥形瓶中过量的硫酸,以酚酞为指示剂,滴定终点时消耗
的NaOH标准溶液滴定锥形瓶中过量的硫酸,以酚酞为指示剂,滴定终点时消耗 NaOH标准溶液。
NaOH标准溶液。
(2)步骤②中,量取
 溶液的仪器是下图所示仪器中的
溶液的仪器是下图所示仪器中的
(3)步骤③中,三颈烧瓶中可能发生的氧化还原反应的化学方程式是
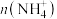 的值将
的值将(4)步骤④中达到滴定终点的现象是
ii.测定 含量(重量分析法)
含量(重量分析法)
⑤另取一份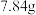 晶体于烧杯,加水溶解,边搅拌边加入过量的
晶体于烧杯,加水溶解,边搅拌边加入过量的 溶液;
溶液;
⑥抽滤,用稀硫酸洗涤沉淀3次;将所得沉淀充分干燥,称量,得沉淀质量为 。
。
(5)步骤⑤中,判断
 溶液已过量的实验操作和现象是
溶液已过量的实验操作和现象是(6)结合实验I和Ⅱ,通过计算得出该晶体的化学式为
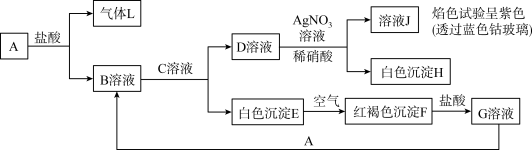
回答下列问题:
(1)C是
(2)E→F的化学方程式:
(3)在氢碘酸溶液中加入少量F,写出离子方程式:
(4)在B溶液中加入(NH4)2C2O4溶液,产生固体MC2O4·2H2O(M是A物质对应的元素)。该固体在空气中加热分解,得到分解产物的热重曲线如图所示。

①a点固体的物质的量为
②b→c的化学方程式为
| A.CuCl2 | B.FeCl2 | C.Fe(OH)2 | D.Fe(OH)3 |
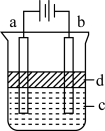
(1)a电极的材料应为
(2)电解液c可以是___________(填字母)。
| A.纯水 | B.NaCl溶液 | C.NaOH溶液 | D.CuCl2溶液 |
(3)d为苯,其作用是
(4)如果没有d,可以观察的现象变化为

| A.②③④⑤ | B.①②④⑤ | C.①③④⑤ | D.①②③⑤ |

(1)操作X是
(2)A与Cl2混合光照可能发生爆炸,A在该反应中作
(3)合金中加入足量NaOH溶液发生反应的离子方程式
(4)加入稀盐酸发生反应的离子方程式为
(5)向溶液D中加入NaOH溶液,观察到产生的现象是