2023高三·全国·专题练习
1 . 某小组同学取含有少量CuO杂质的Cu2O样品进行如下实验,以测定氧化亚铜的纯度。
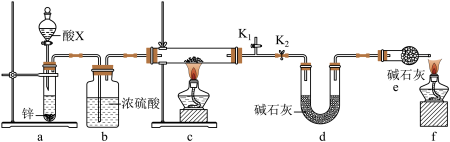
(1)装置a中所加的酸X是___________ (填化学式)。
(2)通过测定下列物理量,能达到实验目的的是___________(填字母)。
(3)熄灭酒精灯之后,仍需通一段时间H2至硬质玻璃管冷却,原因是___________ 。

(1)装置a中所加的酸X是
(2)通过测定下列物理量,能达到实验目的的是___________(填字母)。
| A.反应前后装置a的质量 |
| B.充分反应后装置c所得固体的质量 |
| C.反应前后装置d的质量 |
| D.反应前后装置e的质量 |
(3)熄灭酒精灯之后,仍需通一段时间H2至硬质玻璃管冷却,原因是
您最近半年使用:0次
解题方法
2 . 实验室制取NO和 固体,下列装置能达到实验目的的是
固体,下列装置能达到实验目的的是
 固体,下列装置能达到实验目的的是
固体,下列装置能达到实验目的的是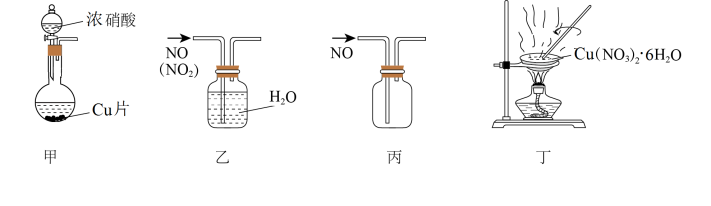
| A.用装置甲制取NO气体 | B.用装置乙除去NO中少量的 |
| C.用装置丙收集NO气体 | D.用装置丁灼烧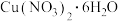 得到 得到 |
您最近半年使用:0次
3 . 铜器久置,表面会生成一层绿色固体,为了解铜在空气中的腐蚀情况、某化学兴趣小组收集家中铜器表面的绿色固体进行探究。查阅相关资料后,猜想该绿色物质可能是铜的碳酸盐。该小组同学利用下图装置进行实验(部分夹持仪器略)。
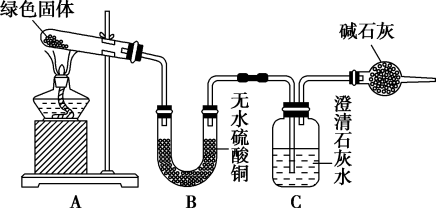
①对试管内的绿色固体进行加热,至完全分解,观察到A装置中绿色固体逐渐变成黑色。B装置中无水硫酸铜变成蓝色,C装置中澄清石灰水变浑浊。
②取少量加热后生成的黑色固体于试管中,加入稀硫酸,观察到黑色固体逐渐溶解,溶液变成蓝色。
③取少量上述蓝色溶液于试管中,浸入一根洁净的铁丝。观察到铁丝表面有红色物质析出。
请回答下列问题:
(1)实验前,应检查装置的气密性,检查该装置气密性的方法是_______ 。
(2)加热后试管中剩余的黑色物质是_______ 。
(3)假设该绿色物质是一种纯净物,则其化学式可能是_______ (填化学式),加热分解的化学方程式为_______ 。
(4)上述实验步骤③中的反应的离子方程式为_______ 。
(5)实验装置最后干燥管的作用是_______ 。
(6)如果将B、C两装置对调,能否达到实验目的_______ (填“能”或“不能”),为什么?_______ 。

①对试管内的绿色固体进行加热,至完全分解,观察到A装置中绿色固体逐渐变成黑色。B装置中无水硫酸铜变成蓝色,C装置中澄清石灰水变浑浊。
②取少量加热后生成的黑色固体于试管中,加入稀硫酸,观察到黑色固体逐渐溶解,溶液变成蓝色。
③取少量上述蓝色溶液于试管中,浸入一根洁净的铁丝。观察到铁丝表面有红色物质析出。
请回答下列问题:
(1)实验前,应检查装置的气密性,检查该装置气密性的方法是
(2)加热后试管中剩余的黑色物质是
(3)假设该绿色物质是一种纯净物,则其化学式可能是
(4)上述实验步骤③中的反应的离子方程式为
(5)实验装置最后干燥管的作用是
(6)如果将B、C两装置对调,能否达到实验目的
您最近半年使用:0次
4 . 已知:①Cu2O在酸性条件下能迅速发生反应:Cu2O+2H+=Cu+Cu2++H2O;②氮的氧化物能与红热的铜反应。某小组设计实验探究NO和Cu反应的氧化产物,装置如图所示(部分夹持装置未画出)。
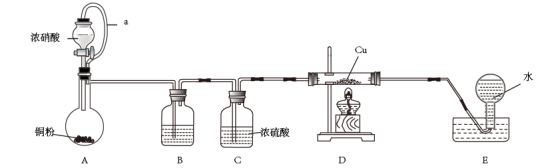
请回答下列问题:
(1)装置A中盛放铜粉的仪器名称为_______ ,a管的作用是_______ ,该装置中发生反应的离子方程式为_______ 。
(2)装置B中试剂为_______ ,装置E的作用是_______ 。
(3)实验开始时,先打开A中分液漏斗活塞,过一会儿,点燃D处酒精灯,这样操作的目的是_______ ,当Cu充分反应,实验结束时,下列操作中应首先进行的操作是_______ (填序号)。
①停止滴加浓硝酸 ②熄灭酒精灯 ③从E装置中取出导气管
(4)为了探究氧化产物是否含有Cu2O,取少量完全反应后的产物,进行如下实验:
(甲)加入足量的稀硝酸,观察是否完全溶解
(乙)加入足量的稀硫酸,观察是否完全溶解
(丙)加入足量的浓硝酸,观察是否完全溶解
(丁)在加热条件下通入乙醇蒸气,观察固体是否变为红色
其中,能达到实验目的的是_______ (填代号)。
(5)若氧化产物为CuO和Cu2O的混合物,为测定其组成,取混合物5.92g与足量稀硝酸反应,测得生成448mL标准状况下NO气体,则混合物中CuO和Cu2O的物质的量之比为_______ 。

请回答下列问题:
(1)装置A中盛放铜粉的仪器名称为
(2)装置B中试剂为
(3)实验开始时,先打开A中分液漏斗活塞,过一会儿,点燃D处酒精灯,这样操作的目的是
①停止滴加浓硝酸 ②熄灭酒精灯 ③从E装置中取出导气管
(4)为了探究氧化产物是否含有Cu2O,取少量完全反应后的产物,进行如下实验:
(甲)加入足量的稀硝酸,观察是否完全溶解
(乙)加入足量的稀硫酸,观察是否完全溶解
(丙)加入足量的浓硝酸,观察是否完全溶解
(丁)在加热条件下通入乙醇蒸气,观察固体是否变为红色
其中,能达到实验目的的是
(5)若氧化产物为CuO和Cu2O的混合物,为测定其组成,取混合物5.92g与足量稀硝酸反应,测得生成448mL标准状况下NO气体,则混合物中CuO和Cu2O的物质的量之比为
您最近半年使用:0次
5 . 铜器久置,表面会生成一层绿色固体,为了解铜在空气中的腐蚀情况,某化学兴趣小组收集家中铜器表面的绿色固体进行探究。查阅相关资料后,猜想该绿色物质可能是铜的碳酸盐。
该小组同学利用下图装置进行实验(部分夹持仪器略)。
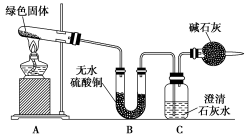
①对试管内的绿色固体进行加热,至完全分解,观察到A装置中绿色固体逐渐变成黑色,B装置中无水硫酸铜变成蓝色,C装置中澄清石灰水变浑浊。
②取少量加热后生成的黑色固体于试管中,加入稀硫酸,观察到黑色固体逐渐溶解,溶液变成蓝色。
③取少量上述蓝色溶液于试管中,浸入一根洁净的铁丝。观察到铁丝表面有红色物质析出。
请回答下列问题:
(1)绿色固体中含有的元素是________________________________________________ 。
(2)加热后试管中剩余的黑色物质是_________________________________________________ 。
(3)假设该绿色物质是一种纯净物,则其化学式可能是______________ ,加热分解的化学方程式为_______________________________________________________________________________________ 。
(4)上述实验步骤③中的反应的离子方程式为________________________________________ 。
(5)实验装置最后的干燥管的作用是___________________________________________________ 。
(6)如果将B、C两装置对调,能否达到实验目的______ (填“能”或“不能”),为什么?_____________________________________________________________________________________________________________ 。
该小组同学利用下图装置进行实验(部分夹持仪器略)。

①对试管内的绿色固体进行加热,至完全分解,观察到A装置中绿色固体逐渐变成黑色,B装置中无水硫酸铜变成蓝色,C装置中澄清石灰水变浑浊。
②取少量加热后生成的黑色固体于试管中,加入稀硫酸,观察到黑色固体逐渐溶解,溶液变成蓝色。
③取少量上述蓝色溶液于试管中,浸入一根洁净的铁丝。观察到铁丝表面有红色物质析出。
请回答下列问题:
(1)绿色固体中含有的元素是
(2)加热后试管中剩余的黑色物质是
(3)假设该绿色物质是一种纯净物,则其化学式可能是
(4)上述实验步骤③中的反应的离子方程式为
(5)实验装置最后的干燥管的作用是
(6)如果将B、C两装置对调,能否达到实验目的
您最近半年使用:0次
6 . 下列操作或装置能达到实验目的的是
A.收集NO2 并防止其污染环境 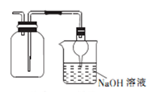 | B.称取一定量的氢氧化钠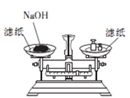 | C.验证浓硫酸与铜反应后产物中是否含有铜离子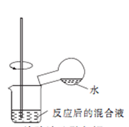 | D.制取碳酸氢钠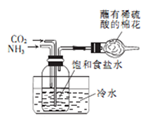 |
您最近半年使用:0次
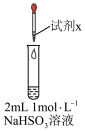
7 . 实验小组对NaHSO3溶液分别与CuCl2、CuSO4溶液的反应进行探究。
已知:Cu+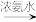 [Cu(NH3)2]+(无色溶液)
[Cu(NH3)2]+(无色溶液) [Cu(NH3)4]2+(深蓝色溶液)
[Cu(NH3)4]2+(深蓝色溶液)
(1)推测实验I产生的无色气体为SO2,实验证实推测正确:用蘸有碘水的淀粉试纸接近试管口,观察到蓝色褪去。反应的离子方程式为___________ 。
(2)对实验I产生SO2的原因进行分析,提出假设:
假设a:Cu2+水解使溶液中c(H+)增大;
假设b:Cl-存在时,Cu2+与 反应生成CuCl白色沉淀,溶液中c(H+)增大。
反应生成CuCl白色沉淀,溶液中c(H+)增大。
①假设a不合理,实验证据是___________ 。
②实验表明假设b合理,实验I反应的离子方程式有___________ 、 。
。
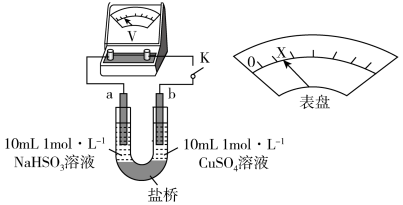
(3)对比实验I、II,根据半反应就物质的氧化性还原性提出假设:Cl-___________ 。
下述实验III证实了假设合理,装置如下图。___________ (补全实验操作及现象)。
(4)将实验I的溶液静置24小时或加热后,得到红色沉淀。经检验,红色沉淀中含有Cu+、Cu2+和 。
。
①通过实验IV证实红色沉淀中含有Cu+和Cu2+。
实验IV:证实红色沉淀中含有Cu+的实验证据是___________ 。___________ 。
②有同学认为实验IV不足以证实红色沉淀中含有Cu2+,设计实验IV的对比实验Ⅴ,证实了Cu2+的存在。实验V的方案和现象是:___________ 。
| 实验 | 装置 | 试剂x | 操作及现象 |
| I |
| 1 mol/LCuCl2溶液 | 加入2mLCuCl2溶液,得到绿色溶液,30s时有无色气泡和白色沉淀产生,上层溶液颜色变浅 |
| II | 1 mol/LCuSO4溶液 | 加入2mL CuSO4溶液,得到绿色溶液,3分钟未见明显变化 |
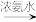 [Cu(NH3)2]+(无色溶液)
[Cu(NH3)2]+(无色溶液) [Cu(NH3)4]2+(深蓝色溶液)
[Cu(NH3)4]2+(深蓝色溶液)(1)推测实验I产生的无色气体为SO2,实验证实推测正确:用蘸有碘水的淀粉试纸接近试管口,观察到蓝色褪去。反应的离子方程式为
(2)对实验I产生SO2的原因进行分析,提出假设:
假设a:Cu2+水解使溶液中c(H+)增大;
假设b:Cl-存在时,Cu2+与
 反应生成CuCl白色沉淀,溶液中c(H+)增大。
反应生成CuCl白色沉淀,溶液中c(H+)增大。①假设a不合理,实验证据是
②实验表明假设b合理,实验I反应的离子方程式有
 。
。(3)对比实验I、II,根据半反应就物质的氧化性还原性提出假设:Cl-
下述实验III证实了假设合理,装置如下图。
(4)将实验I的溶液静置24小时或加热后,得到红色沉淀。经检验,红色沉淀中含有Cu+、Cu2+和
 。
。①通过实验IV证实红色沉淀中含有Cu+和Cu2+。
实验IV:证实红色沉淀中含有Cu+的实验证据是
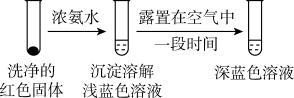
②有同学认为实验IV不足以证实红色沉淀中含有Cu2+,设计实验IV的对比实验Ⅴ,证实了Cu2+的存在。实验V的方案和现象是:
您最近半年使用:0次
名校
解题方法
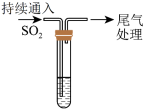
8 . 某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
已知:CuCl为白色固体,难溶于水,能溶于浓盐酸。下列说法不正确的是
| 装置 |
| |
| 序号 | 试管中的药品 | 现象 |
| 实验Ⅰ | 1.5mL1mol·L-1CuSO4溶液和3.5mL1mol·L-1NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
| 实验Ⅱ | 1.5mL1mol·L-1CuCl2溶液和3.5mL1mol·L-1NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
| A.取少量Cu2O固体于试管中,加入5mL0.1mol·L-1NaOH溶液,持续通入SO2,若试管底部有少量紫红色固体,溶液呈绿色,证明实验Ⅰ中砖红色沉淀为Cu2O |
| B.将实验Ⅱ中白色沉淀洗涤干净后,加入浓盐酸,沉淀溶解,然后加入蒸馏水,产生白色沉淀,证明白色沉淀为CuCl |
| C.实验Ⅱ与实验Ⅰ现象不同是因为阴离子不同造成的 |
D.实验Ⅰ、Ⅱ中不一定生成了SO |
您最近半年使用:0次
名校
9 . 用如图装置(搅拌装置略)探究溶液离子浓度变化,灯光变化不可能 出现“亮→暗(或灭)→亮”现象的是
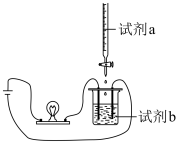

| 选项 | A | B | C | D |
| 试剂a |  |  |  |  |
| 试剂b |  | 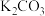 |  |  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
10 . 胆矾(CuSO4·5H2O)是一种重要化工原料。某研究小组以生锈的铜屑为原料(主要成分是Cu,含有少量的油污、CuO、CuCO3、Cu(OH)2)制备胆矾流程如图,下列说法不正确的是
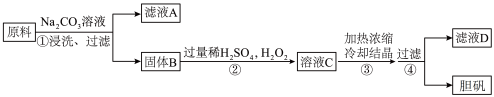

| A.步骤②中包含了氧化还原反应,氧化剂与还原剂的物质的量比为1∶1 |
| B.步骤③④得到的胆矾晶体,可以用水进行洗涤干燥 |
| C.往滤液D中加入淀粉-KI溶液,无明显现象 |
| D.将25g胆矾晶体与75g水混合,配制得到质量分数为16%的硫酸铜溶液 |
您最近半年使用:0次