1 . 2022北京冬奥会采用氢气作为火炬燃料,选择氢能汽车作为赛事交通服务用车,充分体现了绿色奥运的理念。已知
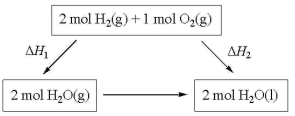
下列说法不正确 的是

下列说法
A. |
B. 的过程中, 的过程中, , , |
C.2mol 和1mol 和1mol 的总能量大于2mol 的总能量大于2mol 的总能量 的总能量 |
D.化学反应的 ,只与反应体系的始态和终态有关,与反应途径无关 ,只与反应体系的始态和终态有关,与反应途径无关 |
您最近半年使用:0次
2 . C和 在生产、生活、科技中是重要的燃料。
在生产、生活、科技中是重要的燃料。
①
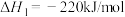
②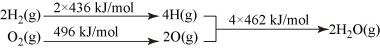
下列推断正确的是
 在生产、生活、科技中是重要的燃料。
在生产、生活、科技中是重要的燃料。①

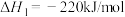
②
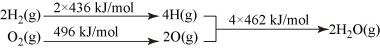
下列推断正确的是
A. 的燃烧热为 的燃烧热为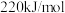 |
B.  |
C.  |
D.欲分解2mol ,至少需要提供 ,至少需要提供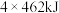 的热量 的热量 |
您最近半年使用:0次
3 . 当今世界,“碳达峰”“碳中和”已经成为了环保领域的“热词”,我国力争于2030前做到碳达峰,2060年前实现碳中和。深度脱碳(CO2)的资源化利用能有效减少CO2排放,充分利用碳资源。
I.大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧,CH4与CO2重整是CO2利用的研究热点之一。该重整反应体系主要涉及以下反应:
(a)CH4(g) C(s)+2H2(g) ΔH1=akJ·mol-1
C(s)+2H2(g) ΔH1=akJ·mol-1
(b)CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=bkJ·mol-1
CO(g)+H2O(g) ΔH2=bkJ·mol-1
(c)2CO(g) CO2(g)+C(s) ΔH3=ckJ·mol-1
CO2(g)+C(s) ΔH3=ckJ·mol-1
(d)······
(1)根据盖斯定律,反应CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH =
2CO(g)+2H2(g) ΔH =_______ kJ·mol-1。
II.利用电化学方法可实现二氧化碳的资源化利用。
(2)原电池法:我国科学家研究Li—CO2电池,取得重大突破。该电池发生的原电池反应为:4Li+3CO2=2Li2CO3+C。
①在Li—CO2电池中,Li为单质锂片,是该原电池的_______ (填“正”或“负”)极。
②CO2电还原过程依次按以下四个步骤进行,写出步骤I的电极反应式
i._______
ii.C2O =CO
=CO +CO2
+CO2
iii.CO2+2CO =2CO
=2CO +C
+C
iv.CO +2Li+=Li2CO3
+2Li+=Li2CO3
(3)电解法:如电解CO2制HCOOK。该原理示意图如下:
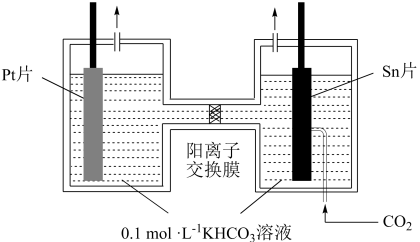
①Pt片为电解池的_______ 极。
②写出CO2还原为HCOO-的电极反应式:_______ 。
③电解一段时间后,阳极区的KHCO3溶液浓度降低,其原因是_______ 。
I.大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧,CH4与CO2重整是CO2利用的研究热点之一。该重整反应体系主要涉及以下反应:
(a)CH4(g)
 C(s)+2H2(g) ΔH1=akJ·mol-1
C(s)+2H2(g) ΔH1=akJ·mol-1(b)CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=bkJ·mol-1
CO(g)+H2O(g) ΔH2=bkJ·mol-1(c)2CO(g)
 CO2(g)+C(s) ΔH3=ckJ·mol-1
CO2(g)+C(s) ΔH3=ckJ·mol-1(d)······
(1)根据盖斯定律,反应CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH =
2CO(g)+2H2(g) ΔH =II.利用电化学方法可实现二氧化碳的资源化利用。
(2)原电池法:我国科学家研究Li—CO2电池,取得重大突破。该电池发生的原电池反应为:4Li+3CO2=2Li2CO3+C。
①在Li—CO2电池中,Li为单质锂片,是该原电池的
②CO2电还原过程依次按以下四个步骤进行,写出步骤I的电极反应式
i.
ii.C2O
 =CO
=CO +CO2
+CO2iii.CO2+2CO
 =2CO
=2CO +C
+Civ.CO
 +2Li+=Li2CO3
+2Li+=Li2CO3(3)电解法:如电解CO2制HCOOK。该原理示意图如下:

①Pt片为电解池的
②写出CO2还原为HCOO-的电极反应式:
③电解一段时间后,阳极区的KHCO3溶液浓度降低,其原因是
您最近半年使用:0次
4 . 甲醇水蒸气重整制氢方法是目前比较成熟的制氢方法,且具有良好的应用前景。依据图示关系,下列说法不正确 的是
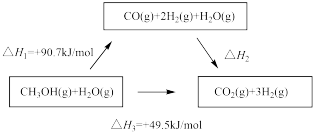

| A.甲醇与水蒸气发生的反应是吸热反应 |
| B.1molCO(g)和1molH2O(g)的总能量高于1molCO2(g)和1molH2(g) 总能量 |
| C.化学反应的ΔH,只与反应体系的始态和终态有关,与反应途径无关 |
| D.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=ΔH3-ΔH1 |
您最近半年使用:0次
5 . 多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃时(各物质均为气态),甲醇与水在钢基催化剂上的反应机理相能量图如下:
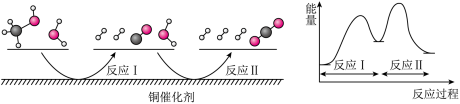
下列说法正确的是( )

下列说法正确的是( )
| A.反应II的热化学方程式为:CO(g)+H2O(g)→H2(g)+CO2(g) -Q kJ(Q>0) |
| B.1 mol CH3OH(g)和l mol H2O(g)的总能量大于l mol CO2(g)和3 mol H2(g)的总能量 |
| C.选择优良的催化剂降低反应I和II的活化能,有利于减少过程中的能耗 |
| D.CO(g)在反应中生成又消耗,CO(g)可认为是催化剂 |
您最近半年使用:0次
2020-10-23更新
|
509次组卷
|
22卷引用:北京市延庆区2019-2020学年高二下学期期末考试化学试题
北京市延庆区2019-2020学年高二下学期期末考试化学试题北京市石景山区2020届高三第一次模拟化学试题(已下线)北京市2019-2020学年高三各区一模化学考试分类汇编 选择题:热化学 电化学天津市红桥区2020届高三第二次模拟考试化学试题北京市北京师范大学燕化附属中学2019-2020 学年高二下学期期末考试化学试题广州市天河中学2019—2020学年高二下学期期末测试化学试卷山西省朔州市怀仁市第一中学校云东校区2019-2020学年高二下学期期末考试化学试题上海市复旦大学附属中学2021届高三上学期第一次教学质量检测化学试题吉林省长春市第一五一中学2020-2021学年高二上学期第一次月考化学试题(希望班)江西省赣州市十五县市十六校2020-2021学年高二上学期期中联考化学试题(已下线)押全国卷理综第13题 反应机理图分析、能垒图分析等创新题型及阿伏伽德罗常数-备战2021年高考化学临考题号押题(课标全国卷)(已下线)专题1.1.2 热化学方程式的书写(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)福建省武平县第一中学2021-2022学年高二上学期10月月考化学试题江西省赣州市2021-2022学高三上学期期末考试化学试题北京市日坛中学2021-2022学年高二上学期期中考试化学试题北京市西城区第一六一中学2022届高三考前热身测试化学试题(已下线)第15讲 化学反应的热效应 (练)-2023年高考化学一轮复习讲练测(新教材新高考)湖北省武汉市青山区2021-2022学年高二上学期期末考试化学试题上海行知中学2022-2023学年高三上学期第一次月考化学试题广东省广州市玉岩中学2022-2023学年高二上学期10月月考化学试题河南省鹤壁市高中2022-2023学年高三上学期第三次模拟考试化学试题(已下线)上海市静安区2022-2023学年高三下学期二模变式题(选择题16-20)
6 . CO2的捕集和利用因为其工业价值和减少CO2排放的环境意义而受到广泛关注。
(1)下列物质中可以作为CO2捕获剂的是______ 。
A.NH4Cl B.Na2CO3 C.HOCH2CH2OH D.HOCH2CH2NH2 E.(NH4)2CO3
(2)在Cu/ZnO催化剂条件下,CO2与H2可生成CH3OH,CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1=-53.7kJ.mol-1。科研人员提出了该催化反应历程的示意图如下,其中CO是重要的中间产物。
CH3OH(g)+H2O(g) ΔH1=-53.7kJ.mol-1。科研人员提出了该催化反应历程的示意图如下,其中CO是重要的中间产物。
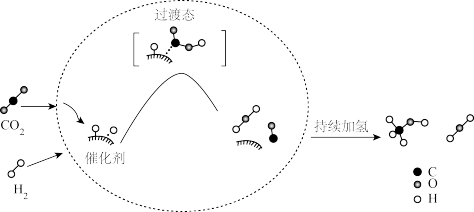
已知:第一步反应I:CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41kJ.mol-1
CO(g)+H2O(g) ΔH2=+41kJ.mol-1
①第二步反应的热化学方程式是______ 。
②CO2与H2生成CH3OH反应的平衡常数表达式K=______ 。
③下图是其他条件一定时,反应温度对CO2平衡转化率影响的曲线,请结合化学用语说明温度低于350℃时,CO2的平衡转化率随温度变化的原因是______ 。

(3)O2辅助的Al—CO2电池工作原理如图所示。该电池电容量大,能有效利用CO2。电池反应产物Al2(C2O4)3是重要的化工原料。电池原理如下:
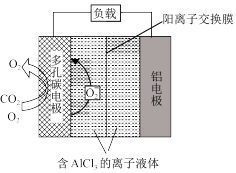
①O2作为正极反应的催化剂,可能的催化过程如下,将i补充完整,并写出ii的离子方程式。
i.O2+_____ ===_____ ;
ii._______ 。
②结合电极反应式简述Al2(C2O4)3的生成______ 。
(1)下列物质中可以作为CO2捕获剂的是
A.NH4Cl B.Na2CO3 C.HOCH2CH2OH D.HOCH2CH2NH2 E.(NH4)2CO3
(2)在Cu/ZnO催化剂条件下,CO2与H2可生成CH3OH,CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1=-53.7kJ.mol-1。科研人员提出了该催化反应历程的示意图如下,其中CO是重要的中间产物。
CH3OH(g)+H2O(g) ΔH1=-53.7kJ.mol-1。科研人员提出了该催化反应历程的示意图如下,其中CO是重要的中间产物。
已知:第一步反应I:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=+41kJ.mol-1
CO(g)+H2O(g) ΔH2=+41kJ.mol-1①第二步反应的热化学方程式是
②CO2与H2生成CH3OH反应的平衡常数表达式K=
③下图是其他条件一定时,反应温度对CO2平衡转化率影响的曲线,请结合化学用语说明温度低于350℃时,CO2的平衡转化率随温度变化的原因是

(3)O2辅助的Al—CO2电池工作原理如图所示。该电池电容量大,能有效利用CO2。电池反应产物Al2(C2O4)3是重要的化工原料。电池原理如下:

①O2作为正极反应的催化剂,可能的催化过程如下,将i补充完整,并写出ii的离子方程式。
i.O2+
ii.
②结合电极反应式简述Al2(C2O4)3的生成
您最近半年使用:0次
解题方法
7 . 合理的利用吸收工业产生的废气CO2可以减少污染,变废为宝。
(1)用CO2可以生产燃料甲醇。
①写出甲醇的官能团名称____________ 。
已知:CO2(g)+3H2(g) ⇌CH3OH(g)+H2O(l) △H=-49.0kJ•mol-1;一定条件下,向体积固定为1 L的密闭容器中充入1mol CO2和3mol H2 ,测得CO2和CH3OH(g)的浓度随时间变化曲线如下图所示。

②反应开始至第3分钟时,反应速率v(H2)=________ mol/(L·min)。
③该条件下,该反应的平衡常数表达式为________ ,CO2的平衡转化率是________ ;
(2)用CO2合成二甲醚(CH3OCH3)。
①CO2 催化加氢合成二甲醚的过程中主要发生下列反应:
反应I:CO2(g) + H2(g)⇌CO(g) + H2O(g) ∆H= +41.2 kJ·mol-1
反应II: 2CO2(g) + 6H2(g)⇌CH3OCH3(g) + 3H2O(g) ∆H = - 122.5 kJ·mol-1
其中,反应II 分以下a、b两步完成,请写出反应a的热化学方程式。
a._________
b.2CH3OH(g)⇌CH3OCH3(g) + H2O(g) ∆H = -23.5 kJ·mol-1
②L(L1、L2)、X分别代表压强或温度,下图表示L一定时,反应II中二甲醚的平衡产率随X变化的关系,其中X代表的物理量是______ 。判断L1、L2的大小,并简述理由:________ 。
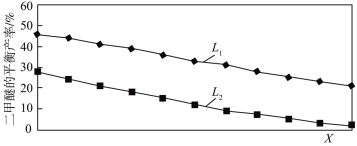
(3) 恒压时,在CO2和H2起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性(CH3OCH3的选择性= )随温度变化如下图。
)随温度变化如下图。
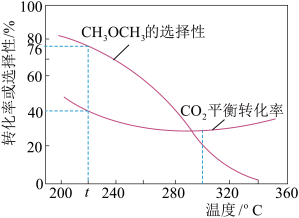
①t℃时,起始投入a molCO2,b mol H2,达到平衡时反应II消耗的H2的物质的量为______ mol。
②温度高于300℃,CO2平衡转化率随温度升高而增大的原因是_________ 。
(1)用CO2可以生产燃料甲醇。
①写出甲醇的官能团名称
已知:CO2(g)+3H2(g) ⇌CH3OH(g)+H2O(l) △H=-49.0kJ•mol-1;一定条件下,向体积固定为1 L的密闭容器中充入1mol CO2和3mol H2 ,测得CO2和CH3OH(g)的浓度随时间变化曲线如下图所示。

②反应开始至第3分钟时,反应速率v(H2)=
③该条件下,该反应的平衡常数表达式为
(2)用CO2合成二甲醚(CH3OCH3)。
①CO2 催化加氢合成二甲醚的过程中主要发生下列反应:
反应I:CO2(g) + H2(g)⇌CO(g) + H2O(g) ∆H= +41.2 kJ·mol-1
反应II: 2CO2(g) + 6H2(g)⇌CH3OCH3(g) + 3H2O(g) ∆H = - 122.5 kJ·mol-1
其中,反应II 分以下a、b两步完成,请写出反应a的热化学方程式。
a.
b.2CH3OH(g)⇌CH3OCH3(g) + H2O(g) ∆H = -23.5 kJ·mol-1
②L(L1、L2)、X分别代表压强或温度,下图表示L一定时,反应II中二甲醚的平衡产率随X变化的关系,其中X代表的物理量是

(3) 恒压时,在CO2和H2起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性(CH3OCH3的选择性=
 )随温度变化如下图。
)随温度变化如下图。
①t℃时,起始投入a molCO2,b mol H2,达到平衡时反应II消耗的H2的物质的量为
②温度高于300℃,CO2平衡转化率随温度升高而增大的原因是
您最近半年使用:0次
8 . 氢气作为清洁能源有着广泛的应用前景,采用天然气制备氢气的流程如下。
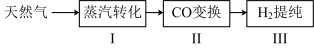
请回答下列问题:
Ⅰ.蒸汽转化:在催化剂的作用下,水蒸气将CH4氧化,结合图表信息回答问题。
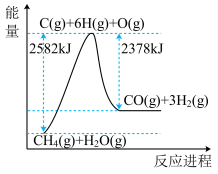
(1)该过程的热化学方程式是__________ 。
(2)平衡混合物中CO的体积分数与压强的关系如图所示,判断T1和T2的大小关系:T1_______ T2(填“>”“<”或“=”),并说明理由__________ 。

(3)一定温度下,在1L恒容的密闭容器中充入1mol CH4和1mol水蒸气充分反应达平衡后,测得反应前后容器中气体的物质的量之比是3:4,计算该条件下反应的平衡常数为______________ 。
Ⅱ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅲ.模拟H2提纯工艺:将CO2和H2分离得到H2的过程如下:
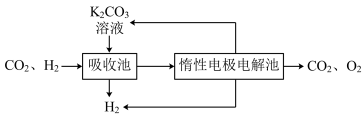
依据图示信息回答:
(4)吸收池中发生反应的离子方程式是_________ 。
(5)写出电解池中阳极发生的电极反应式________ ;结合化学用语说明K2CO3溶液再生的原因_________ 。

请回答下列问题:
Ⅰ.蒸汽转化:在催化剂的作用下,水蒸气将CH4氧化,结合图表信息回答问题。

(1)该过程的热化学方程式是
(2)平衡混合物中CO的体积分数与压强的关系如图所示,判断T1和T2的大小关系:T1

(3)一定温度下,在1L恒容的密闭容器中充入1mol CH4和1mol水蒸气充分反应达平衡后,测得反应前后容器中气体的物质的量之比是3:4,计算该条件下反应的平衡常数为
Ⅱ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅲ.模拟H2提纯工艺:将CO2和H2分离得到H2的过程如下:

依据图示信息回答:
(4)吸收池中发生反应的离子方程式是
(5)写出电解池中阳极发生的电极反应式
您最近半年使用:0次
2020-04-20更新
|
173次组卷
|
3卷引用:北京市延庆区2020届高三统测化学试题



