名校
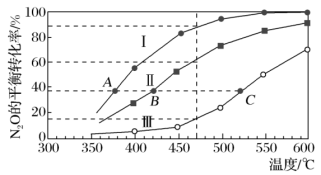
1 . 现有反应2N2O(g) 2N2(g)+O2(g),在四个恒容密闭容器中按下表充入气体进行反应,容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图所示。下列说法正确的是
2N2(g)+O2(g),在四个恒容密闭容器中按下表充入气体进行反应,容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图所示。下列说法正确的是
 2N2(g)+O2(g),在四个恒容密闭容器中按下表充入气体进行反应,容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图所示。下列说法正确的是
2N2(g)+O2(g),在四个恒容密闭容器中按下表充入气体进行反应,容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图所示。下列说法正确的是| 容器 | 容积/L | 起始物质的量/mol | ||
| N2O | N2 | O2 | ||
| Ⅰ | V1 | 0.1 | 0 | 0 |
| Ⅱ | 1.0 | 0.1 | 0 | 0 |
| Ⅲ | V3 | 0.1 | 0 | 0 |
| Ⅳ | 1.0 | 0.06 | 0.06 | 0.04 |

| A.该反应的正反应放热 |
| B.相同温度下,起始反应速率:v(Ⅰ)>v(Ⅱ) |
| C.图中A、B、C三点处,三个容器内的压强:pA(Ⅰ)<pB(Ⅱ)<pC(Ⅲ) |
| D.若Ⅳ在470℃进行反应,反应逆向进行 |
您最近半年使用:0次
2024-02-03更新
|
132次组卷
|
2卷引用:湖南省衡阳市第八中学2024届高三模拟预测信息卷(一)化学试题
2 .  是常见的环境污染性气体。一定温度下,向三个容积不等的恒容密闭容器中分别投入
是常见的环境污染性气体。一定温度下,向三个容积不等的恒容密闭容器中分别投入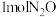 ,发生反应:
,发生反应: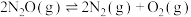 。反应相同时间内,三个容器中
。反应相同时间内,三个容器中 的转化率如图中A、B、C三点。下列叙述正确的是
的转化率如图中A、B、C三点。下列叙述正确的是

 是常见的环境污染性气体。一定温度下,向三个容积不等的恒容密闭容器中分别投入
是常见的环境污染性气体。一定温度下,向三个容积不等的恒容密闭容器中分别投入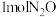 ,发生反应:
,发生反应: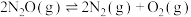 。反应相同时间内,三个容器中
。反应相同时间内,三个容器中 的转化率如图中A、B、C三点。下列叙述正确的是
的转化率如图中A、B、C三点。下列叙述正确的是
A.A点的 小于C点的 小于C点的 |
B.C点加入适当催化剂,不能提高 的转化率 的转化率 |
C.若B点为平衡点,在该温度下,反应的平衡常数 |
D.在恒温恒容下,向A点平衡体系中再充入一定量的 ,与原平衡相比, ,与原平衡相比, 的平衡转化率减小 的平衡转化率减小 |
您最近半年使用:0次
名校
3 . 一定温度下,在3个1.0L的恒容密闭容器中分别进行反应2X(g)+Y(g)⇌Z(g) ΔH,达到平衡。相关数据如表。下列说法不正确 的是
| 容器 | 温度/K | 物质的起始浓度/mol·L-1 | 物质的平衡浓度/mol·L-1 | ||
| c(X) | c(Y) | c(Z) | c(Z) | ||
| I | 400 | 0.20 | 0.10 | 0 | 0.080 |
| II | 400 | 0.40 | 0.20 | 0 | a |
| III | 500 | 0.20 | 0.10 | 0 | 0.025 |
| A.平衡时,X的转化率:II>I | B.平衡常数:K(II)=K(I) |
| C.达到平衡所需时间:III<I | D.a=0.16,ΔH<0 |
您最近半年使用:0次
名校
4 . 工业合成氨的原料气来源于化石燃料,如采用甲烷与二氧化碳反应:
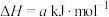 ,恒温、恒压条件下,向密闭容器中充入等物质的量的
,恒温、恒压条件下,向密闭容器中充入等物质的量的 和
和 ,测得
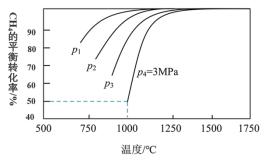
,测得 平衡转化率在不同反应条件(温度、压强)下变化情况如图所示,下列说法正确的是
平衡转化率在不同反应条件(温度、压强)下变化情况如图所示,下列说法正确的是

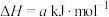 ,恒温、恒压条件下,向密闭容器中充入等物质的量的
,恒温、恒压条件下,向密闭容器中充入等物质的量的 和
和 ,测得
,测得 平衡转化率在不同反应条件(温度、压强)下变化情况如图所示,下列说法正确的是
平衡转化率在不同反应条件(温度、压强)下变化情况如图所示,下列说法正确的是
A.该原料气的制备反应为放热反应, |
B.压强关系: |
C.1000℃、 时的压强平衡常数 时的压强平衡常数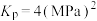 |
| D.恒温恒压条件下,充入He,平衡逆向移动 |
您最近半年使用:0次
名校
5 . 二氧化碳一甲烷重整反应制备合成气(H2+CO)是一种生产高附加值化学品的低碳过程。该过程存在如下化学反应:
①

②
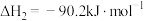
③
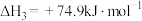
④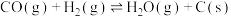
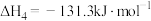
回答下列问题:
(1)
_______ ,反应①_______ 正向自发进行(填标号)。
A.低温下能 B.高温下能 C.任何温度下都能 D.任何温度下都不能
(2)反应体系总压强分别为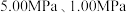 和
和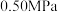 时,
时, 平衡转化率随反应温度变化如图所示,则代表反应体系总压强为
平衡转化率随反应温度变化如图所示,则代表反应体系总压强为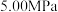 的曲线是
的曲线是_______ (填“Ⅰ”“Ⅱ”或“Ⅲ”),判断依据是_______ 。 时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升高,
时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升高, 的物质的量先增加后减少,主要原因是
的物质的量先增加后减少,主要原因是_______ 。 和
和 ,达到平衡时
,达到平衡时 的转化率为
的转化率为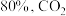 的转化率为
的转化率为 ,碳单质的物质的量为
,碳单质的物质的量为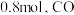 的物质的量为
的物质的量为_______  ,反应①用摩尔分数表示的平衡常数
,反应①用摩尔分数表示的平衡常数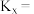
_______ (结果保留两位小数)。
上述平衡时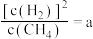 ,向体系通入
,向体系通入 气,重新达到平衡时,
气,重新达到平衡时,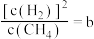 ,则a
,则a_______ b(填“>”“<”或“=”)。(已知反应 的
的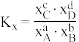 ,物质
,物质 的摩尔分数
的摩尔分数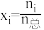 )
)
①


②

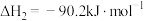
③

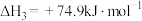
④
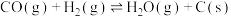
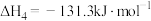
回答下列问题:
(1)

A.低温下能 B.高温下能 C.任何温度下都能 D.任何温度下都不能
(2)反应体系总压强分别为
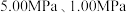 和
和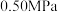 时,
时, 平衡转化率随反应温度变化如图所示,则代表反应体系总压强为
平衡转化率随反应温度变化如图所示,则代表反应体系总压强为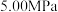 的曲线是
的曲线是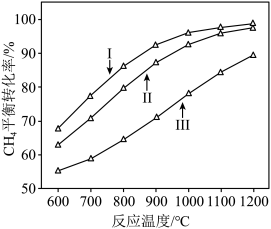
 时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升高,
时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升高, 的物质的量先增加后减少,主要原因是
的物质的量先增加后减少,主要原因是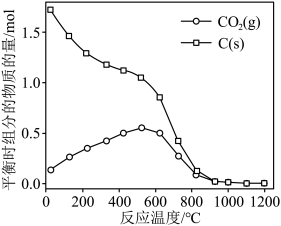
 和
和 ,达到平衡时
,达到平衡时 的转化率为
的转化率为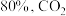 的转化率为
的转化率为 ,碳单质的物质的量为
,碳单质的物质的量为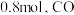 的物质的量为
的物质的量为 ,反应①用摩尔分数表示的平衡常数
,反应①用摩尔分数表示的平衡常数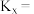
上述平衡时
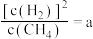 ,向体系通入
,向体系通入 气,重新达到平衡时,
气,重新达到平衡时,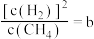 ,则a
,则a 的
的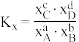 ,物质
,物质 的摩尔分数
的摩尔分数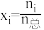 )
)
您最近半年使用:0次
2024-01-20更新
|
1066次组卷
|
4卷引用:湖南省长沙市雅礼中学2023-2024学年高三下学期月考(八)化学试题
湖南省长沙市雅礼中学2023-2024学年高三下学期月考(八)化学试题2024年1月河南普通高等学校招生考试适应性测试化学试题(已下线)T29-原理综合题(已下线)2024年1月“九省联考”河南卷真题完全解读与考后提升
12-13高二上·江西宜春·阶段练习
名校
解题方法
6 . 在一容积可变的密闭容器中加入一定量的X、Y,发生反应mX(g)⇌nY(g) ∆H=QkJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如表所示:
下列说法正确 的是
| 温度(℃) | c(Y)/(mol/L) | ||
| 1L | 2L | 4L | |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
| A.m>n |
| B.Q<0 |
| C.体积不变,温度升高,平衡向逆反应方向移动 |
| D.温度不变,压强增大,Y的质量分数减少 |
您最近半年使用:0次
2024-01-18更新
|
30次组卷
|
22卷引用:2011-2012学年湖南省望城县第一中学高二上学期期末质量检测化学试卷
(已下线)2011-2012学年湖南省望城县第一中学高二上学期期末质量检测化学试卷(已下线)2014-2015湖南省新化一中高二上学期期中化学试卷湖南师范大学附属中学2021-2022学年高一下学期期末考试化学试题湖南省常德市第一中学2023-2024学年高二上学期12月月考化学试题(已下线)2011-2012学年江西省上高二中高二上学期第三次月考化学试卷(已下线)2012-2013学年河北省邢台一中高一下学期第三次月考化学试卷(已下线)2013-2014学年黑龙江省哈师大附中高二上学期期中化学试卷(已下线)2013-2014学年安徽省屯溪一中高二上学期期中考试化学试卷(已下线)2014年高二化学人教版选修四 8化学平衡移动练习卷(已下线)2015届黑龙江省双鸭山市第一中学高三9月月考化学试卷2014-2015学年内蒙古包头市第一中学高一下学期期末考试化学试卷2015-2016浙江宁波效实中学高二上期中考试化学试题卷2015-2016学年云南省昆明三中高二下期中化学试卷2016-2017学年四川省成都开发区实验中学高二10月月考化学卷辽宁省大连市第二十四中学2017-2018学年高二上学期期中考试化学试题黑龙江省孙吴县第一中学2017-2018学年高二上学期期中考试化学试题步步为赢 高二化学暑假作业:作业九 化学反应速率和化学平衡吉林省白城市第一中学2018-2019学年高一下学期期末考试化学试题福建省三明市三地三校2020-2021学年高二上学期期中联考化学试题吉林省延边朝鲜族自治州汪清县第四中学2020-2021学年高二上学期期末考试化学试题黑龙江省鹤岗市第一中学2021-2022学年高二上学期期中考试化学试题海南省琼海市嘉积中学2023-2024学年高二上学期期末考试化学试题A卷
名校
7 . 反应
 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化的曲线如图所示。下列说法正确的是
的体积分数随压强变化的曲线如图所示。下列说法正确的是


 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化的曲线如图所示。下列说法正确的是
的体积分数随压强变化的曲线如图所示。下列说法正确的是
| A.X、Z两点气体的颜色:X比Z浅 |
| B.X、Y两点的反应速率:X<Y |
C. |
| D.X、Z两点气体的平均相对分子质量:X>Z |
您最近半年使用:0次
名校
8 . 在一定条件下,取一定量的A和B在恒容密闭容器中发生反应:aA(g)+bB(s)⇌mM(g)+nN(g) △H,达到平衡时,M的浓度与温度和容器容积的关系如图所示。下列有关判断正确的是
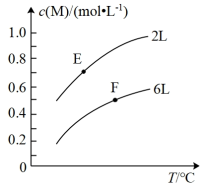

| A.ΔS<0 | B.达到平衡后,增大B的量将会提高A的转化率 |
| C.E点的平衡常数大于F点的平衡常数 | D.ΔH>0 |
您最近半年使用:0次
名校
解题方法
9 . 以 、
、 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:
①

②

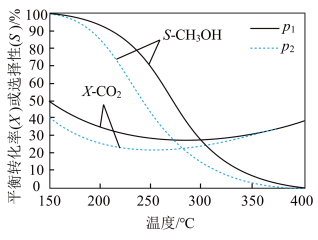
 的平衡转化率(
的平衡转化率(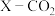 )、
)、 的选择性(
的选择性(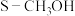 )随温度、压强变化如图。
)随温度、压强变化如图。
已知: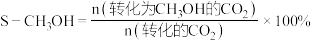
下列分析正确的是
 、
、 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:①


②


 的平衡转化率(
的平衡转化率(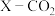 )、
)、 的选择性(
的选择性(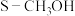 )随温度、压强变化如图。
)随温度、压强变化如图。
已知:
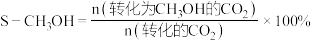
下列分析正确的是
A.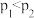 |
| B.反应①理论上高温下可自发进行 |
| C.反应②的平衡常数随温度升高而减小 |
D.初始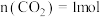 、 、 ,平衡后 ,平衡后 、 、 ,若只发生①、②,则 ,若只发生①、②,则 的平衡转化率为28% 的平衡转化率为28% |
您最近半年使用:0次
名校
解题方法
10 . 工业上利用 和
和 在催化剂的作用下合成
在催化剂的作用下合成 ,发生如下反应:
,发生如下反应:
 。现于一定条件下向
。现于一定条件下向 的密闭容器中充入一定量的
的密闭容器中充入一定量的 和
和 发生反应,测得在不同压强下平衡体系中
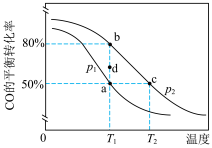
发生反应,测得在不同压强下平衡体系中 的转化率随温度的变化情况如图所示。下列说法正确的是
的转化率随温度的变化情况如图所示。下列说法正确的是
 和
和 在催化剂的作用下合成
在催化剂的作用下合成 ,发生如下反应:
,发生如下反应:
 。现于一定条件下向
。现于一定条件下向 的密闭容器中充入一定量的
的密闭容器中充入一定量的 和
和 发生反应,测得在不同压强下平衡体系中
发生反应,测得在不同压强下平衡体系中 的转化率随温度的变化情况如图所示。下列说法正确的是
的转化率随温度的变化情况如图所示。下列说法正确的是
A. , , |
B.在 、 、 条件下,d→a的过程中,正、逆反应速率之间的关系: 条件下,d→a的过程中,正、逆反应速率之间的关系: |
C.a、b、c三点对应的平衡常数 、 、 、 、 的大小关系是 的大小关系是 |
| D.b→c的过程,正反应速率变小,逆反应速率变大 |
您最近半年使用:0次
2023-11-21更新
|
340次组卷
|
2卷引用:湖南省衡阳市衡南县第一次联考2023-2024学年高三上学期11月期中化学试题



