名校
1 . 下图是可逆反应A+2B 2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断

 2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
| A.正反应是吸热反应 |
| B.若A、B是气体,则D是纯液体或固体 |
| C.逆反应是放热反应 |
| D.A、B、C、D均为气体 |
您最近一年使用:0次
2016-12-09更新
|
1965次组卷
|
25卷引用:广东省湛江市第二十一中学2019-2020学年高二上学期期中考试化学试题
广东省湛江市第二十一中学2019-2020学年高二上学期期中考试化学试题(已下线)2010-2011学年北京市密云二中高二下期3月份月考化学试卷(已下线)2011-2012学年福建师大附中高二上学期期末考试化学试卷(已下线)2015届黑龙江省双鸭山一中高三9月月考化学试卷2015届浙江省严州中学高三1月份阶段测试化学试卷江西省抚州市临川区第一中学2017-2018学年高二上学期第一次月考化学试题甘肃省武威第十八中学2017-2018学年高二上学期期末考试化学试题广西陆川县中学2017-2018学年高二下学期开学考试化学试题2018-2019学年人教版高中化学选修四章化学反应速率和化学平衡末综合测评(二)(已下线)2018年9月14日 《每日一题》人教选修4-影响化学平衡移动的因素(二)甘肃省岷县第二中学2018-2019学年高二上学期期中考试化学试题吉林省通化市第十四中学2018-2019学年高二上学期期末考试化学试题山西省运城市河津中学2019-2020学年高二9月月考化学试题吉林省吉林地区普通高中友好学校联合体第三十一届2019-2020学年高二上学期期中考试化学试题2020届人教版高三专题基础复习专题7《化学反应速率与化学平衡》测试卷宁夏贺兰县景博中学2019-2020学年高二上学期第一次月考化学试题湖北省巴东县第二高级中学2020-2021学年高二上学期期中考试化学试题湖南省长沙县第九中学2020-2021学年高二上学期第三次月考化学试题安徽省六安市新安中学2020-2021学年高二下学期入学考试(重点班)化学试题江西省赣州市兴国县第三中学2020-2021学年高二上学期第二次月考(兴国班)化学试题湖北省华中师范大学潜江附属中学2020-2021学年高一下学期5月月考化学试题广西玉林市普通中学2020-2021学年高二下学期月考化学试题江西省南城第二中学2021-2022学年高二上学期第一次月考化学试题江西省宜春中学2021-2022学年高二上学期第一次月考化学试题四川省遂宁中学校2020-2021学年高二上学期第二次月考化学试题
11-12高二上·广东·期中
2 . 在一容积为2 L的密闭容器内加入0.2 mol 的N2和0.6 mol 的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图:
2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图:
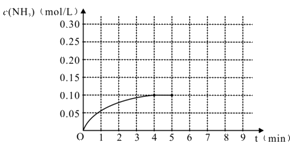
(1)根据右图,计算从反应开始到平衡时,平均反应速率v(NH3)为_________________ 。
(2)该反应的化学平衡常数表达式K=___________________ 。
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为________ 。
a. 0.20 mol/L b. 0.12 mol/L c. 0.10 mol/L d. 0.08 mol/L
(4)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡_________________________ 移动(填“向逆反应方向”、“向正反应方向”或“不”),化学平衡常数________________ (填“增大”、“减小”或“不变”)。
(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L)。请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。___________________
 2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图:
2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图:
(1)根据右图,计算从反应开始到平衡时,平均反应速率v(NH3)为
(2)该反应的化学平衡常数表达式K=
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为
a. 0.20 mol/L b. 0.12 mol/L c. 0.10 mol/L d. 0.08 mol/L
(4)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡
(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L)。请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。
您最近一年使用:0次
11-12高二上·广东·期中
名校
3 . 在可逆反应2A(g) + B(g) 2C(g) △H<0中,为了有利于A的利用,应采用的反应条件是
2C(g) △H<0中,为了有利于A的利用,应采用的反应条件是
 2C(g) △H<0中,为了有利于A的利用,应采用的反应条件是
2C(g) △H<0中,为了有利于A的利用,应采用的反应条件是| A.高温、高压 | B.高温、低压 |
| C.低温、低压 | D.适当温度、高压 |
您最近一年使用:0次
10-11高三·广东·阶段练习
4 . 随着氮氧化物污染的日趋严重,国家将于“十二五”期间加大对氮氧化物排放的控制力度。目前,用活性炭还原法处理氮氧化物是消除氮氧化物污染的有效方法。
⑴已知产物 A、B 都是参与大气循环的气体,请结合下表数据写出NO与活性炭反应的化学方程式:_______________
⑵某研究小组向某密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
①T1℃时,求该反应平衡常数(列出K的表达式,要求计算过程)____________ 。
②30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是______________ 。
③若30min后升高温度至T2℃,达到平衡时,容器中NO、A、B的浓度之比为5:3:3,则该反应的△H________ 0(填“>”、“=”或“<”)。
④压缩容器体积,增大压强对该反应的反应速率和平衡移动的影响是________ 。
⑴已知产物 A、B 都是参与大气循环的气体,请结合下表数据写出NO与活性炭反应的化学方程式:
⑵某研究小组向某密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度/mol•L-1 / 时间/min | NO | A | B |
0 | 0.10 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
50 | 0.032 | 0.034 | 0.017 |
①T1℃时,求该反应平衡常数(列出K的表达式,要求计算过程)
②30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是
③若30min后升高温度至T2℃,达到平衡时,容器中NO、A、B的浓度之比为5:3:3,则该反应的△H
④压缩容器体积,增大压强对该反应的反应速率和平衡移动的影响是
您最近一年使用:0次
10-11高二下·广东中山·阶段练习
5 . 在密闭容器中,进行下列反应: 2A(g)+B(g)+C(s) D(g)+E(g);△H>0 达到平衡后,下列说法中正确的是
D(g)+E(g);△H>0 达到平衡后,下列说法中正确的是
 D(g)+E(g);△H>0 达到平衡后,下列说法中正确的是
D(g)+E(g);△H>0 达到平衡后,下列说法中正确的是| A.若恒温定容情况下,充入一些稀有气体压强增大,但平衡不移动 |
| B.若恒温定压条件下,加入C(s),则B的转化率将增大 |
| C.若定容升温,在新平衡体系中A的质量分数将减小 |
| D.恒容,升高温度,正反应速率减小 |
您最近一年使用:0次
10-11高二上·山东济南·阶段练习
名校
6 . 在其他条件不变的情况下,能使合成氨反应进行程度增大的方法是
| A.升高温度 | B.减小压强 | C.使用催化剂 | D.及时分离出氨气 |
您最近一年使用:0次
2016-12-09更新
|
473次组卷
|
6卷引用:2010-2011学年广东省白云中学高二下学期期中考试化学试卷
(已下线)2010-2011学年广东省白云中学高二下学期期中考试化学试卷(已下线)2011届山东省济南市高三12月质量调研检测化学试卷B卷鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 第4节 化学反应条件的优化——工业合成氨高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第四节 化学反应的调控山东省枣庄市第八中学东校区2020-2021学年高二上学期第二次质量检测化学试题山西省朔州市怀仁县大地学校2020-2021学年高二上学期第一次月考化学试题
10-11高三上·广东深圳·阶段练习
7 . 在某一容积为2L的密闭容器内,加入0.2mol的CO和 0.2mol的 H2O(g),在催化剂存在的条件下恒温下发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g) ΔH=a kJ/mol(a>0)。反应达到平衡后,测得c(CO)∶c(CO2)=3∶2。下列说法正确的是
CO2(g)+H2(g) ΔH=a kJ/mol(a>0)。反应达到平衡后,测得c(CO)∶c(CO2)=3∶2。下列说法正确的是
 CO2(g)+H2(g) ΔH=a kJ/mol(a>0)。反应达到平衡后,测得c(CO)∶c(CO2)=3∶2。下列说法正确的是
CO2(g)+H2(g) ΔH=a kJ/mol(a>0)。反应达到平衡后,测得c(CO)∶c(CO2)=3∶2。下列说法正确的是| A.当体系压强不变时反应一定达到平衡 |
| B.反应放出的热量为 0.2a kJ |
| C.若升高温度,v(正)加快, v(逆)减慢,平衡正向移动 |
| D.在相同条件下再加入0.2mol的CO和0.2mol的 H2O(g),重新达平衡时,c(CO)∶c(CO2)=3∶2 |
您最近一年使用:0次
9-10高二下·福建福州·期末
名校
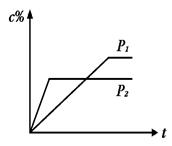
8 . 在温度相同,压强分别为P1和P2的条件下,A(g)+2B(g)  nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如图所示,下面结论正确的是
nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如图所示,下面结论正确的是
 nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如图所示,下面结论正确的是
nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如图所示,下面结论正确的是
| A.P1>P2,n<3 | B.P1<P2,n>3 |
| C.P1>P2,n>3 | D.P1<P2,n<3 |
您最近一年使用:0次
2016-12-09更新
|
784次组卷
|
10卷引用:2010年广东省东莞市光明、常平、厚街、万江四校高二上学期期中考试化学试卷
(已下线)2010年广东省东莞市光明、常平、厚街、万江四校高二上学期期中考试化学试卷(已下线)2010年福建省福州八中高二第二学期期末考试化学试题(已下线)2012-2013学年重庆市重庆一中高二上学期期中考试理科化学试卷2015届山东省桓台县第二中学高三1月检测化学试卷2016届山东省桓台第二中学高三上学期期中测试化学试卷2015-2016学年陕西省黄陵中学高二上学期期末考试化学试卷2015-2016学年陕西省延安市黄陵中学高二下期末化学试卷江西省南昌市进贤县第一中学2019-2020学年高二上学期期中考试化学试题(已下线)【南昌新东方】2019 进贤一中 高二上 期中新疆阿勒泰地区2018-2019学年高二上学期期末考试化学试题
10-11高二上·广东东莞·期中
9 . 对于反应:C(S) + H2O(g) CO(g) + H2(g) △H>0,为了提高C(S)的转化率,可采取的措施是
CO(g) + H2(g) △H>0,为了提高C(S)的转化率,可采取的措施是
 CO(g) + H2(g) △H>0,为了提高C(S)的转化率,可采取的措施是
CO(g) + H2(g) △H>0,为了提高C(S)的转化率,可采取的措施是| A.升高反应温度 | B.降低反应温度 |
| C.增大压强 | D.再加入一些C(S) |
您最近一年使用:0次
10-11高二上·广东东莞·期中
10 . 已知反应mA(g)+nB(g) xC(g)+yD(g),A的转化率RA与p、T的关系如图,根据图示可以得出的正确结论是
xC(g)+yD(g),A的转化率RA与p、T的关系如图,根据图示可以得出的正确结论是
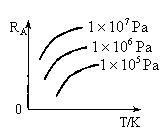
 xC(g)+yD(g),A的转化率RA与p、T的关系如图,根据图示可以得出的正确结论是
xC(g)+yD(g),A的转化率RA与p、T的关系如图,根据图示可以得出的正确结论是
| A.正反应放热 | B.正反应吸热 |
| C.m+n>x+y | D.m+n<x+y |
您最近一年使用:0次



